Clear Sky Science · fr
Bifidobacterium breve favorise la croissance et l’altération des lipides chez Trichomonas vaginalis de façon transitoire via un reprogrammation transcriptomique
Pourquoi de minuscules microbes vaginaux comptent
Le vagin humain abrite une communauté animée de microbes qui contribuent discrètement à empêcher les infections. Parmi ces habitants figurent des bactéries amies comme Bifidobacterium breve et un parasite indésirable, Trichomonas vaginalis, responsable de l’infection sexuellement transmissible non virale la plus fréquente au monde. Cette étude pose une question apparemment simple mais importante : lorsque ces deux microbes se rencontrent, les bactéries « bonnes » nous protègent-elles, ou donnent-elles par inadvertance un coup de pouce au parasite ?
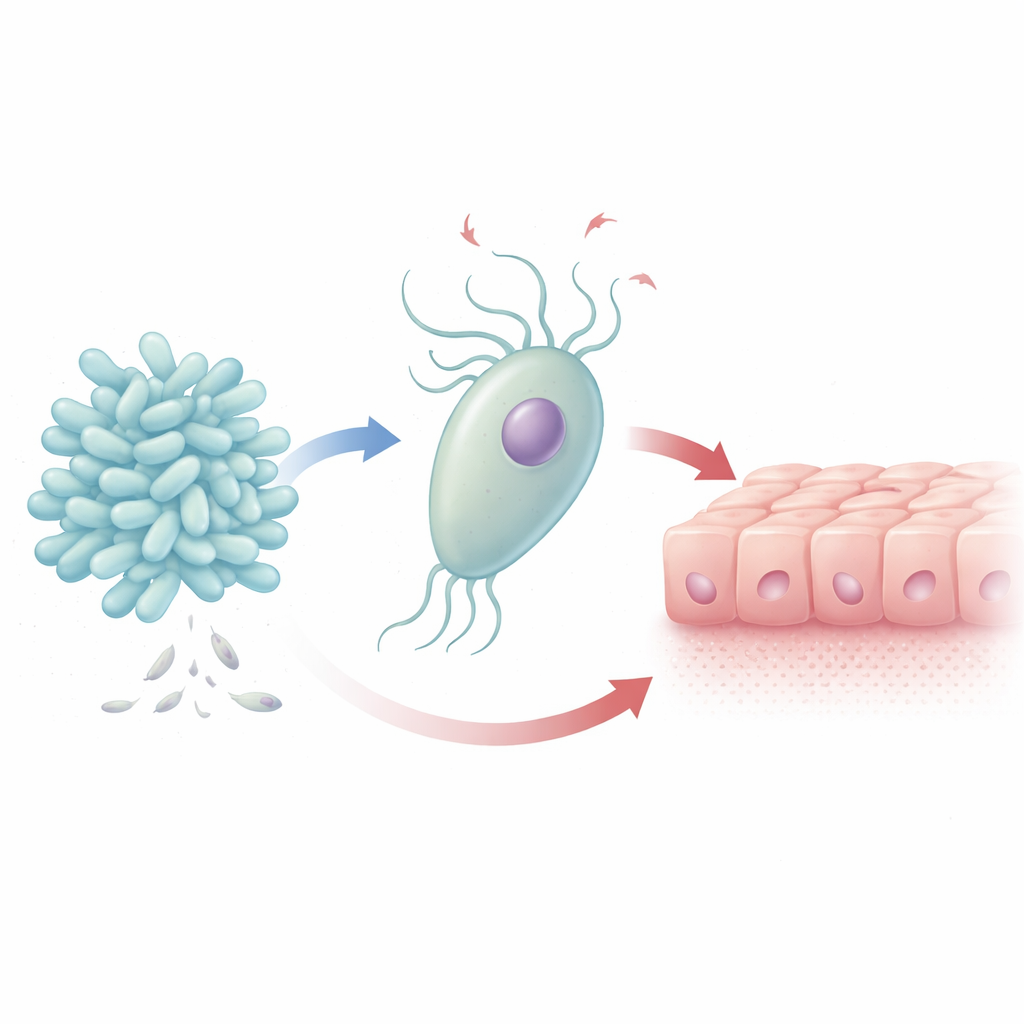
Un équilibre délicat dans le voisinage vaginal
Les femmes ayant un écosystème vaginal sain présentent généralement des communautés dominées par des bactéries protectrices qui produisent de l’acide lactique et contribuent à maintenir un pH bas, défavorable aux envahisseurs. B. breve est l’une de ces espèces utiles, tandis que T. vaginalis est un protozoaire flagellé associé non seulement à l’inconfort et à l’inflammation, mais aussi à un risque accru de transmission du VIH et d’infections persistantes à papillomavirus humain. Des études cliniques ont observé que les femmes infectées par T. vaginalis ont souvent moins de B. breve, ce qui suggère qu’une prolifération parasitaire s’accompagne de perturbations de l’équilibre microbien normal. Les auteurs ont cherché à déterminer si B. breve combat le parasite, l’ignore ou, de manière inattendue, le soutient.
Lorsque des bactéries « bonnes » rencontrent un parasite
En laboratoire, les chercheurs ont cultivé B. breve avec T. vaginalis dans des conditions anaérobies reproduisant l’environnement vaginal. En seulement quatre heures, le nombre de parasites a augmenté d’environ 20 %, tandis que la population bactérienne a chuté de plus d’un quart. Au microscope, B. breve s’agglutinait autour de la surface de T. vaginalis, ce qui suggère un contact physique direct entre les deux. Lorsque le parasite exposé à B. breve a ensuite été ajouté à des cellules cervicales humaines (cellules HeLa), les cellules hôtes n’ont montré aucune protection supplémentaire : la capacité du parasite à endommager la couche cellulaire n’a pas été réduite.
Tester la protection de l’hôte et l’inflammation
L’équipe a ensuite exploré deux scénarios réalistes : que se passe-t-il si B. breve se fixe sur les cellules vaginales avant l’arrivée du parasite, et que se passe-t-il si les deux atteignent les cellules en même temps ? Dans les deux cas, B. breve n’a pas réussi à protéger les cellules épithéliales des dommages causés par T. vaginalis. Les mesures de couverture et de morphologie cellulaire restaient essentiellement inchangées en présence ou en l’absence de B. breve. Lorsqu’ils ont mesuré les signaux inflammatoires, en particulier les cytokines IL-6 et IL-8, les scientifiques ont constaté que B. breve renforçait parfois ces réponses précoces. Plutôt que d’atténuer l’inflammation, une exposition simultanée ou préalable à B. breve tendait à produire des pics brefs de ces signaux, ce qui peut être à double tranchant — soutenant la défense immunitaire, mais pouvant aussi favoriser la survie du parasite.
Reprogrammer le parasite de l’intérieur
Pour comprendre comment le parasite lui‑même change en présence de B. breve, les chercheurs ont analysé les gènes activés ou réprimés chez T. vaginalis et ce qui arrivait à ses molécules liées aux lipides. Ils ont constaté que les gènes impliqués dans la réplication de l’ADN, le conditionnement des chromosomes et la production d’énergie étaient activés, ce qui concorde avec une croissance parasitaire accélérée. De manière importante, les gènes et voies liés à l’utilisation des acides gras — en particulier la gestion des acides gras à chaîne longue et des acides gras à chaîne courte comme le propionate — ont été fortement stimulés. Des mesures chimiques détaillées ont révélé que de nombreux acides gras à l’intérieur du parasite diminuaient après la co‑culture, suggérant que T. vaginalis consommait ces lipides comme carburant et matériau de construction. Ensemble, les données indiquent une brève « reprogrammation » métabolique dans laquelle le contact avec B. breve incite le parasite à utiliser davantage de lipides et à se diviser plus rapidement.
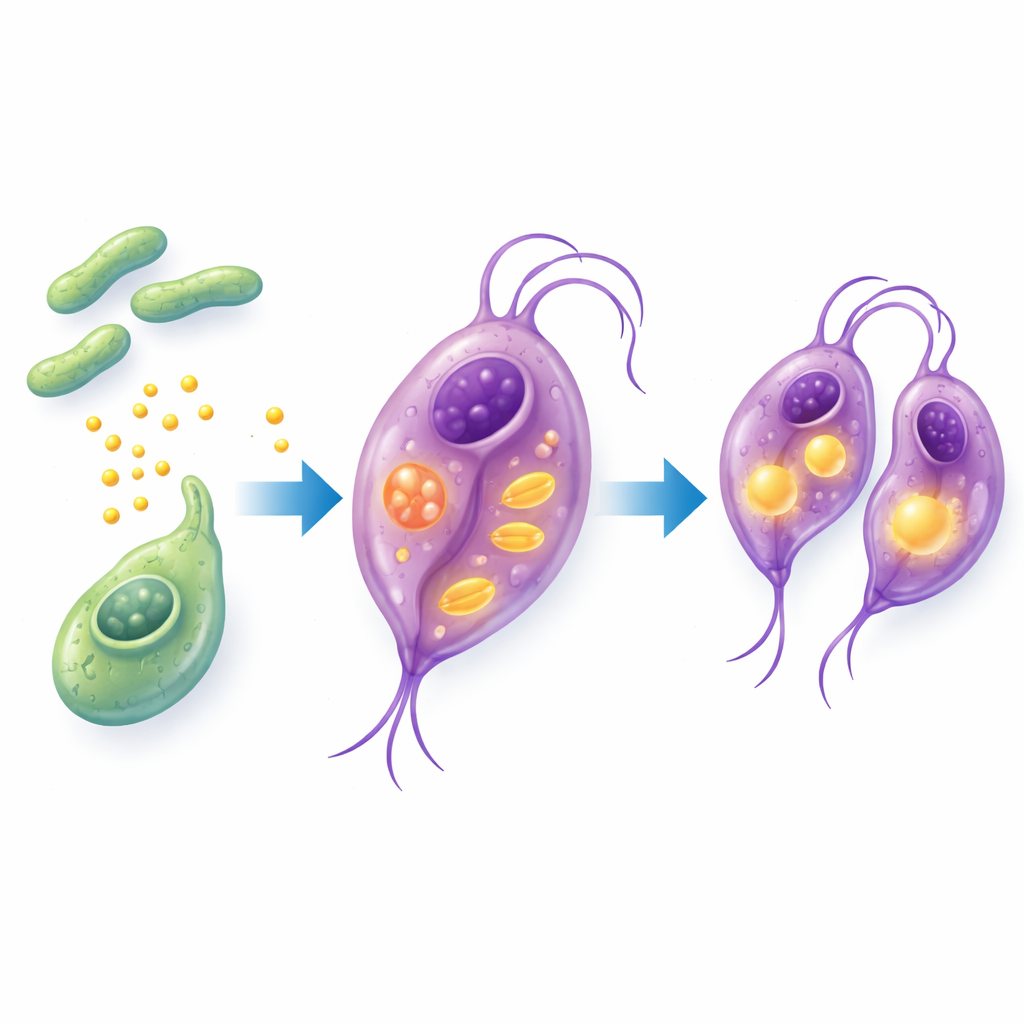
Que signifie cela pour la santé vaginale
Globalement, l’étude montre que B. breve, malgré sa réputation d’allié probiotique, n’agit pas comme un simple bouclier contre T. vaginalis. À court terme, ces bactéries amies semblent s’attacher au parasite, stimuler sa croissance et modifier son utilisation des lipides, sans protéger les cellules humaines des dommages. Sur des périodes plus longues, B. breve peut néanmoins contribuer au maintien de l’équilibre microbien général, mais il ne s’oppose pas directement à ce pathogène particulier. Pour les patientes et les cliniciens, ce travail souligne que toutes les bactéries « bonnes » ne sont pas protectrices en toutes circonstances et que la composition et le timing des microbes vaginaux peuvent indiquer quand les conditions favorisent une prolifération parasitaire, offrant potentiellement de nouveaux marqueurs d’alerte précoce ou des cibles pour des thérapies basées sur le microbiome.
Citation: Chen, PY., Yeh, YM., Chen, CH. et al. Bifidobacterium breve promotes growth and lipid alteration in Trichomonas vaginalis transiently through transcriptomic reprogramming. Sci Rep 16, 8997 (2026). https://doi.org/10.1038/s41598-026-38866-0
Mots-clés: microbiote vaginal, Trichomonas vaginalis, Bifidobacterium breve, métabolisme des acides gras, interaction probiotique–parasite