Clear Sky Science · fr
Les dynamiques conformationnelles et les analyses d’énergie libre de liaison révèlent un inhibiteur flavonoïde stable de la polymérase NS5 du virus de la dengue
Pourquoi un virus transmis par les moustiques a besoin d’un coup de pouce d’origine végétale
La dengue a explosé dans le monde ces dernières années, rendant des millions de personnes malades et causant des milliers de morts. Pourtant, nous ne disposons toujours pas d’un comprimé antiviral largement efficace et abordable pour traiter les personnes infectées. Cette étude pose une question apparemment simple mais aux implications importantes : des composés naturels d’origine végétale peuvent-ils être transformés en « clés » moléculaires précises qui grippent l’une des machines les plus importantes du virus de la dengue ?
Le moteur viral que les scientifiques cherchent à arrêter
Le virus de la dengue survit en copiant son matériel génétique à l’intérieur de nos cellules. Pour cela, il dépend d’une protéine clé appelée NS5, qui agit comme un petit moteur copiant l’ARN du virus. Si NS5 cesse de fonctionner, le virus ne peut pas fabriquer de nouveaux génomes et l’infection s’arrête. Les développeurs de médicaments voient donc NS5—en particulier sa région qui copie l’ARN, connue sous le nom d’ARN dépendante ARN polymérase—comme une cible de choix pour de nouveaux traitements. Plusieurs composés synthétiques et extraits végétaux ont déjà montré qu’il est possible de bloquer NS5, mais nombre de ces premiers candidats lient faiblement, sont instables ou soulèvent des inquiétudes quant à la sécurité et à leur pharmacocinétique.
Chercher dans les plantes des aiguilles chimiques prometteuses dans une botte de foin
Les chercheurs se sont concentrés sur les flavonoïdes, une vaste famille de composés végétaux présents dans des aliments comme les baies, le thé et les herbes, connus de longue date pour leurs effets antiviraux et anti-inflammatoires. À partir d’une base de données sélectionnée de composés secondaires végétaux, ils ont extrait 326 flavonoïdes et préparé des modèles tridimensionnels à la fois de l’enzyme NS5 du virus et de chaque molécule candidate. À l’aide d’un docking informatique progressif, ils ont demandé : quelles formes s’ajustent le mieux dans une région « par la porte arrière » spécifique de NS5 appelée le N-pocket—un site allostérique qui peut éteindre l’enzyme lorsqu’il est occupé, et qui tend à muter moins que le site actif principal ?
À chaque étape de ce criblage virtuel, les composés mal ajustés ou peu susceptibles de se comporter comme de vrais médicaments dans l’organisme ont été écartés. Les molécules restantes ont ensuite été évaluées non seulement sur l’ajustement géométrique, mais aussi sur la force de liaison estimée au moyen d’une méthode qui approche les énergies en jeu lorsqu’un composé se fixe à NS5 dans des conditions aqueuses similaires à la cellule. Ce processus a réduit le champ à quelques flavonoïdes en tête, dont un candidat, étiqueté PSCdb01560, s’est distingué par une énergie de liaison prédite particulièrement élevée.
Observer les molécules bouger dans un microscope virtuel
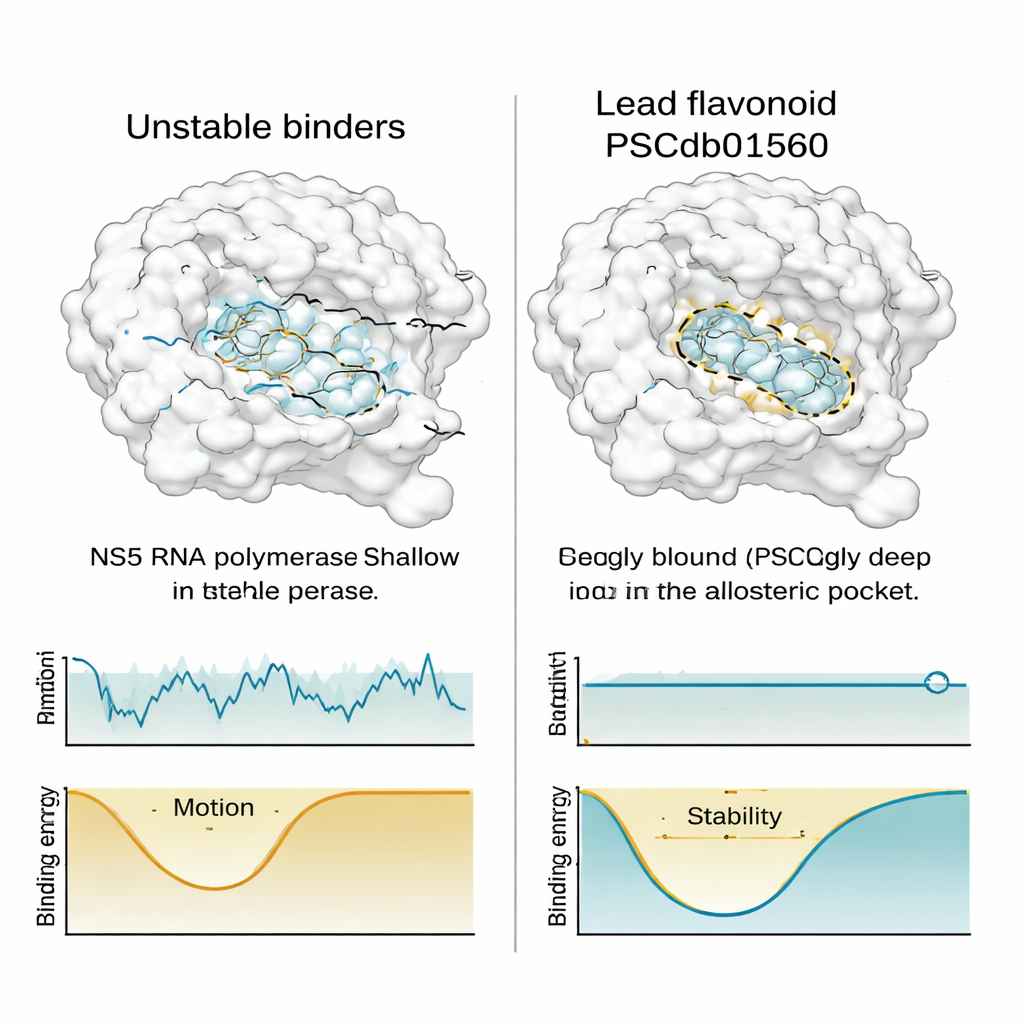
Un bon ajustement dans un cliché statique ne suffit pas ; un médicament utile doit aussi rester en place quand tout vibre en conditions réelles. Pour tester cela, l’équipe a réalisé de longues simulations de dynamique moléculaire détaillées—des films informatiques durant l’équivalent d’une demi-microseconde—pour NS5 associé aux meilleurs flavonoïdes et à un inhibiteur de référence connu. Ils ont suivi l’amplitude des mouvements de la protéine et de chaque composé, la compacité du complexe, son exposition à l’eau environnante, et la fréquence de formation et de rupture des contacts chimiques clés. PSCdb01560 a montré un comportement remarquablement stable : il est resté profondément installé dans le N-pocket, a peu bougé par rapport aux molécules rivales, et a semblé stabiliser la forme globale de NS5 plutôt que de la perturber.
En revanche, deux autres flavonoïdes initialement prometteurs ont commencé à dériver dans la poche ou sont devenus plus exposés au solvant avec le temps—des signes d’une liaison plus faible et moins fiable. Lorsque les chercheurs ont cartographié le « paysage d’énergie libre » de chaque complexe—une manière de visualiser quelles conformations sont favorisées thermodynamiquement—ils ont constaté que PSCdb01560 occupait une vallée d’énergie profonde et bien définie, tandis que les composés moins stables sautaient entre plusieurs bassins plus superficiels. En comparant les clichés de plus basse énergie aux poses initiales issues du docking, la position de PSCdb01560 avait à peine changé, soulignant sa fidélité conformationnelle.
Des chiffres qui suggèrent une puissance comparable à un médicament
Enfin, l’équipe a utilisé un cadre de calcul d’énergie pour estimer la force de liaison de chaque flavonoïde après avoir pris en compte tous les mouvements simulés. PSCdb01560 a obtenu une énergie libre de liaison plus favorable que le composé de référence établi, portée par une combinaison de complémentarité de forme serrée, d’interactions électriques attractives et de contacts hydrophobes à l’intérieur de la poche. Ce schéma—affinité calculée forte, positionnement stable dans le temps, flexibilité interne limitée et engagement de résidus NS5 cruciaux conservés entre les souches de dengue—fait de PSCdb01560 un point de départ particulièrement convaincant pour la conception de médicaments.
Ce que cela pourrait signifier pour les futurs traitements de la dengue
Ces résultats ne livrent pas encore de comprimé contre la dengue, mais ils réduisent considérablement la recherche. Le travail identifie une base flavonoïde d’origine végétale qui, in silico, surpasse plusieurs concurrents et même un inhibiteur de référence connu en termes de stabilité et d’énergie de liaison prédite. Les prochaines étapes sont expérimentales : tester si PSCdb01560 bloque réellement NS5 en éprouvette, empêche la dengue de se répliquer dans des cellules infectées et s’avère sûr dans des modèles animaux. Si ces obstacles sont franchis, des chimistes pourraient affiner ce flavonoïde en un antiviral cliniquement utile. Pour l’heure, l’étude livre un message porteur d’espoir : la bibliothèque chimique de la nature recèle encore des outils prometteurs pour désarmer l’une des menaces transmises par les moustiques qui croît le plus rapidement dans le monde.
Citation: Alsaady, I.M., Gattan, H.S., Aljahdali, S.M. et al. Conformational dynamics and binding free energy analyses unveil a stable flavonoid inhibitor of dengue virus NS5 polymerase. Sci Rep 16, 7761 (2026). https://doi.org/10.1038/s41598-026-38864-2
Mots-clés: virus de la dengue, polymérase NS5, inhibiteur flavonoïde, découverte de médicaments antiviraux, dock moléculaire