Clear Sky Science · fr
Détermination du débit cardiaque, de la fraction de shunt et du volume circulant actif chez les enfants atteints de syndrome du ventricule gauche hypoplasique après la procédure de Norwood avec shunt VD‑vers‑AP.
Maintenir l'équilibre d'un cœur néonatal fragile
Chez les nouveau‑nés porteurs d’un syndrome du ventricule gauche hypoplasique, la principale chambre de pompage destinée à envoyer le sang vers le corps est gravement sous‑développée. Les chirurgiens peuvent réacheminer la circulation lors d’une première intervention appelée procédure de Norwood, mais les jours qui suivent l’opération sont une équilibration délicate : les médecins doivent partager un seul ventricule fonctionnel entre les poumons et le reste du corps. Cette étude examine comment différentes concentrations d’oxygène dans le gaz respiratoire influent sur cet équilibre fragile et ce qui détermine réellement la répartition du flux sanguin.
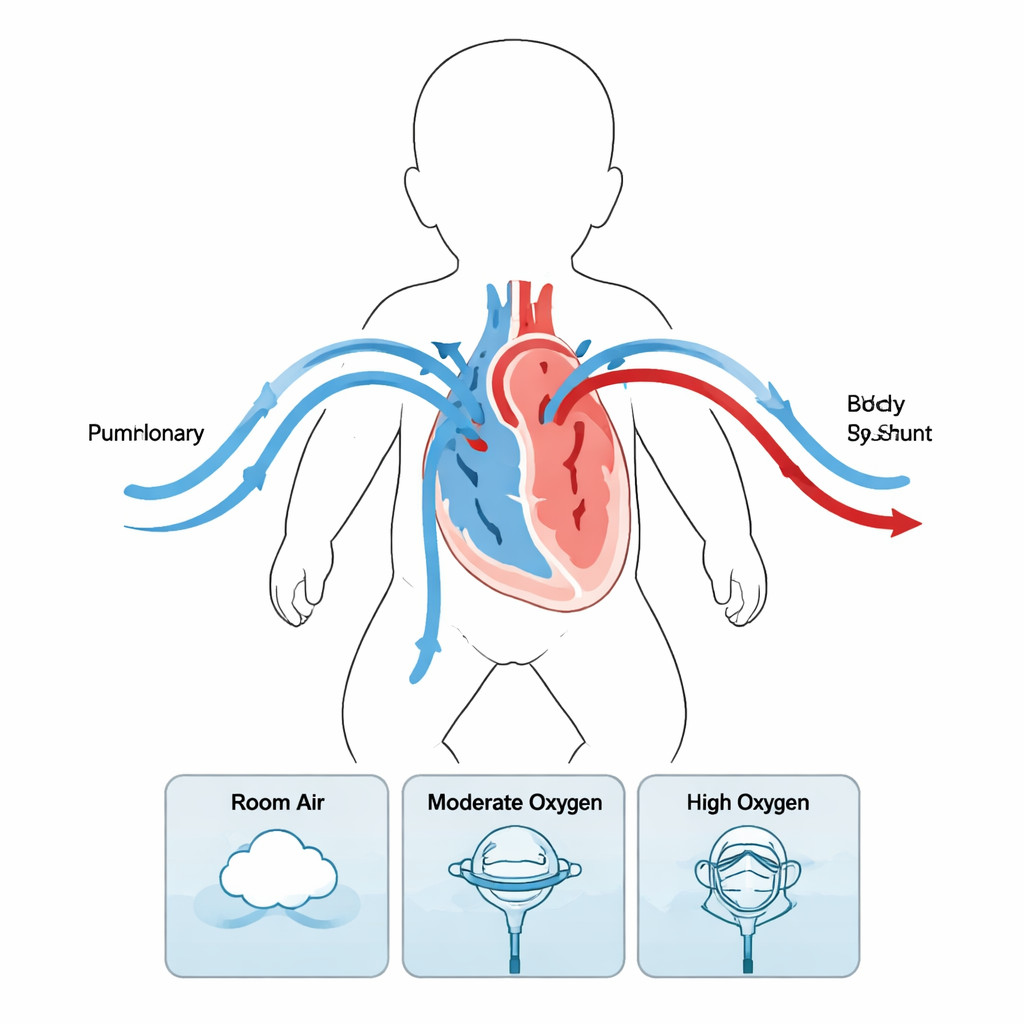
Une pompe unique faisant deux emplois
Dans un cœur normal, un ventricule envoie le sang vers les poumons et l’autre vers le corps. Chez ces nouveau‑nés, un seul ventricule doit accomplir les deux fonctions. Lors de la procédure de Norwood, les chirurgiens créent une nouvelle voie du cœur vers le corps et relient le ventricule droit aux artères pulmonaires via un petit tube, ou shunt. Le sang quittant le cœur se sépare donc : une partie passe par le shunt vers les poumons (flux pulmonaire, Qp) et une partie irrigue le corps (flux systémique, Qs). Obtenir le bon équilibre Qp/Qs est critique. Trop vers les poumons prive le corps de sang riche en oxygène ; trop peu menace la captation d’oxygène dans les poumons.
Une nouvelle façon de mesurer de petits cœurs
Les signes cliniques de chevet classiques, comme la tension artérielle et les saturations, donnent seulement une image approximative de la circulation chez ces nourrissons fragiles. Mesurer directement la consommation d’oxygène et le flux sanguin, nécessaire aux calculs classiques, est particulièrement difficile et sujet à erreur chez de petits bébés gravement malades. Les chercheurs ont utilisé à la place une technique de dilution ultrasonore. Ils ont injecté brièvement du sérum physiologique tiède dans une voie veineuse et mesuré de très faibles changements dans la propagation du son à travers le sang passant par une boucle extracorporelle. À partir de la forme des courbes obtenues, un logiciel spécialisé a pu estimer le débit cardiaque total, la part du sang allant aux poumons versus le corps, et le volume de sang effectivement en circulation dans les vaisseaux à un instant donné.
Augmenter l’oxygène : ce qui change vraiment
Seize nouveau‑nés ont été étudiés peu après leur opération de Norwood alors qu’ils étaient légèrement sédatés et sous ventilateur. L’équipe a mesuré les débits et les pressions à trois niveaux d’oxygène dans le gaz inspiré : environ l’air ambiant, un apport d’oxygène modéré, et un apport très élevé. À mesure que l’oxygène augmentait, le flux pulmonaire restait essentiellement stable, mais le flux vers le corps diminuait. Parce que le flux pulmonaire demeurait constant tandis que le flux systémique baissait, le ratio calculé Qp/Qs augmentait. Pourtant, les pressions qui propulsent le sang à travers les poumons et la résistance globale du circuit pulmonaire n’ont pas varié de façon significative. En revanche, les vaisseaux sanguins périphériques se sont contractés, augmentant la résistance vasculaire systémique, et le volume sanguin effectif en circulation — déjà faible comparé aux enfants à deux ventricules fonctionnels — a encore diminué.
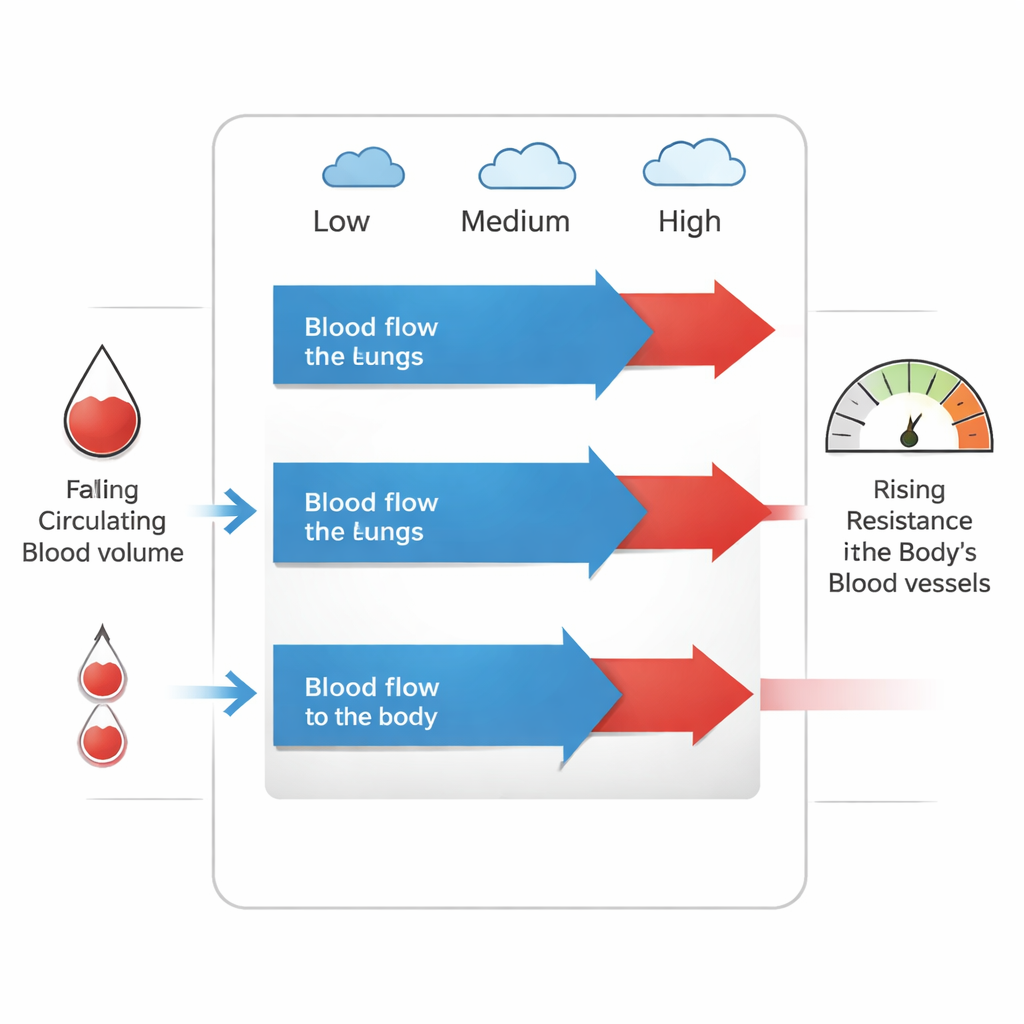
Pourquoi un tube fixe compte plus que l’oxygène
Ces observations suggèrent que, tôt après l’intervention, le shunt rigide reliant le ventricule aux artères pulmonaires agit comme la principale « valve » contrôlant le flux pulmonaire. Parce que le shunt se comporte comme un goulot mécanique fixe, un apport d’oxygène supplémentaire — normalement un puissant vasodilatateur pulmonaire — a peu de marge pour augmenter le flux vers les poumons. En revanche, une oxygénation plus élevée semble provoquer une vasoconstriction systémique, ralentir légèrement la fréquence cardiaque et aggraver la relative pénurie de volume sanguin en circulation. Le résultat est moins de sang atteignant les organes vitaux, même si les valeurs d’oxygène artérielles et veineuses augmentent parce que les échanges gazeux pulmonaires se sont améliorés. De petites variations du volume sanguin, par exemple lors d’une infection ou d’une inflammation, peuvent encore déplacer l’équilibre en faveur des poumons au détriment du corps.
Ce que cela signifie pour la prise en charge de ces nouveau‑nés
Pour les cliniciens, l’étude suggère que simplement augmenter l’oxygène ou utiliser des médicaments relaxant les vaisseaux pulmonaires n’est peut‑être pas la stratégie la plus efficace pour protéger ces bébés. Comme le débit pulmonaire est largement déterminé par la taille et la rigidité du shunt, le choix chirurgical soigneux du calibre du shunt et des stratégies postopératoires visant à augmenter le volume sanguin circulant et à réduire en douceur la résistance vasculaire systémique peuvent être plus importants pour maintenir une bonne perfusion des organes. En termes simples, les résultats plaident en faveur d’un soutien du côté systémique de la circulation — la quantité de sang qu’il reçoit et la résistance contre laquelle le cœur doit pomper — plutôt que d’essayer d’ajuster finement le flux pulmonaire par l’oxygène pendant les jours cruciaux qui suivent l’opération de Norwood.
Citation: Aronsson, A., Sigurdsson, T.S. & Lindberg, L. Determination of cardiac output, shunt-fraction, and active circulatory volume in children with hypoplastic left heart syndrome after the Norwood procedure with RV to PA-shunt.. Sci Rep 16, 4748 (2026). https://doi.org/10.1038/s41598-026-38858-0
Mots-clés: syndrome du ventricule gauche hypoplasique, procédure de Norwood, ventricule unique, hémodynamique néonatale, oxygénothérapie