Clear Sky Science · fr
LINC01857 favorise la progression du carcinome rénal à cellules claires en servant d’échafaudage à DNMT1 pour réprimer l’expression de WIF1
Pourquoi cette histoire sur le cancer du rein importe
Le carcinome rénal à cellules claires est la forme la plus courante et la plus mortelle de cancer du rein chez l’adulte. De nombreux patients ne sont diagnostiqués qu’après que la maladie s’est déjà propagée, et les traitements disponibles ne fonctionnent pas pour tout le monde. Cette étude met au jour un « interrupteur » moléculaire caché — un long ARN non codant nommé LINC01857 — qui aide les tumeurs rénales à croître et à se disséminer. Comprendre ce mécanisme pourrait ouvrir de nouvelles voies pour un diagnostic plus précoce et des traitements plus ciblés.
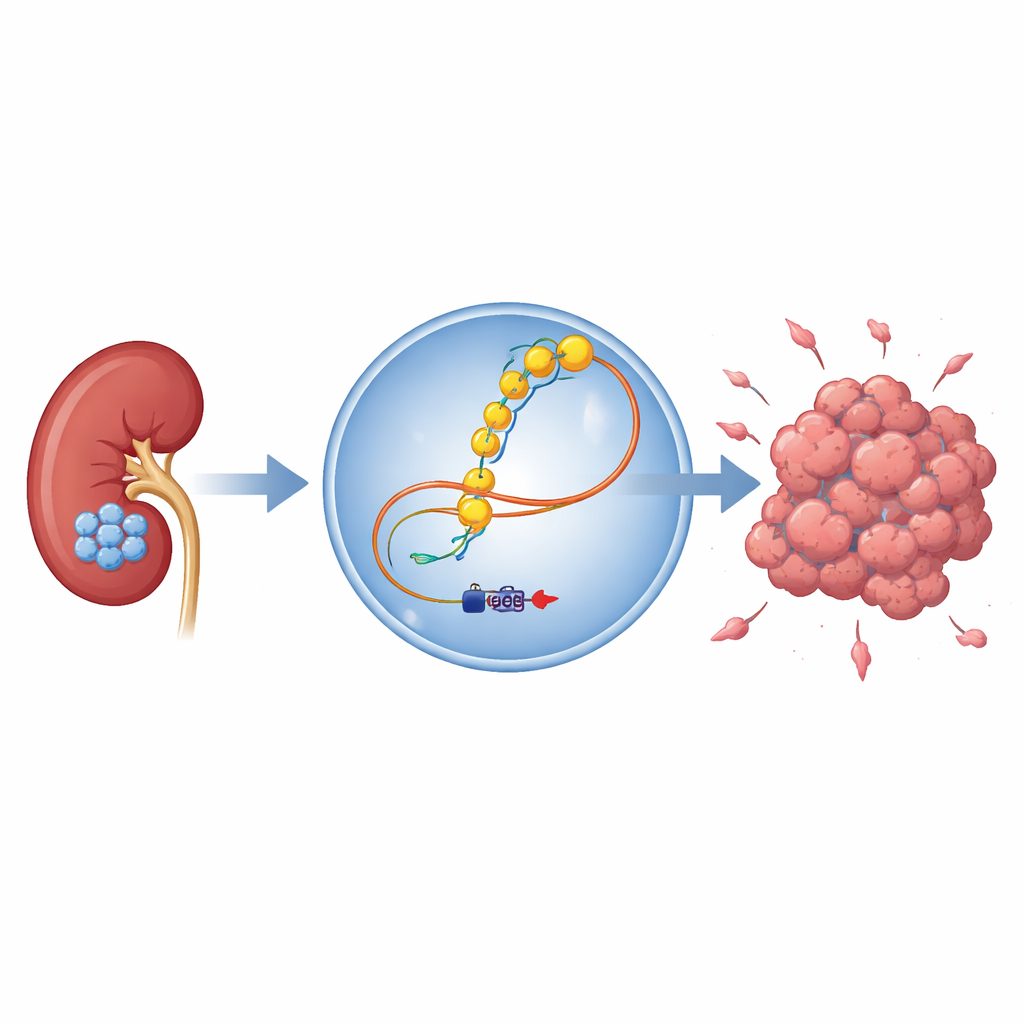
Un problème de cancer rénal en augmentation
Le carcinome rénal à cellules claires prend naissance dans les minuscules unités filtrantes du rein et est responsable de la majorité des décès par cancer rénal. Bien que l’imagerie ait amélioré la détection, jusqu’à un tiers des patients présentent une récidive après chirurgie, souvent parce que des foyers tumoraux microscopiques se sont déjà échappés. Les chercheurs savent que les cellules cancéreuses reprogramment leurs systèmes de contrôle internes en activant ou en désactivant certains gènes, mais la liste complète des acteurs et leurs interactions dans le cancer du rein reste incomplète. Les auteurs ont donc cherché à savoir si une classe de matériel génétique négligée — les longs ARN non codants — pouvait piloter ce processus.
L’essor d’un perturbateur silencieux
Contrairement aux gènes classiques qui portent les plans des protéines, les longs ARN non codants agissent davantage comme des câbles de commande, façonnant quels gènes sont utilisés et quand. L’équipe s’est concentrée sur l’un de ces ARN, LINC01857, déjà associé à plusieurs autres cancers. En analysant de larges bases de données publiques sur le cancer et des échantillons de 26 patients, ils ont constaté que les niveaux de LINC01857 étaient beaucoup plus élevés dans les tumeurs rénales à cellules claires que dans le tissu rénal normal adjacent. Dans des lignées cellulaires de cancer du rein cultivées en laboratoire, LINC01857 était également fortement augmenté et principalement localisé dans le noyau cellulaire — le centre de commande où s’organise l’activité des gènes — ce qui suggère qu’il pourrait influencer directement quels gènes sont silencieux ou activés.
Comment LINC01857 aide les tumeurs à croître et à se propager
Pour déterminer la fonction de LINC01857, les chercheurs ont modifié ses niveaux à la hausse et à la baisse dans des cellules de cancer du rein. Lorsqu’ils ont réduit LINC01857, les cellules se divisaient plus lentement et avaient moins de capacité à migrer et à envahir des barrières artificielles — des comportements associés à des tumeurs moins agressives. Augmenter LINC01857 produisait l’effet inverse, accélérant la croissance et l’invasion. Chez la souris, des cellules cancéreuses modifiées pour produire moins de LINC01857 formaient des tumeurs plus petites et donnaient moins de métastases pulmonaires après injection dans la circulation sanguine. Ensemble, ces expériences montrent que LINC01857 n’est pas un simple spectateur : il alimente activement la croissance et la dissémination tumorales.
Une pince moléculaire sur un frein protecteur
En creusant plus loin, les scientifiques ont découvert comment LINC01857 exerce son influence. Dans le noyau, LINC01857 se lie à DNMT1, une enzyme qui ajoute des marques chimiques à l’ADN et peut éteindre des gènes. Agissant comme un échafaudage, LINC01857 guide DNMT1 vers le régulateur d’un gène protecteur appelé WIF1, qui contribue normalement à contenir une voie de croissance puissante connue sous le nom de Wnt/β‑caténine. Une fois en place, DNMT1 « décore » fortement la région de contrôle de WIF1 avec des groupes méthyle, étouffant ainsi son expression. L’équipe a confirmé que chez les cellules de cancer du rein, cette région est plus fortement marquée lorsque LINC01857 est élevé, et que bloquer DNMT1 ou diminuer LINC01857 restaure l’activité de WIF1. Lorsque WIF1 est silencieux, la voie Wnt/β‑caténine s’active davantage, augmentant les niveaux de protéines qui stimulent la division cellulaire et la migration, rendant les tumeurs plus agressives.
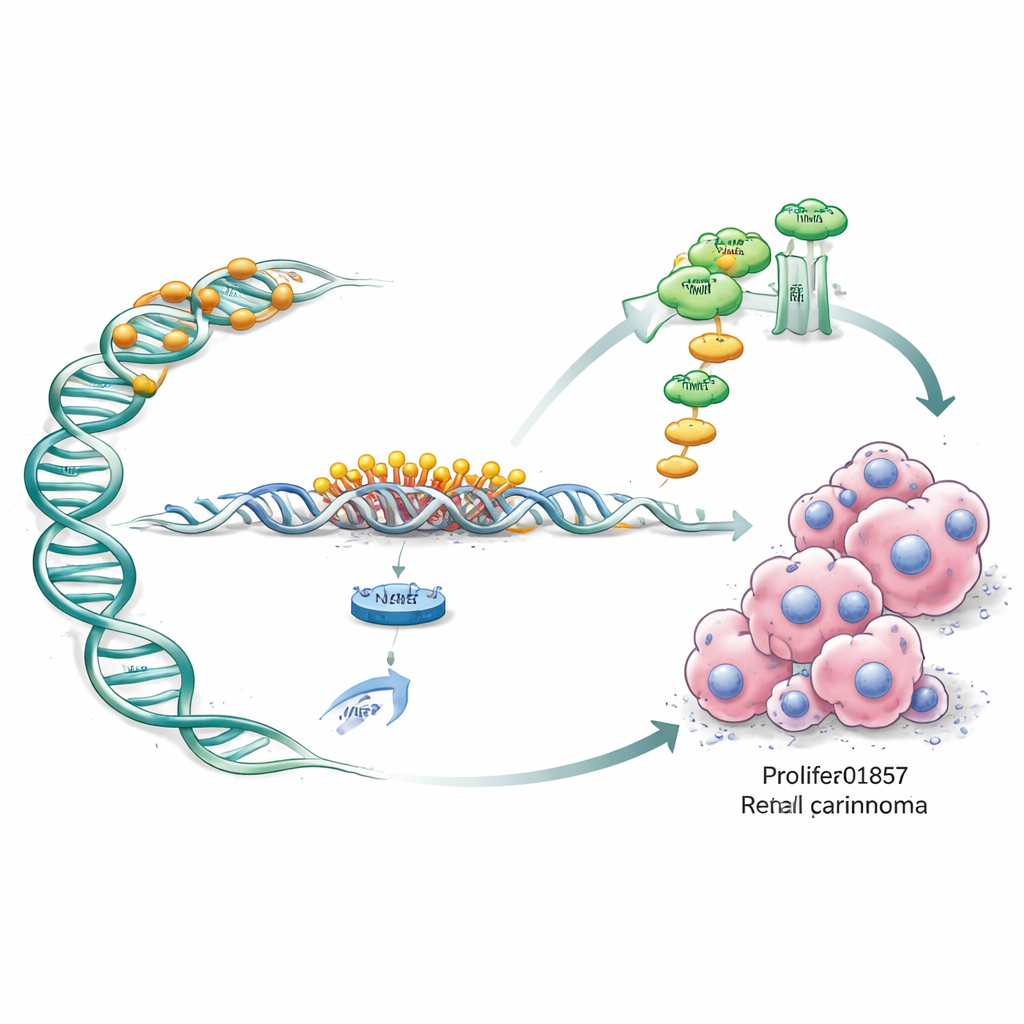
Transformer une découverte en piste thérapeutique
En cartographiant cette chaîne — de LINC01857 à DNMT1 puis à WIF1 et à la voie Wnt/β‑caténine — l’étude révèle une voie claire par laquelle un ARN non codant peut basculer les cellules rénales vers le cancer. Cibler LINC01857, perturber son interaction avec DNMT1 ou réactiver WIF1 pourrait être exploré comme nouvelles stratégies pour ralentir ou arrêter le carcinome rénal à cellules claires. Bien que des travaux supplémentaires soient nécessaires, y compris des mesures plus fines des marquages de l’ADN et des études chez les patients, cette recherche identifie LINC01857 à la fois comme un possible marqueur de sévérité de la maladie et comme une cible prometteuse pour de futures thérapies visant à empêcher la diffusion des tumeurs rénales.
Citation: Xiang, W., Lyu, L., Zheng, F. et al. LINC01857 promotes clear cell renal cell carcinoma progression by scaffolding DNMT1 to suppress WIF1 expression. Sci Rep 16, 8069 (2026). https://doi.org/10.1038/s41598-026-38828-6
Mots-clés: carcinome rénal à cellules claires, LINC01857, méthylation de l’ADN, WIF1, signalisation Wnt bêta-caténine