Clear Sky Science · fr
Le cadmium induit la ferroptose dans les spermatocytes de souris en activant la voie ROS–TCA
Pourquoi un métal courant importe pour la santé des hommes
Le cadmium est un métal mou utilisé dans les batteries, les pigments et d’autres produits industriels. Il peut s’accumuler dans les sols, l’eau et les aliments, pénétrant discrètement dans nos organismes au fil du temps. De nombreuses études ont lié l’exposition au cadmium à une baisse du nombre de spermatozoïdes et à une détérioration de leur qualité chez l’homme, mais le mécanisme précis par lequel il endommage les cellules productrices de spermatozoïdes est resté flou. Cette étude s’attache à ce problème, révélant comment le cadmium pousse les spermatocytes de souris vers une voie spécifique de mort cellulaire liée au fer et à un système énergétique mitochondrial stressé, les « centrales » de la cellule.
De la pollution aux cellules spermatiques vulnérables
Le cadmium est un perturbateur environnemental bien connu du système reproducteur masculin. Les hommes exposés au travail ou vivant dans des zones polluées présentent souvent une réduction du nombre de spermatozoïdes, de leur mobilité et de leur morphologie normale, et parfois des dommages de l’ADN spermatiques. Les études animales confirment ces observations, montrant des testicules atrophiés, des barrières protectrices perméables, un faible taux de testostérone et une perte étendue de cellules germinales. Les auteurs ont précédemment observé que le cadmium pouvait déclencher une forme inhabituelle de mort cellulaire dépendante du fer appelée ferroptose dans le tissu testiculaire. Dans ce travail, ils se sont concentrés sur les spermatocytes de souris — des cellules en cours de transformation en spermatozoïdes — pour comprendre précisément comment le cadmium les endommage et si cette voie de mort liée au fer est impliquée.
Surcharge en fer et une forme particulière de mort cellulaire
Pour enquêter, l’équipe a cultivé une lignée de spermatocytes de souris en bocaux et exposé les cellules au cadmium, avec ou sans des médicaments connus pour bloquer la ferroptose. Le cadmium a réduit la survie cellulaire d’environ moitié et ralenti la division cellulaire. À l’intérieur des cellules, les niveaux de fer libre et d’un marqueur de l’altération lipidique appelé malondialdéhyde ont fortement augmenté, tandis qu’une enzyme protectrice clé, GPX4, a diminué. D’autres protéines impliquées dans le stockage et l’export du fer ont augmenté, indiquant une perturbation grave de la gestion du fer. Lorsque les chercheurs ont ajouté des inhibiteurs de la ferroptose — un chélateur du fer et une molécule protégeant les lipides — bon nombre de ces changements nuisibles se sont atténués et la survie cellulaire s’est améliorée. Ensemble, ces modifications correspondent au signature de la ferroptose, indiquant que le cadmium ne se contente pas de tuer les cellules de manière vague, mais les pousse dans ce programme de mort spécifique dépendant du fer et des lipides.
Des mitochondries assiégées
L’histoire s’est approfondie lorsque les scientifiques ont tourné leur attention vers les mitochondries, centres énergétiques qui génèrent aussi des espèces réactives de l’oxygène (ROS) comme sous-produit. Au microscope, les cellules saines présentaient des mitochondries longues et filamenteuses, alors que les cellules exposées au cadmium montraient des mitochondries courtes et fragmentées, signe d’une atteinte structurelle. Les mesures ont confirmé que les ROS mitochondriaux ont fortement augmenté, tandis que la charge électrique à travers la membrane mitochondriale — un indicateur clé de la fonction — a diminué. Les cellules ont réagi en renforçant leurs systèmes de défense internes, y compris des protéines régulées par le senseur de stress Nrf2, mais ces défenses n’étaient pas suffisantes. Fait important, les médicaments bloquant la ferroptose ont réduit les ROS mitochondriaux et partiellement restauré la santé mitochondriale, reliant directement ces « centrales » endommagées à la voie de mort dépendante du fer.
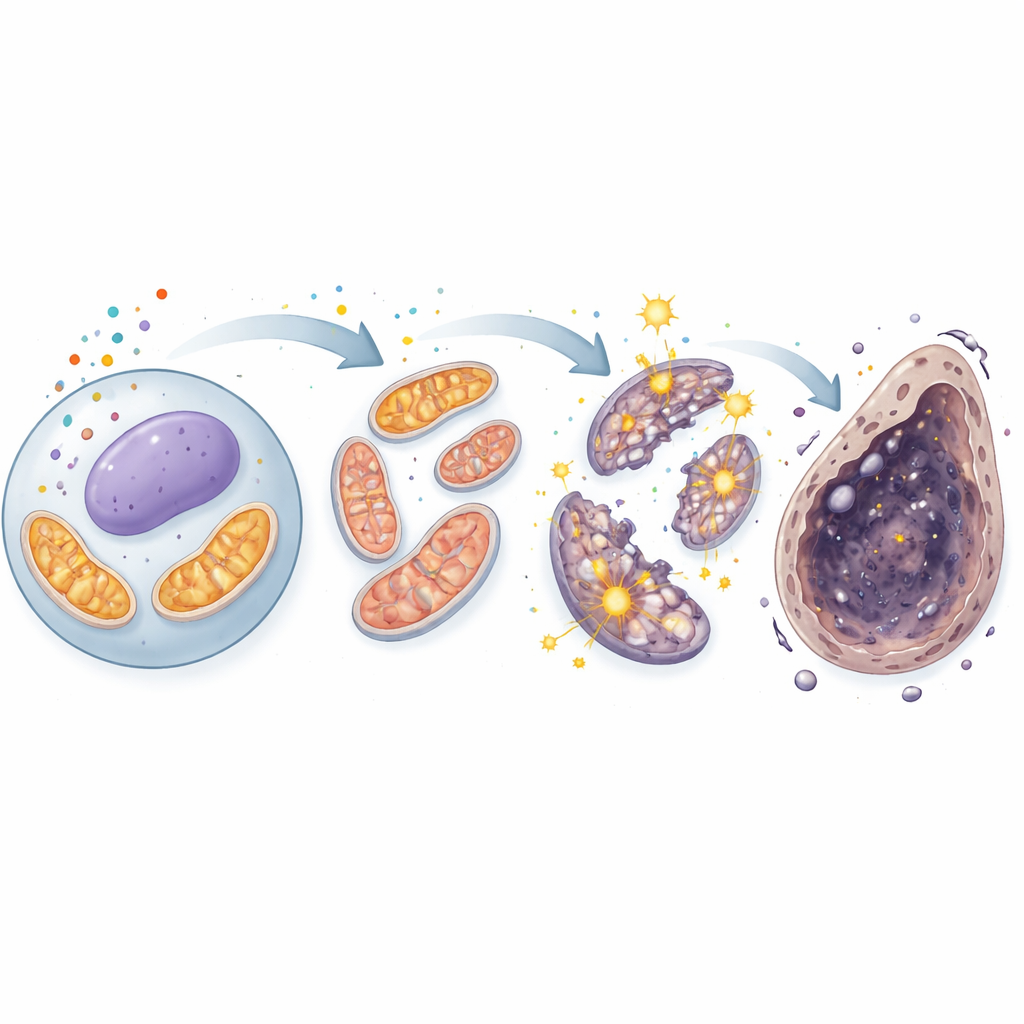
Un cercle vicieux dans la centrale énergétique de la cellule
Grâce à une combinaison de profils d’activité génique et de mesures métabolitiques, les chercheurs ont constaté que le cadmium faisait plus que simplement endommager les mitochondries — il semblait pirater leur circuit énergétique central, le cycle des acides tricarboxyliques (TCA). Les niveaux de deux intermédiaires centraux du TCA, l’alpha-cétoglutarate et le succinate, ont augmenté de manière significative, et l’activité de la pyruvate carboxylase, une enzyme qui alimente le cycle en carburant frais, était renforcée. Cela suggère que le cycle TCA devenait paradoxalement hyperactif dans les cellules endommagées, forçant un flux accru d’électrons dans la chaîne respiratoire et provoquant davantage de fuites de ROS. Ces ROS supplémentaires ont ensuite interagi avec la chimie du fer et endommagé les membranes, renforçant la ferroptose. Là encore, les inhibiteurs de la ferroptose ont atténué ces distorsions métaboliques, soulignant le lien étroit entre cadmium, suractivation mitochondriale et mort cellulaire dépendante du fer.
Ce que cela signifie pour la fertilité et la recherche future
En termes simples, l’étude montre que le cadmium attaque les cellules formant les spermatozoïdes en endommageant directement leurs mitochondries et en déréglant leur cycle énergétique, qui bascule en surrégime nocif. Cette combinaison inonde les cellules de molécules réactives de l’oxygène et perturbe l’équilibre du fer, les poussant vers la ferroptose. Comme les spermatocytes sont essentiels à la production d’un sperme sain, leur perte peut contribuer à expliquer pourquoi l’exposition au cadmium est si fortement associée à une baisse de la fertilité masculine. Bien que ces expériences aient été réalisées sur des cellules de souris en culture, elles fournissent une carte mécanistique claire que des études futures chez l’animal et chez l’humain pourront tester. Ce travail met aussi en lumière des stratégies protectrices potentielles : des médicaments ou des nutriments qui calment le stress mitochondrial, ajustent finement le cycle TCA ou empêchent les dommages membranaires liés au fer pourraient aider à protéger le système reproducteur masculin contre des métaux environnementaux comme le cadmium.
Citation: Xiong, L., Yi, L., Zeng, X. et al. Cadmium induces ferroptosis in mouse spermatocytes by activating the ROS–TCA pathway. Sci Rep 16, 8449 (2026). https://doi.org/10.1038/s41598-026-38827-7
Mots-clés: toxicité du cadmium, fertilité masculine, stress mitochondrial, ferroptose, espèces réactives de l’oxygène