Clear Sky Science · fr
Déterminants au niveau des résidus de la stabilité thermique de l’endolysine extrémophile Ts2631
Pourquoi les virus thermophiles comptent pour les antibiotiques de demain
À mesure que la résistance aux antibiotiques augmente, les chercheurs cherchent de nouvelles façons d’éliminer les bactéries dangereuses. Une piste prometteuse emprunte des armes à des virus qui infectent les bactéries, appelés bactériophages. Ces virus produisent des enzymes, nommées endolysines, qui perforent la paroi cellulaire bactérienne. L’étude présentée ici porte sur une endolysine remarquablement résistante à la chaleur, Ts2631, issue d’un virus vivant dans des sources chaudes islandaises. En identifiant quels blocs constitutifs individuels de cette protéine lui confèrent une telle stabilité à des températures proches de l’ébullition, les chercheurs espèrent concevoir des enzymes antibactériennes plus robustes et durables pour la médecine et la biotechnologie. 
Un outil viral forgé dans des sources bouillantes
Ts2631 provient d’un bactériophage qui infecte la bactérie thermophile Thermus scotoductus, qui prospère dans des eaux dépassant largement 60 °C. L’enzyme Ts2631 clive une liaison spécifique du peptidoglycane, le réseau robuste qui entoure les cellules bactériennes. Ce qui distingue Ts2631, c’est son extrême thermostabilité : elle reste repliée jusqu’à environ 100–105 °C, selon le milieu. C’est bien au‑delà des températures auxquelles la plupart des protéines se déploient. Les auteurs ont comparé Ts2631 à son homologue le mieux étudié issu d’un virus à température modérée, la lysozyme T7, pour déterminer quels tours structurels la nature a employés pour maintenir Ts2631 intacte dans de telles conditions hostiles.
Boucles plus courtes et composition différente des éléments constitutifs
Les protéines sont des chaînes constituées de 20 types d’acides aminés, repliées en formes complexes. Lorsque les chercheurs ont superposé les structures 3D de Ts2631 et de la lysozyme T7, ils ont constaté que l’architecture générale est très similaire : les deux présentent un cœur compact de hélices et de feuillets. La différence clé réside dans les régions de boucles flexibles qui relient ces éléments. Dans Ts2631, ces boucles sont plus courtes et présentent une flexibilité réduite, tandis que la lysozyme T7 a des boucles plus longues et plus lâches. Ts2631 contient également davantage de certains acides aminés souvent associés à la résistance à la chaleur : la proline rigide ; des résidus aromatiques tels que la tyrosine et le tryptophane ; et l’arginine chargée positivement. En même temps, elle possède moins de sérine, d’acide aspartique et d’acide glutamique, résidus qui peuvent fragiliser les protéines à haute température. Ce schéma se maintient non seulement par rapport à la lysozyme T7, mais aussi lorsque Ts2631 est comparée à des centaines de milliers de protéines virales et à des millions de protéines bactériennes.
Échanger des acides aminés isolés pour tester leur importance
Pour passer des corrélations à la causalité, l’équipe a remplacé systématiquement 55 acides aminés individuels dans Ts2631 et a mesuré comment chaque mutation affectait la température de fusion (Tm) et la capacité de l’enzyme à dégrader la paroi bactérienne. Certains changements autour du site actif contenant du zinc ont été particulièrement délétères. Lorsqu’ils ont modifié trois résidus coordonnant le zinc (H30, H131 et C139), la Tm de la protéine a chuté jusqu’à environ 20 °C et l’activité a été perdue. Deux tyrosines conservées (Y60 et Y69) ont aussi contribué à la stabilité. De manière surprenante, la suppression d’un pont disulfure — un type de liaison covalente entre les cystéines C80 et C90 — a en réalité augmenté la température de fusion, bien que cela ait détruit l’activité. Cela montre qu’être très stable en éprouvette ne signifie pas toujours qu’une protéine fonctionnera mieux dans des conditions réelles. 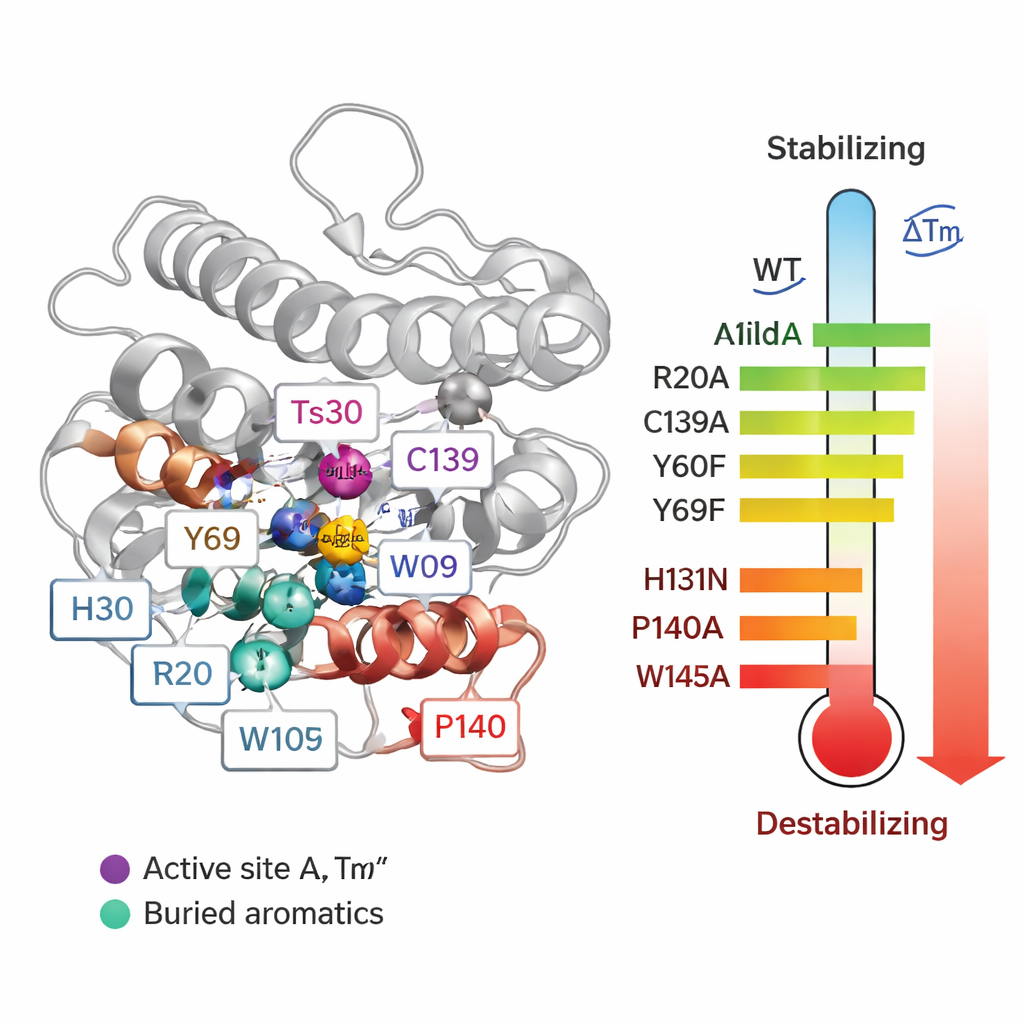
Ancrages aromatiques cachés et une prise clé sur la paroi bactérienne
Les résultats les plus frappants sont issus des mutations de résidus de proline et de tryptophane. Remplacer une seule proline (P140), située juste à côté de la cystéine de liaison au zinc C139, a réduit la Tm de plus de 21 °C et affaibli l’activité après chauffage, car la mutation a perturbé une géométrie de liaison particulière nécessaire à la coordination correcte du métal. Plusieurs tryptophanes profondément enfouis (W102, W109 et surtout W145) se sont aussi révélés critiques : leur remplacement par de l’alanine a provoqué des baisses de Tm de 14–24 °C et a rendu l’enzyme beaucoup plus sensible à la chaleur lors des tests d’activité. Ces résidus aromatiques agissent comme des ancrages internes qui verrouillent le cœur de la protéine. Parmi les arginines, la plupart ont eu peu d’effet sur la stabilité, mais R20 s’est avérée essentielle pour l’accrochage au peptidoglycane. Lorsque R20 a été remplacée, l’enzyme liait mal la paroi bactérienne et perdait son activité après chauffage, révélant que certains résidus contribuent davantage à la fonction qu’à la seule robustesse thermique.
Des enzymes de sources chaudes vers des antibactériens plus résistants
Dans l’ensemble, l’étude montre que l’extraordinaire résistance thermique de Ts2631 repose sur une poignée d’acides aminés bien positionnés plutôt que sur un renforcement uniforme de l’ensemble de la protéine. Les résidus liant le zinc, une proline conservée proche du site actif, et des chaînes latérales aromatiques enfouies forment un noyau stabilisant, tandis que certaines caractéristiques classiques de stabilisation, comme les ponts disulfure ou les liaisons ioniques, comptent moins ici qu’on ne le présumerait. Pour le domaine en général, ce travail suggère que les endolysines mésophiles (à température modérée) pourraient être rendues plus durables en remplaçant soigneusement certaines positions par du tryptophane ou de la proline sans sacrifier l’activité antibactérienne. Autrement dit, en apprenant comment la nature construit des enzymes capables de résister à des températures proches de l’ébullition, les scientifiques obtiennent une feuille de route pratique pour concevoir des antibiotiques protéiques plus fiables et de plus longue durée de vie.
Citation: Cieminska, K., Kaczorowska, AK., Kozlowski, L.P. et al. Residue-level determinants of the thermal stability of the extremophilic Ts2631 endolysin. Sci Rep 16, 7630 (2026). https://doi.org/10.1038/s41598-026-38786-z
Mots-clés: endolysine thermostable, enzymes de bactériophages, thermostabilité des protéines, résistance aux antibiotiques, ingénierie des protéines