Clear Sky Science · fr
Étude sur les biomarqueurs de la transformation des cellules musculaires lisses vasculaires en cellules spumeuses induite par l’homocystéine
Pourquoi les artères s’obstruent à partir de petits changements cellulaires
L’athérosclérose — l’obstruction et le durcissement progressifs des artères — est une cause majeure d’infarctus et d’accidents vasculaires cérébraux. On parle souvent de cholestérol et d’alimentation, mais moins de la façon dont des cellules individuelles de la paroi vasculaire évoluent au fil de la maladie. Cette étude examine de près un déclencheur particulier, une molécule sanguine appelée homocystéine, et montre comment elle peut pousser des cellules musculaires normalement bienveillantes des artères à accumuler des lipides et à se transformer en cellules dites spumeuses, les éléments constitutifs des plaques dangereuses.
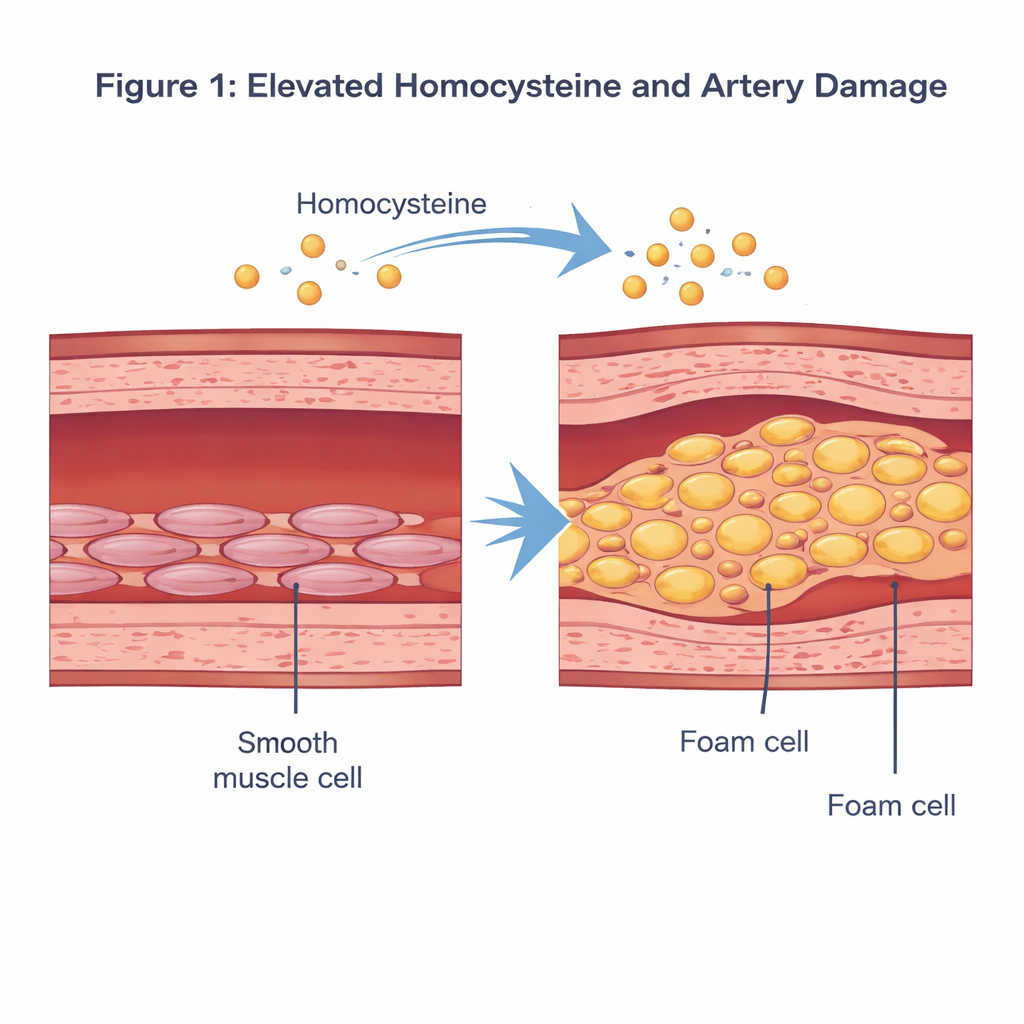
Un acide aminé perturbateur dans le sang
L’homocystéine est un acide aminé contenant du soufre produit lorsque notre organisme métabolise la méthionine, un nutriment alimentaire. En conditions normales, son taux sanguin est faible. Lorsqu’il dépasse environ 15 micromoles par litre — état appelé hyperhomocystéinémie — des études épidémiologiques l’ont associé à un risque cardiovasculaire accru. Des travaux antérieurs suggéraient qu’un excès d’homocystéine peut endommager la couche interne des artères, déclencher une inflammation et modifier le comportement des cellules musculaires lisses vasculaires, qui se situent dans la couche médiane de la paroi et contribuent à réguler la pression artérielle par contraction et relaxation.
Comment les cellules musculaires artérielles deviennent des cellules spumeuses chargées de lipides
Les chercheurs se sont concentrés sur la façon dont l’homocystéine reconfigure ces cellules musculaires lisses. En culture, ils ont exposé des cellules musculaires lisses vasculaires humaines à une dose d’homocystéine destinée à reproduire un état pathologique et les ont comparées à des cellules non traitées. À l’aide de colorations classiques et de tests biochimiques, ils ont observé que les cellules traitées par l’homocystéine se remplissaient de gouttelettes lipidiques colorées en rouge, et que leurs taux de cholestérol et de triglycérides augmentaient fortement. Parallèlement, les marqueurs protéiques de leur identité « contractile » habituelle diminuaient, tandis que les marqueurs d’un état plus synthétique et favorisant la formation de plaques augmentaient. Ensemble, ces changements montrent que l’homocystéine peut pousser les cellules musculaires lisses hors de leur rôle normal vers un phénotype de type cellule spumeuse, chargé en lipides, qui contribue directement à la formation des plaques.
À la recherche des empreintes moléculaires à l’intérieur des cellules
Pour comprendre quelles protéines changent au cours de cette transformation, l’équipe a eu recours à la protéomique moderne, une technologie capable de mesurer des milliers de protéines simultanément. Ils ont comparé les niveaux protéiques des cellules traitées par l’homocystéine aux témoins et ont quantifié de manière fiable près de 4 800 protéines. Parmi elles, 54 se sont révélées significativement modifiées : 13 augmentées et 41 diminuées. Bon nombre de ces protéines impliquées sont liées à la gestion des lipides, à la survie cellulaire, au stress oxydatif et au remodelage structural des cellules. Les auteurs ont ensuite utilisé des outils bioinformatiques pour regrouper ces protéines par voies fonctionnelles et cartographier leurs interactions, mettant en évidence des réseaux associés au métabolisme du cholestérol et aux réponses au stress dans la paroi vasculaire.
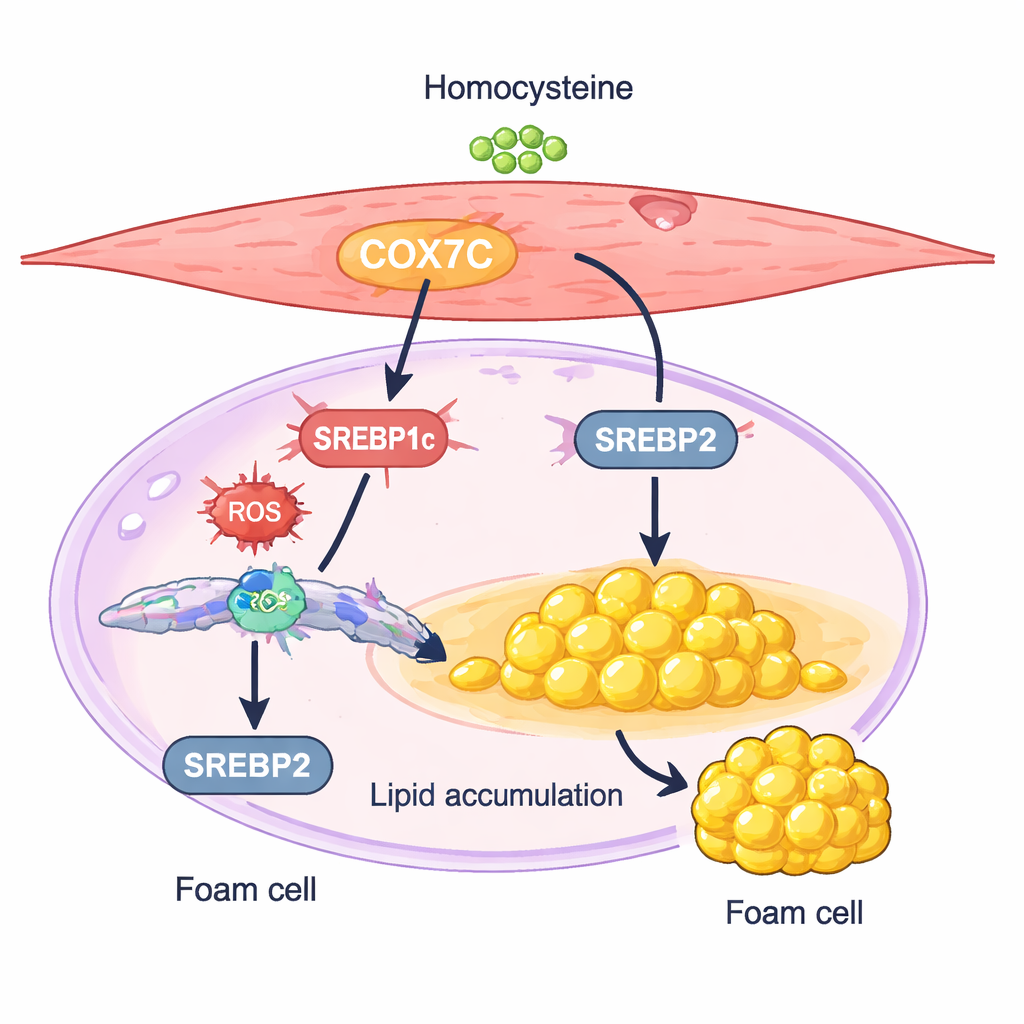
Un commutateur mitochondrial qui pousse les cellules à stocker des lipides
Une protéine, nommée COX7C, est apparue comme une suspecte particulièrement intéressante. COX7C fait partie des « centrales » énergétiques de la cellule, les mitochondries, où elle contribue à la gestion de la production d’énergie. Dans les cellules musculaires lisses traitées par l’homocystéine, les niveaux de COX7C étaient plus élevés que dans les témoins. Les chercheurs ont montré qu’une surexpression de COX7C accentuait encore l’accumulation lipidique et augmentait l’expression de deux régulateurs maîtres de la synthèse lipidique, SREBP1c et SREBP2. L’extinction de COX7C produisait l’effet inverse : elle atténuait l’activité des SREBP, réduisait l’accumulation de cholestérol et de triglycérides et limitait les changements de type cellule spumeuse. Ces résultats soutiennent un modèle selon lequel l’homocystéine augmente COX7C dans les mitochondries, renforce les signaux de stress cellulaires et active à son tour la synthèse lipidique pilotée par les SREBP, poussant ainsi les cellules musculaires lisses vers un état d’accumulation lipidique.
Ce que cela signifie pour la santé cardiaque et les thérapies futures
Ce travail ne démontre pas encore ce qui se passe dans les artères humaines, et il a été réalisé sur des cellules en culture plutôt que chez des patients. Il offre néanmoins un aperçu détaillé de la manière dont une homocystéine élevée peut contribuer à convertir des cellules musculaires artérielles utiles en cellules spumeuses nuisibles, et il identifie COX7C et des protéines associées comme biomarqueurs ou cibles médicamenteuses potentielles. Pour le grand public, le message clé est que, au-delà du « bon » et du « mauvais » cholestérol, de petits changements dans la chimie du sang — comme un excès d’homocystéine — peuvent reprogrammer la paroi vasculaire de l’intérieur. En identifiant des acteurs moléculaires tels que COX7C et la voie SREBP, cette étude jette les bases de stratégies futures visant à empêcher la formation de plaques en évitant que les cellules artérielles ne deviennent de véritables réservoirs lipidiques miniatures.
Citation: Wang, X., Ma, X., Zhang, X. et al. Study on biomarkers of homocysteine-induced transformation of vascular smooth muscle cells into foam cells. Sci Rep 16, 7411 (2026). https://doi.org/10.1038/s41598-026-38763-6
Mots-clés: athérosclérose, homocystéine, cellules spumeuses, cellules musculaires lisses vasculaires, COX7C