Clear Sky Science · fr
Activation transcriptionnelle de LINGO1 favorise la prolifération et l’échappement immunitaire dans le cancer colorectal
Pourquoi une protéine cérébrale compte dans le cancer du côlon
Le cancer colorectal est l’un des cancers les plus fréquents et mortels dans le monde, et de nombreux patients rechutent ou développent des maladies disséminées malgré la chirurgie, la chimiothérapie et les nouvelles thérapies immunitaires. Cette étude se concentre sur une molécule peu connue appelée LINGO1, étudiée à l’origine dans le cerveau, et montre qu’elle peut aider les tumeurs du côlon à croître et à se dissimuler aux défenses de l’organisme. Comprendre ce nouvel acteur pourrait améliorer la prédiction des pronostics et, à terme, ouvrir la voie à des traitements plus ciblés.
Un interrupteur caché activé dans les cellules tumorales
Les chercheurs ont d’abord cherché à savoir si les niveaux de LINGO1 diffèrent entre le tissu intestinal sain et le tissu cancéreux. En utilisant d’importantes bases de données publiques de gènes et plusieurs cohortes indépendantes de patients, ils ont constaté que LINGO1 est systématiquement beaucoup plus élevé dans les tumeurs colorectales que dans le tissu adjacent normal. Les patients dont les tumeurs présentaient davantage de LINGO1 avaient tendance à présenter une maladie plus avancée, une atteinte des ganglions lymphatiques, des métastases à distance et une survie plus courte. Même après prise en compte d’autres facteurs cliniques, LINGO1 restait un signe d’alerte indépendant, suggérant qu’il agit comme un « bouton de volume » qui, lorsqu’il est monté, signale un cancer plus agressif.
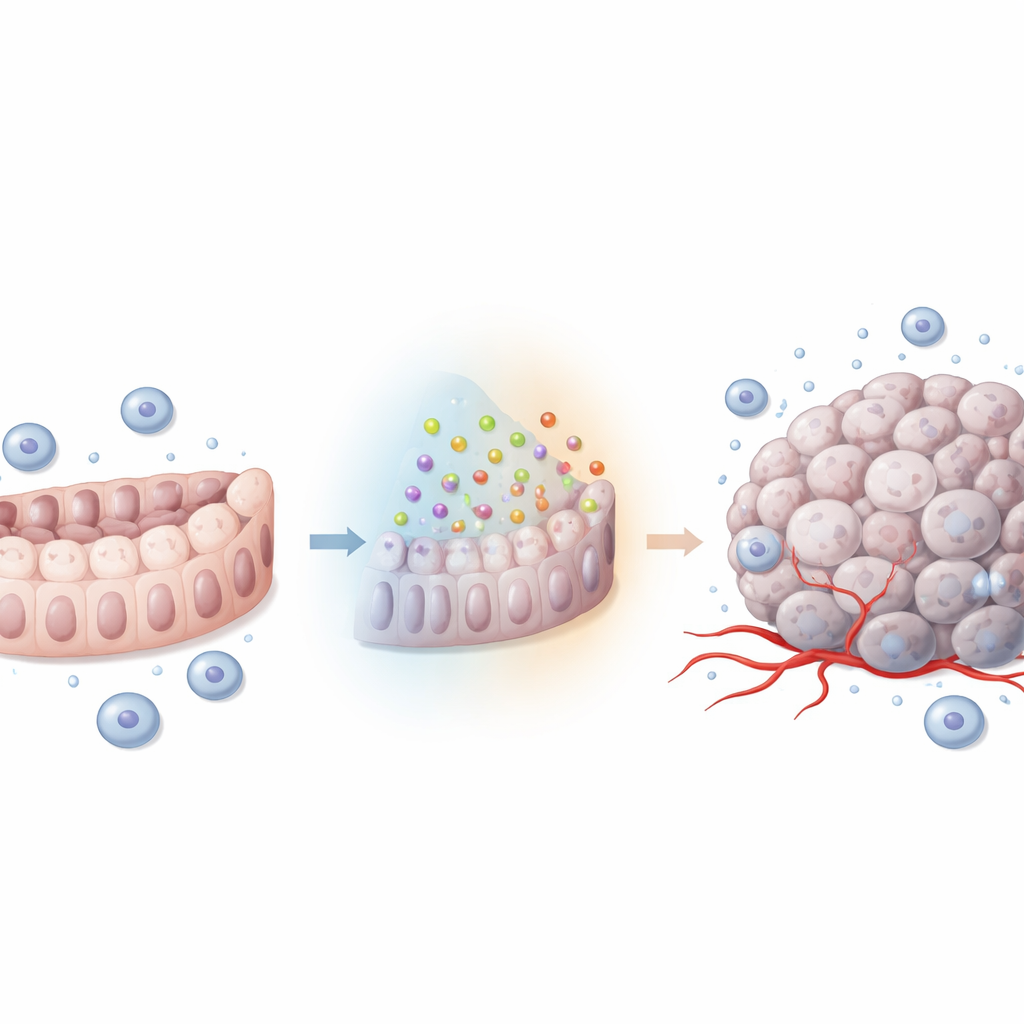
De l’activité génique à une croissance et une dissémination accrues
Pour aller au-delà des statistiques, l’équipe a testé ce qui se passe lorsqu’ils augmentent ou diminuent LINGO1 dans des cellules de cancer du côlon cultivées en laboratoire. Lorsqu’ils ont réduit LINGO1, les cellules tumorales se divisaient plus lentement, formaient moins de colonies et étaient moins capables de traverser des membranes artificielles mimant les barrières tissulaires. Elles perdaient aussi leur capacité à stimuler la croissance et la migration des cellules endothéliales des vaisseaux sanguins, suggérant que les tumeurs avec moins de LINGO1 pourraient être moins aptes à se vasculariser. Lorsque LINGO1 a été surexprimé dans une autre lignée cellulaire de cancer du côlon, l’effet inverse est survenu : la croissance, la migration, l’invasion et la capacité à stimuler les vaisseaux sanguins ont toutes augmenté. Chez la souris, les tumeurs implantées avec LINGO1 éteint ont crû plus lentement et présentaient moins de cellules en division active, reliant directement cette molécule à l’expansion tumorale chez l’animal vivant.
Comment LINGO1 remodèle le voisinage tumoral
L’étude a également examiné quels types de gènes et de voies sont plus actifs lorsque LINGO1 est élevé. Les profils d’expression génique ont mis en évidence des programmes cancéreux bien connus, notamment ceux qui relâchent les contacts entre cellules pour permettre la migration, et ceux qui favorisent la néovascularisation. Tout aussi important, LINGO1 élevé était associé à des changements dans « l’écosystème » entourant la tumeur. Les tumeurs riches en LINGO1 contenaient moins de lymphocytes T cytotoxiques — les cellules immunitaires capables d’attaquer directement le cancer — et plus de types cellulaires connus pour atténuer la réponse immunitaire, tels que certains macrophages et des lymphocytes T régulateurs. De nombreux « freins » moléculaires qui éteignent l’attaque immunitaire, communément appelés points de contrôle immunitaires, étaient également plus actifs lorsque LINGO1 était élevé. Des échantillons tumoraux cliniques ont confirmé que les zones à forte expression de LINGO1 présentaient peu de lymphocytes T tueurs et de faibles signes d’activité cytotoxique, tandis que les zones à faible LINGO1 étaient densément peuplées de combattants immunitaires actifs.
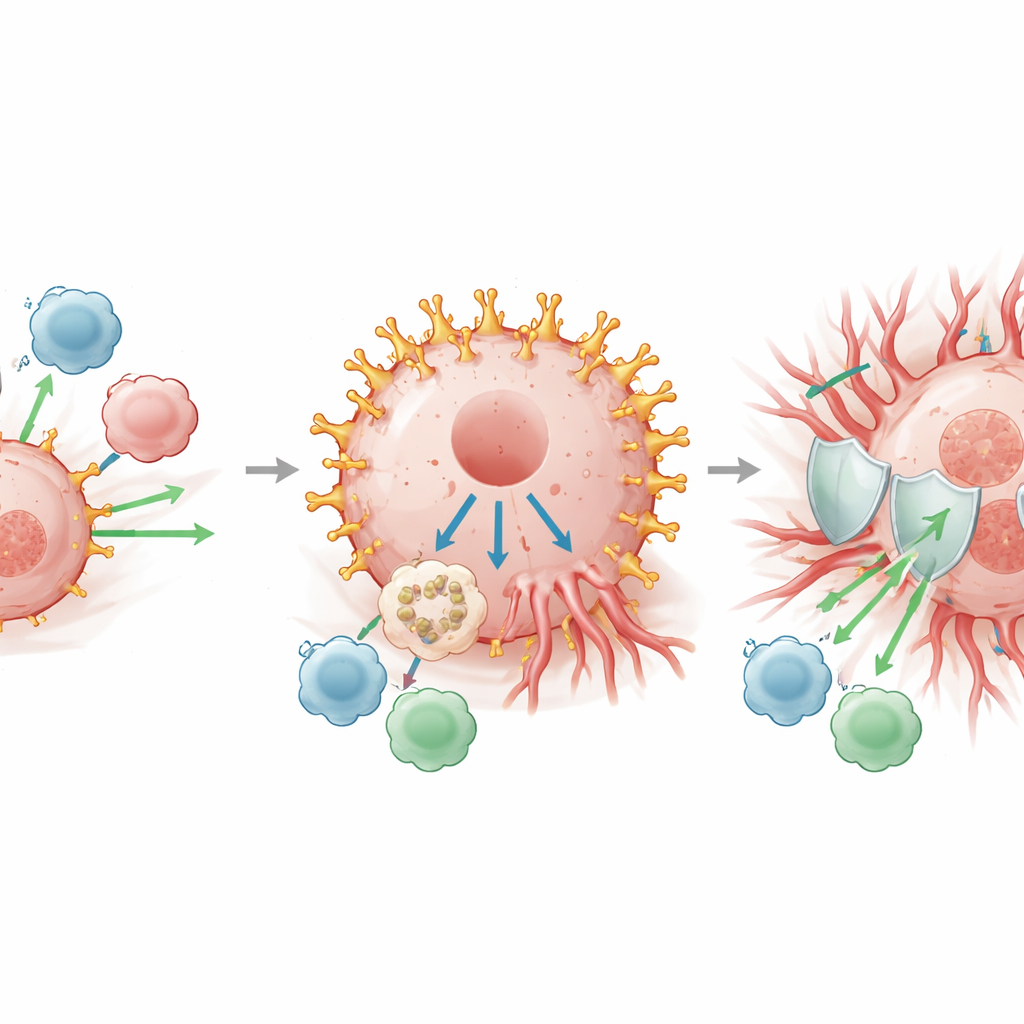
Un point de contrôle possible en amont
Pour comprendre pourquoi LINGO1 est si élevé dans ces tumeurs, les auteurs ont recherché des protéines de contrôle en amont qui pourraient agir comme des interrupteurs sur son gène. Ils ont identifié un facteur appelé USF1 qui peut se lier directement à la région régulatrice de LINGO1. Dans des expériences rapporteur, l’ajout d’USF1 a significativement augmenté l’activité de cette région, mais seulement lorsque son site de fixation était intact. Cela suggère que, dans au moins certains cancers colorectaux, USF1 contribue à monter LINGO1, qui à son tour alimente une croissance tumorale plus rapide et un environnement plus hostile pour les cellules immunitaires. Les travaux ont également montré que LINGO1 est anormalement élevé et souvent associé à de moins bons résultats dans plusieurs autres types de cancer, laissant entendre que son influence pourrait s’étendre au-delà du côlon.
Ce que cela signifie pour les patients et les soins futurs
Dans l’ensemble, l’étude dresse le portrait de LINGO1 comme d’un contributeur à double tranchant dans le cancer colorectal : il pousse les cellules tumorales à proliférer, migrer et favoriser la néovascularisation, tout en aidant la tumeur à se protéger contre l’attaque immunitaire. Parce que ses niveaux prédisent une maladie plus avancée et une survie plus mauvaise, LINGO1 pourrait servir de biomarqueur pour repérer les patients à risque plus élevé. À long terme, des médicaments qui réduisent l’activité de LINGO1 — ou qui perturbent son contrôle par USF1 — pourraient non seulement ralentir la croissance tumorale mais aussi rendre les cancers plus visibles pour le système immunitaire et plus réceptifs à l’immunothérapie.
Citation: Ma, P., Yao, F., Yue, P. et al. Transcriptional activation of LINGO1 facilitates proliferation and immune escape in colorectal cancer. Sci Rep 16, 9360 (2026). https://doi.org/10.1038/s41598-026-38760-9
Mots-clés: cancer colorectal, immunité tumorale, biomarqueurs, microenvironnement tumoral, progression du cancer