Clear Sky Science · fr
Synthèse chimique de nouveaux dérivés aminopyrimidin-4-yl-1H-pyrazole en tant qu’inhibiteurs de la tyrosine kinase splénique (SYK)
Pourquoi bloquer une seule enzyme pourrait aider à lutter contre le cancer et l’inflammation
Notre système immunitaire s’appuie sur des messages internes rapides pour dire aux cellules quand attaquer les envahisseurs et quand se calmer. Lorsque ces signaux déraillent, ils peuvent alimenter des maladies auto-immunes et le cancer. Cette étude explore une voie prometteuse pour étouffer ces signaux défectueux en concevant de petites molécules de type médicament qui bloquent sélectivement une enzyme clé, la tyrosine kinase splénique (SYK), qui se trouve au cœur de nombreuses réactions immunitaires.
Un commutateur de signal au cœur de nombreuses maladies
La SYK fonctionne comme un interrupteur maître à l’intérieur de certains types de cellules immunitaires. Lorsqu’elle est activée, elle favorise l’inflammation, la production d’anticorps et la croissance cellulaire. Dans des conditions saines, cela aide à combattre les infections. Mais dans des affections telles que la polyarthrite rhumatoïde, l’asthme et plusieurs cancers du sang et solides, l’activité de la SYK peut devenir excessive, maintenant les cellules immunitaires en état d’activation et soutenant la survie tumorale. En raison de ce rôle central, des équipes de recherche du monde entier tentent de développer des médicaments bloquant la SYK assez puissants pour être efficaces, mais suffisamment précis pour éviter d’atteindre de nombreuses autres enzymes et provoquer des effets indésirables.
Construire une famille de petites molécules sur mesure
Les auteurs ont créé une nouvelle série de molécules apparentées construites autour d’un même noyau chimique appelé aminopyrimidin-4-yl-1H-pyrazole. À partir de blocs de construction simples, ils ont assemblé ces éléments étape par étape puis modifié une portion de la structure pour obtenir neuf candidats finaux. Chaque molécule a été soigneusement contrôlée par des méthodes analytiques standard pour confirmer que sa structure et sa pureté étaient conformes aux attentes. Cette approche modulaire a permis à l’équipe d’explorer comment des changements subtils de forme et de flexibilité influencent la manière dont ces composés interagissent avec la SYK.
Observer comment les composés s’accrochent à leur cible
Avant de passer au laboratoire, les chercheurs ont utilisé des simulations informatiques pour estimer l’affinité potentielle de chaque molécule pour la SYK. Des calculs de docking ont évalué la qualité de l’ajustement des composés dans la poche de liaison de l’enzyme, mettant en évidence un candidat, désigné 44, comme particulièrement prometteur. Des simulations de dynamique moléculaire plus détaillées, au cours desquelles le complexe protéine–médicament est suivi sur des centaines de nanosecondes, ont montré que le composé 44 forme un partenariat particulièrement stable avec la SYK. La protéine restait compacte, les contacts clés demeuraient, et le système se stabilisait dans une seule conformation basse énergie avec de nombreuses liaisons hydrogène fortes, impliquant notamment des acides aminés tels que le tryptophane et la sérine qui contribuent à soutenir la molécule.
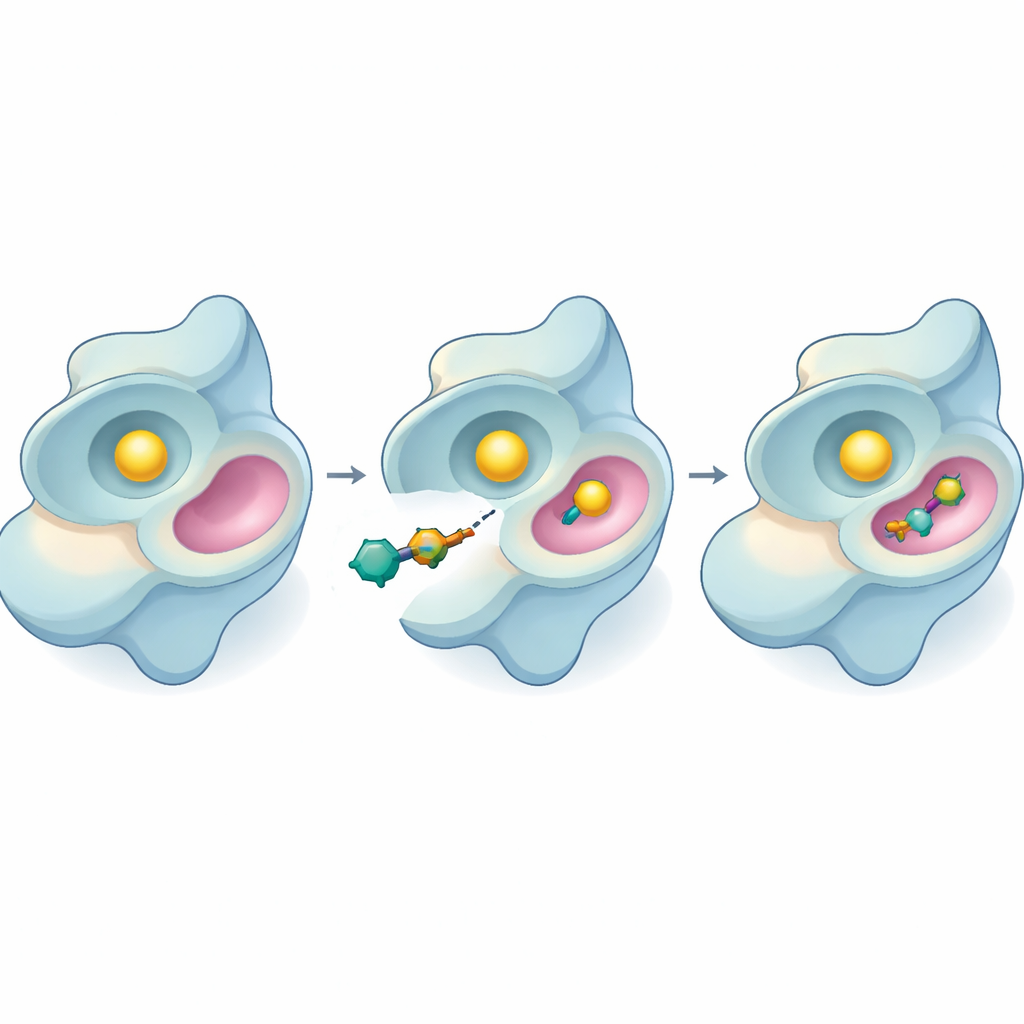
Mettre les nouveaux inhibiteurs à l’épreuve
L’équipe est ensuite passée aux expériences de laboratoire en utilisant un test lumineux qui mesure l’activité de la SYK sur sa molécule carburant, l’ATP. Plusieurs des nouveaux composés ont ralenti l’enzyme, mais le 44 s’est de nouveau distingué. Il inhibait la SYK à de très faibles concentrations et devenait plus efficace plus il restait lié à l’enzyme. En faisant varier la quantité de substrat présente, les chercheurs ont pu déduire le mode d’action de 44 : plutôt que de concurrencer directement l’ATP au site actif principal, il semble se lier à un site distinct, allostérique, et modifier le comportement de l’enzyme à distance. C’est important car les inhibiteurs allostériques conservent souvent leur effet même lorsque les niveaux d’ATP sont élevés ou lorsque des mutations altèrent le site primaire.
Ce que cela pourrait signifier pour les traitements futurs
Pris ensemble, les modèles informatiques et les mesures en laboratoire dessinent un tableau cohérent : la molécule 44 se lie fortement à la SYK, maintient l’enzyme dans un état stable et moins flexible, et inhibe son activité par un mécanisme indirect et non compétitif. Pour les non-spécialistes, cela signifie que les chercheurs ont identifié une clé chimique finement ajustée qui s’emboîte dans une serrure critique pour de nombreuses maladies à composante immunitaire, sans simplement bloquer l’ouverture principale. Bien qu’il reste beaucoup de travail — en particulier des tests cellulaires, animaux et des panels plus larges d’enzymes apparentées — ce noyau offre un point de départ prometteur pour de futurs médicaments visant à maîtriser l’inflammation nocive et ralentir certains cancers en ciblant la SYK.
Citation: Rajasheker, K.V., Pallavi, M.S., Singh, P. et al. Chemical synthesis of novel aminopyrimidin-4-yl-1H-pyrazole derivatives as spleen tyrosine kinase (SYK) inhibitors. Sci Rep 16, 8323 (2026). https://doi.org/10.1038/s41598-026-38719-w
Mots-clés: tyrosine kinase splénique, inhibiteurs de kinase, thérapeutiques contre le cancer, maladie auto-immune, médicaments allostériques