Clear Sky Science · fr
Validation des phénotypes de chimiorésistance dans le mésothéliome pleural à travers des modèles 2D, 3D et in vivo
Pourquoi certains cancers résistent à la chimiothérapie
Pour les personnes diagnostiquées avec un mésothéliome pleural — un cancer lié à l’exposition à l’amiante — la chimiothérapie est souvent l’option de traitement principale. Pourtant, de nombreuses tumeurs répondent peu, ou régressent d’abord puis rebondissent rapidement. Cette étude pose une question apparemment simple mais aux conséquences importantes : les modèles de laboratoire utilisés pour tester les médicaments sont-ils suffisamment réalistes pour prédire ce qui se passe réellement dans le corps d’un patient ?
Des couches cellulaires plates aux petites boules tumorales
La plupart des médicaments anticancéreux sont d’abord testés sur des cellules cultivées en couches plates sur des boîtes en plastique. Ces cultures bidimensionnelles (2D) sont pratiques, mais elles ne ressemblent pas aux tumeurs réelles, qui sont des masses tridimensionnelles (3D) de cellules compactes entourées d’un voisinage complexe de vaisseaux sanguins, de protéines de charpente et de cellules immunitaires. Les chercheurs ont construit un modèle de mésothéliome en « sphéroïdes » 3D, où les cellules cancéreuses se regroupent en mini-tumeurs compactes. Ils ont comparé la réponse des cellules de mésothéliome de tous les sous‑types majeurs — épithélioïde, biphasique et le très agressif sarcomatoïde — à la chimiothérapie standard lorsqu’elles étaient cultivées en couches 2D ou en sphéroïdes 3D.
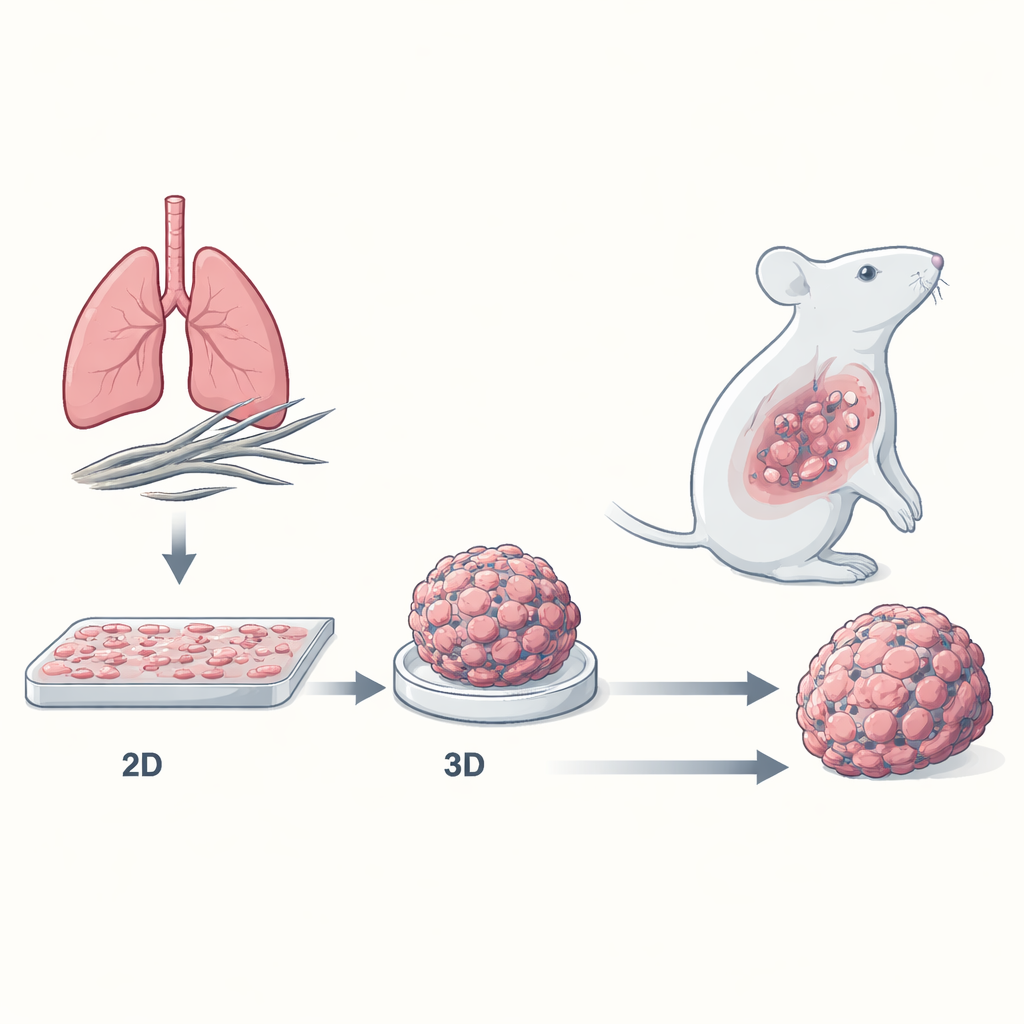
Les mini‑tumeurs 3D sont bien plus difficiles à tuer
Exposées à la combinaison couramment utilisée cisplatine–pemetrexed, les cellules de mésothéliome cultivées en 2D étaient facilement endommagées : leur croissance ralentissait, beaucoup entraient dans une phase S arrêtée du cycle cellulaire, et un grand nombre subissaient la mort programmée (apoptose). En revanche, les sphéroïdes 3D rétrécissaient à peine et nécessitaient des doses de médicament beaucoup plus élevées pour obtenir des effets comparables. Le sous‑type sarcomatoïde, connu chez les patients comme le plus difficile à traiter, était aussi le plus résistant aux médicaments dans le modèle 3D — reflétant le comportement clinique réel. Des mesures détaillées ont montré qu’après traitement, les cellules 2D perdaient leur viabilité et évoluaient vers la mort cellulaire, tandis que les cellules dans les sphéroïdes restaient majoritairement vivantes, avec seulement de faibles augmentations d’apoptose en phase précoce.
Un métabolisme plus calme et des signaux favorables à la survie
L’équipe a exploré les différences d’utilisation d’énergie entre les deux modèles à l’aide d’un « test de stress métabolique ». La chimiothérapie poussait les cellules 2D d’un état actif et énergivore vers un mode plus calme, avec des baisses marquées de la consommation d’oxygène mitochondriale — preuve que le traitement perturbait leurs centrales énergétiques internes. En revanche, les sphéroïdes 3D existaient déjà dans un état de faible énergie et pauvre en oxygène qui changeait peu avec le traitement, similaire aux conditions hypoxiques et stressées observées à l’intérieur des tumeurs réelles. Les chercheurs ont également mesuré de petites molécules régulatrices appelées microARN et trouvé des profils spécifiques aux sous‑types liés à la résistance aux médicaments. Les sphéroïdes non épithélioïdes, en particulier, augmentaient des microARN déjà associés à un mauvais pronostic et à une réduction de la mort cellulaire dans d’autres cancers. Dans des tumeurs cultivées chez la souris à partir de sphéroïdes 3D, des protéines impliquées dans des voies de survie puissantes — PI3K/AKT et VEGF/Notch — étaient suractivées, protégeant encore davantage les cellules cancéreuses de la mort.
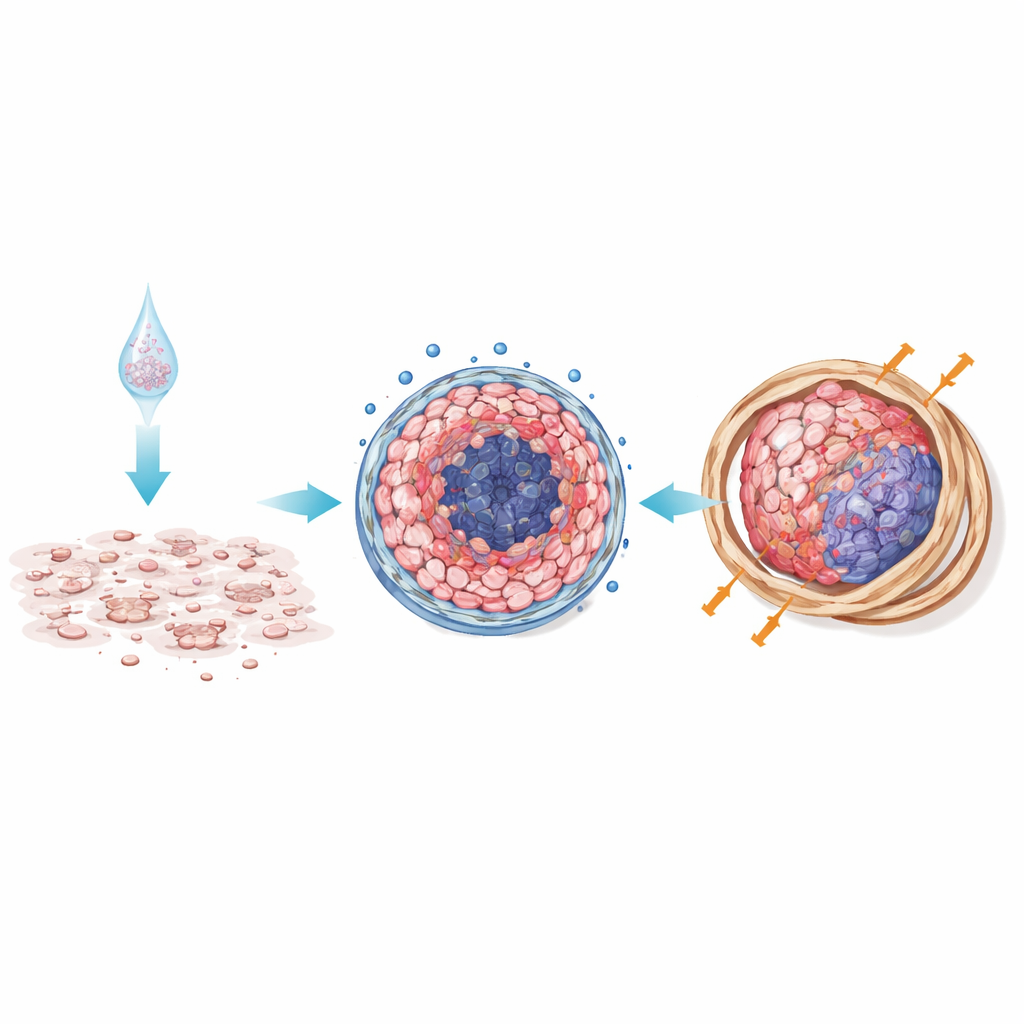
Les tumeurs murines confirment les prédictions de la boîte de culture
Pour savoir si ces différences avaient un impact in vivo, les scientifiques ont implanté des cellules de mésothéliome chez des souris soit en tant que cellules uniques (mimant la culture 2D), soit sous forme de sphéroïdes 3D préformés. Les tumeurs issues de sphéroïdes ont grandi davantage et ont moins répondu à la chimiothérapie que celles issues de cellules uniques. Au microscope, les tumeurs dérivées de 3D présentaient des bandes denses de collagène et de tissu fibreux, avec des nids cellulaires plus organisés et moins de tissu nécrotique. Cette enveloppe fibreuse agit probablement comme une barrière physique et biochimique, limitant la pénétration des médicaments et renforçant les signaux de survie — des conditions qui ressemblent étroitement aux tumeurs humaines récalcitrantes.
Ce que cela signifie pour les traitements futurs
Pour un lecteur non spécialiste, le message central est que la façon dont nous cultivons les cellules cancéreuses en laboratoire peut faire la différence pour le réalisme des tests pharmacologiques. Les petits sphéroïdes tumoraux 3D reproduisent des caractéristiques clés du mésothéliome que les couches cellulaires plates ne montrent pas : des cœurs pauvres en oxygène, des cellules en détresse mais difficiles à tuer, un tissu cicatriciel protecteur et l’activation de voies de survie qui bloquent la mort cellulaire. Parce que ces modèles 3D se comportent beaucoup plus comme de vraies tumeurs chez les patients et chez la souris, ils offrent une plateforme plus solide pour découvrir des médicaments et tester des combinaisons visant à cibler à la fois les cellules cancéreuses et leur environnement protecteur. À long terme, l’utilisation de tels modèles réalistes pourrait aider les chercheurs à identifier des traitements ayant de meilleures chances de fonctionner en clinique, pas seulement en laboratoire.
Citation: Shi, H., Selvamani, S.P., Zelei, R. et al. Validation of chemoresistance phenotypes in pleural mesothelioma across 2D, 3D, and in vivo models. Sci Rep 16, 8396 (2026). https://doi.org/10.1038/s41598-026-38692-4
Mots-clés: mésothéliome pleural, résistance à la chimiothérapie, sphéroïdes tumoraux 3D, microenvironnement tumoral, modèles d’essai de médicaments anticancéreux