Clear Sky Science · fr
Un capteur colorimétrique robuste à base d'aminothiazole pour la détection visuelle des ions Fe3+ dans des échantillons environnementaux et pharmaceutiques
Pourquoi il est important d'observer les changements de couleur de l'eau
Le fer est essentiel à la vie, mais un excès dans l'eau potable ou les médicaments peut nuire à la santé et endommager canalisations et écosystèmes. Aujourd'hui, la mesure du fer exige généralement des appareils coûteux et des techniciens formés dans des laboratoires centralisés. Cette étude présente une petite molécule organique, appelée MPTP, qui peut simplement transformer une solution jaune pâle en brun lorsqu'elle rencontre le fer sous sa forme chargée la plus courante (Fe3+). Ce changement de couleur visible peut être lu à l'œil nu ou avec un simple photomètre, ce qui facilite grandement la surveillance du fer dans les rivières, l'eau du robinet et les produits pharmaceutiques.
Une molécule minuscule qui change de couleur
Les chercheurs ont conçu et synthétisé le MPTP à partir de produits chimiques de départ simples dans un procédé en une seule étape (one-pot), c’est‑à‑dire en combinant tous les ingrédients dans une même réaction. Le cœur du MPTP est un noyau thiazole, une structure annulaire compacte qui attire naturellement les ions métalliques car elle contient des atomes d'azote et de soufre, agissant comme points d'ancrage. Dissous dans l'éthanol, le MPTP apparaît jaune pâle. Dès l'ajout d'ions Fe3+, la solution vire vers un brun net. Ce changement visible reflète un réarrangement des électrons au sein de la molécule lors de la liaison au fer, ce qui modifie son absorption de la lumière.
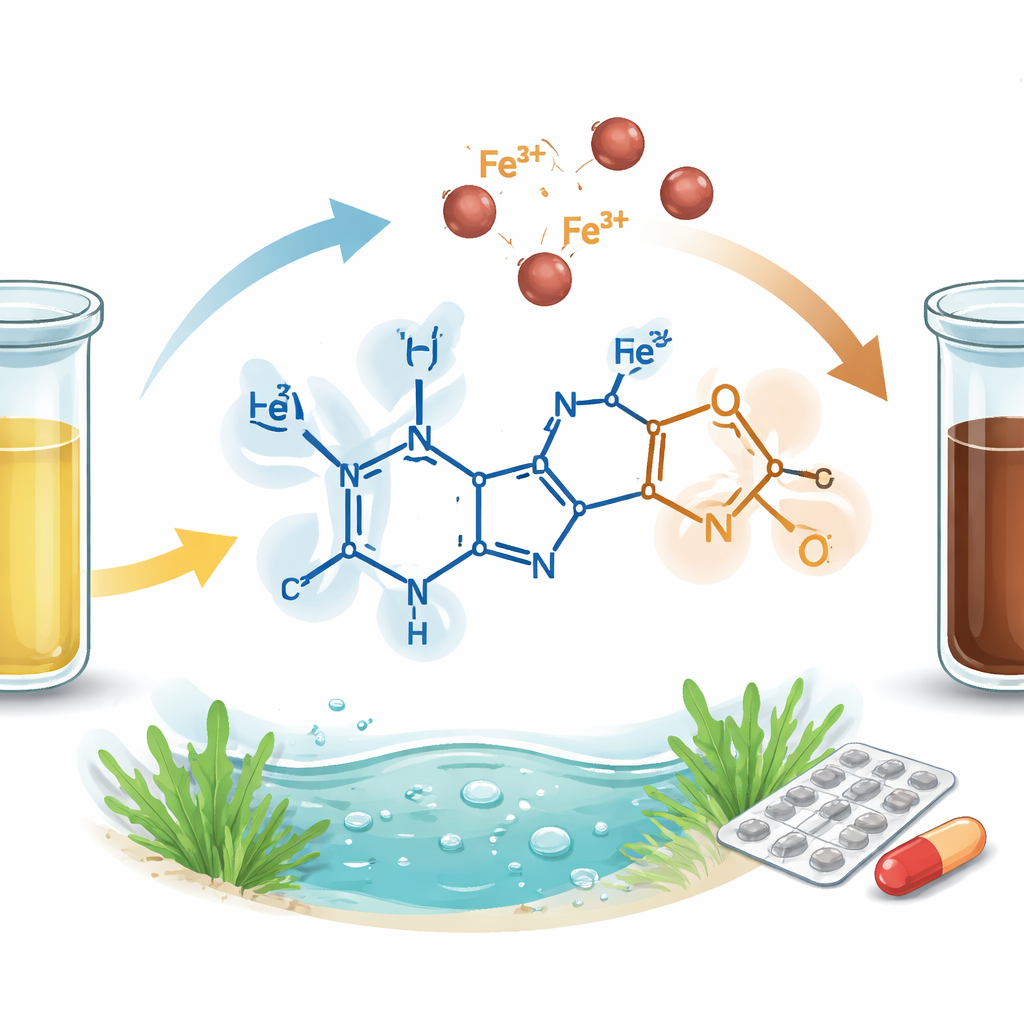
Une sélectivité visible à l'œil nu
Pour être pratique, un capteur doit répondre fortement à une cible tout en ignorant de nombreux semblables. L'équipe a soumis le MPTP à une série d'ions métalliques courants, notamment cuivre, zinc, nickel, manganèse, aluminium et d'autres. Seul le Fe3+ a produit la couleur brune frappante ; tous les autres échantillons sont restés jaune pâle. Les mesures d'absorption lumineuse confirment cela : l'ajout de Fe3+ a affiné et légèrement décalé la bande d'absorption principale du MPTP, et son intensité a presque triplé, signes clairs d'un complexe fer‑capteur stable. Le capteur tolère aussi une large gamme d'acidité et d'alcalinité — de milieux très acides à assez basiques — tout en fonctionnant au mieux dans la fenêtre quasi neutre typique des eaux naturelles et des liquides biologiques.
D'une forte affinité et de faibles besoins en fer
L'équipe a quantifié la force de liaison du MPTP envers le Fe3+ et la plus faible quantité de fer détectable. À l'aide d'une analyse standard des variations d'absorption lors de l'ajout de fer, ils ont montré qu'une molécule de MPTP lie un ion Fe3+ avec une forte constante d'affinité. La plus petite concentration détectable de manière fiable était d'environ 0,27 micromole par litre, bien en dessous de la limite fixée pour le fer dans l'eau potable par la réglementation américaine. Fait important, la liaison n'est pas irréversible : lorsqu'on ajoute un agent chélateur courant, l'EDTA, il récupère le fer et la solution redevient jaune. Le rajout de Fe3+ restaure la couleur brune. Ce comportement réversible signifie que la même solution ou le même dispositif capteur peut être utilisé à plusieurs reprises.
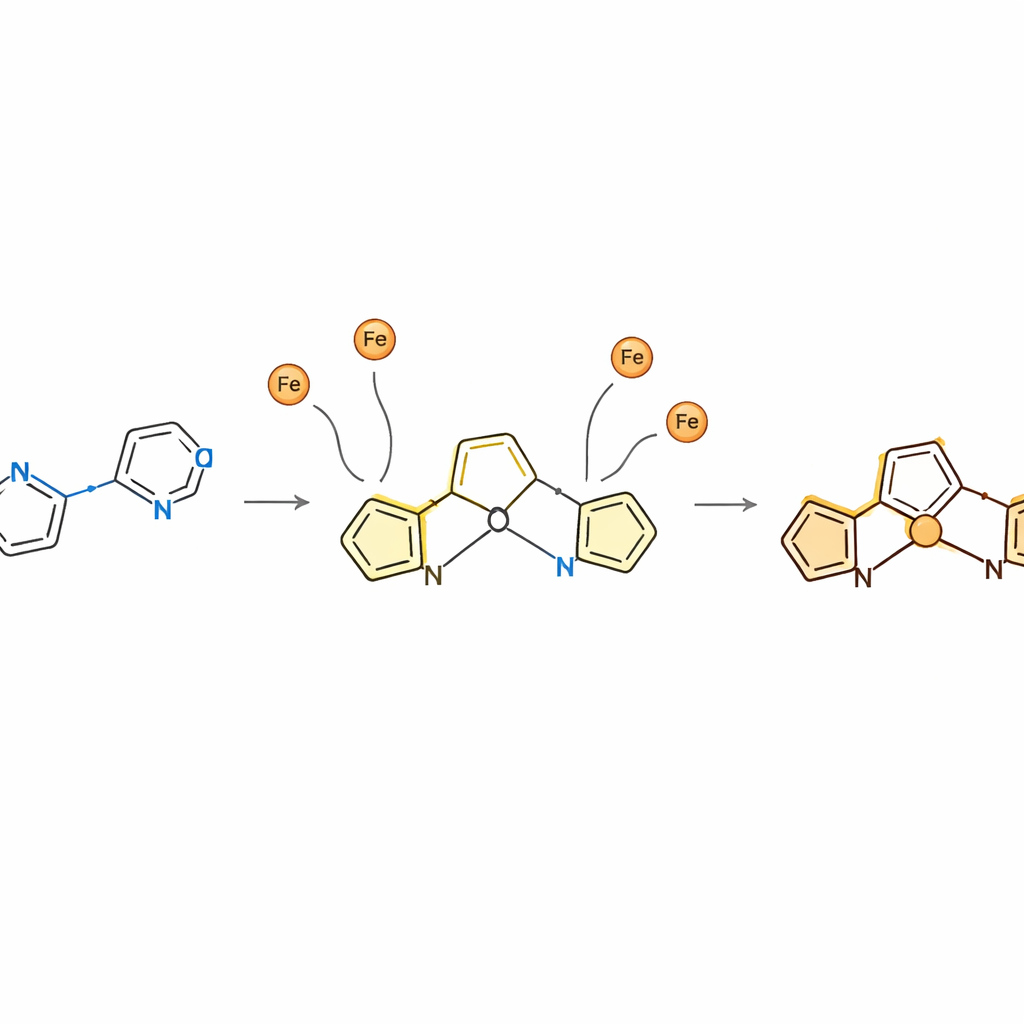
Du tube à essai à la bandelette
Pour sortir du banc de laboratoire, les scientifiques ont imbibé du papier filtre ordinaire d'une solution de MPTP puis l'ont laissé sécher. Ces bandelettes apparaissaient d'abord blanc cassé à jaune pâle. Lorsqu'elles sont plongées dans de l'eau contenant des quantités croissantes de Fe3+, elles s'assombrissent par paliers allant du beige clair au brun foncé, créant une échelle visuelle rapide. Des essais sur des cibles réelles, y compris un comprimé commercial de supplément de fer et des échantillons d'eau simulés, ont montré que le capteur retrouvait des quantités de fer très proches des valeurs connues (environ 98–102 % de précision). Des simulations informatiques de la distribution électronique de la molécule ont soutenu le tableau expérimental, mettant en évidence des régions riches en azote comme sites de liaison préférentiels pour Fe3+ et expliquant pourquoi le changement de couleur est si prononcé.
Ce que cela signifie pour les tests courants
Pris dans leur ensemble, les résultats montrent que le MPTP est une sonde colorimétrique robuste, réutilisable et facile à préparer pour le Fe3+. Elle répond rapidement, fonctionne sur une large gamme de conditions d'eau, repère le fer même en présence de nombreux autres métaux, et peut être intégrée à de simples bandelettes en papier ne nécessitant ni alimentation ni instrument. Pour les communautés surveillant la qualité de l'eau potable, les fabricants contrôlant des médicaments contenant du fer ou les agents de terrain inspectant des sites environnementaux, un tel capteur peu coûteux et lisible visuellement offre un moyen pratique de repérer des niveaux de fer problématiques avant qu'ils ne constituent un risque.
Citation: Rakshitha, G.S., Karthik, C.S., Karuppasamy, K. et al. A robust aminothiazole-based colorimetric sensor for visual detection of Fe3+ ions in environmental and pharmaceutical samples. Sci Rep 16, 9399 (2026). https://doi.org/10.1038/s41598-026-38683-5
Mots-clés: détection du fer, capteur colorimétrique, qualité de l'eau, bandelette test en papier, détection d'ions métalliques