Clear Sky Science · fr
Étude sur l'expression différentielle des gènes liés à la disulfidptose et leur association avec la régulation immunitaire chez des patients atteints de rétinopathie diabétique
Pourquoi cette maladie oculaire nous concerne tous
À mesure que le diabète se répand dans le monde, l'une de ses complications les plus redoutées est la rétinopathie diabétique, une atteinte du tissu sensible à la lumière au fond de l'œil qui peut conduire à une cécité irréversible. Les médecins ont encore du mal à prédire quels patients perdront la vue et comment mieux les protéger. Cette étude explore une forme de mort cellulaire récemment identifiée, appelée disulfidptose, et se demande si des gènes associés détectables dans le sang peuvent signaler des lésions oculaires précoces et révéler de nouvelles voies pour prévenir la perte de vision.
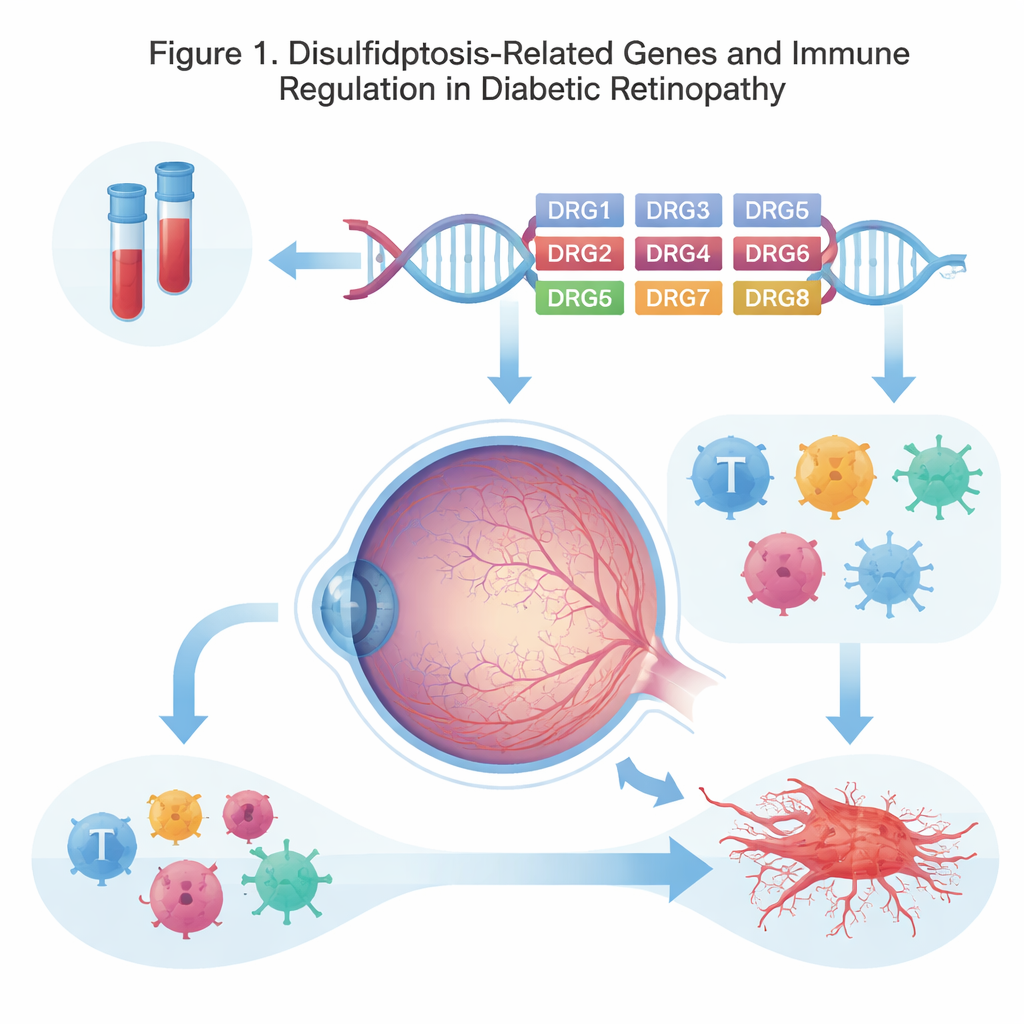
Une nouvelle forme d'effondrement cellulaire
Nos cellules se réparent et se recyclent en permanence, et de nombreuses maladies apparaissent lorsque ces programmes intrinsèques de mort cellulaire dysfonctionnent. Les chercheurs ont récemment décrit la disulfidptose, un processus dans lequel certaines liaisons chimiques au sein des protéines structurelles s'accumulent de façon anormale, déstabilisant l'échafaudage interne de la cellule et provoquant son effondrement. Comme la rétinopathie diabétique implique une hyperglycémie chronique, un stress oxydatif et des vaisseaux fragiles dans la rétine, les auteurs ont émis l'hypothèse que des gènes liés à la disulfidptose pourraient participer aux dommages lents qui privent les personnes de la vue.
À la recherche de signaux d'alerte dans le sang
L'équipe s'est tournée vers une grande base de données publique de prélèvements sanguins de personnes avec ou sans rétinopathie diabétique. Ils se sont concentrés sur 16 gènes préalablement reliés à la disulfidptose et ont comparé le niveau d'expression de ces gènes chez les patients atteints et les volontaires sains. Huit gènes se sont distingués par des différences constantes, plusieurs présentant une activité légèrement augmentée et deux une activité diminuée chez les patients atteints. Les chercheurs ont ensuite prélevé des échantillons sanguins frais de leurs propres patients hospitalisés et ont confirmé que les mêmes gènes, en particulier deux appelés FLNB et GYS1, suivaient le même schéma d'augmentation ou de diminution. Même si chaque variation génique était modeste, les changements étaient suffisamment constants à travers de nombreuses personnes pour être significatifs.
Comment les cellules sanguines et les plaquettes peuvent endommager l'œil
Les scientifiques se sont ensuite demandés quelles fonctions ces gènes pouvaient exercer. À l'aide d'outils bioinformatiques standard, ils ont trouvé que les gènes altérés étaient enrichis dans des voies liées à la coagulation sanguine, à l'activation des plaquettes et au maintien d'une circulation normale. Ces processus sont au cœur de la rétinopathie diabétique, où de minuscules capillaires rétiniens se bouchent, fuient, puis forment des néovaisseaux fragiles. Un autre groupe de voies, dont les voies de signalisation Rap1 et MAPK, contrôle la cohésion des cellules vasculaires et leur réponse au stress inflammatoire. L'étude suggère que des modifications subtiles des gènes liés à la disulfidptose pourraient pousser les plaquettes et les cellules vasculaires vers des comportements nocifs, contribuant au fil du temps à l'obstruction ou à l'affaiblissement des vaisseaux rétiniens.
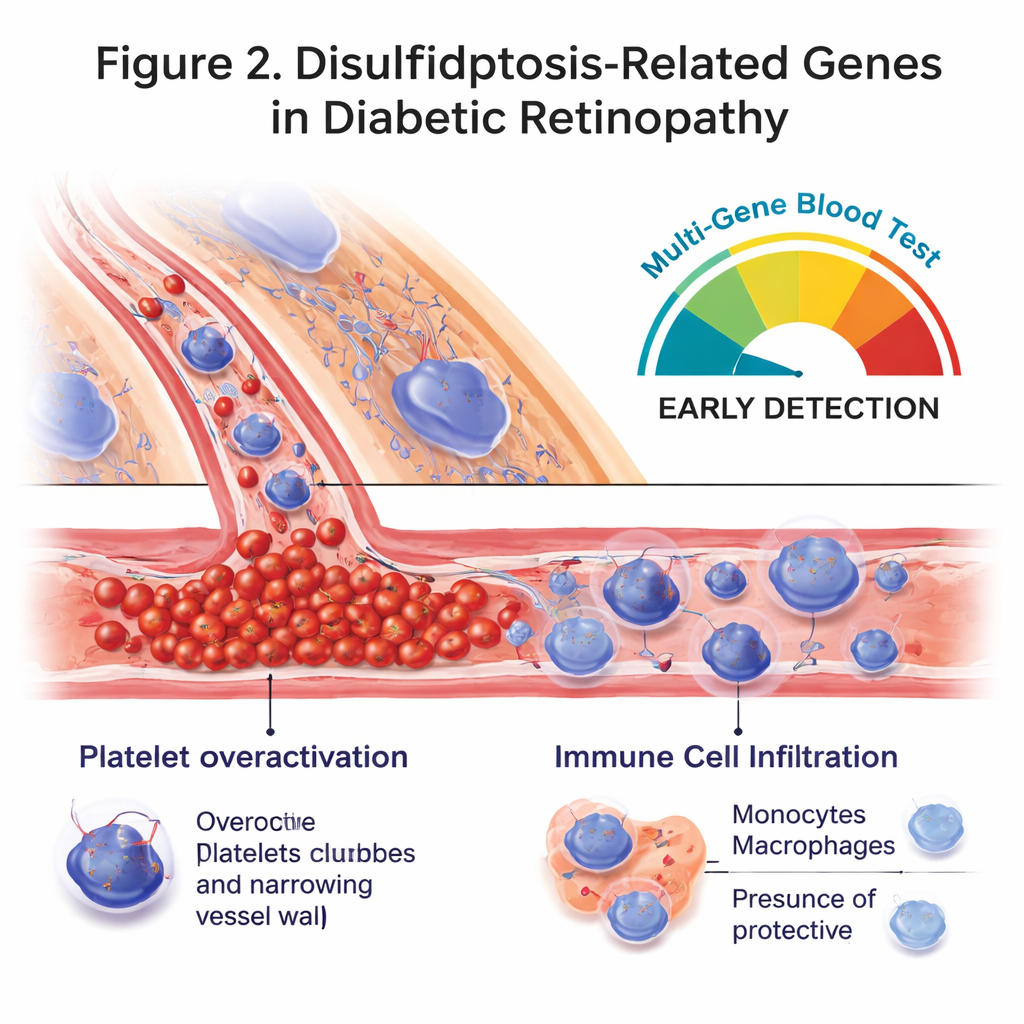
Cellules immunitaires et score de risque sanguin
Les auteurs ont également examiné les profils de cellules immunitaires dans les mêmes échantillons sanguins à l'aide de méthodes computationnelles. Les personnes atteintes de rétinopathie diabétique présentaient davantage de monocytes circulants et de macrophages en stade précoce — des cellules pouvant amplifier l'inflammation — et moins de cellules T mémoire activées, qui contribuent généralement à coordonner une réponse immunitaire équilibrée. Plusieurs des gènes liés à la disulfidptose étaient modérément associés à ces changements immunitaires, suggérant qu'ils pourraient influencer le comportement du système immunitaire dans le diabète. En s'appuyant sur ces corrélations, l'équipe a combiné les huit gènes clés en un score de risque unique à l'aide d'un modèle statistique. Cette « signature » multi‑génique distinguait les patients atteints de la maladie oculaire des témoins sains avec une précision relativement élevée, surpassant chaque gène pris isolément et offrant un schéma potentiel pour un futur test sanguin.
Ce que cela pourrait signifier pour les personnes diabétiques
Pour l'instant, ces travaux constituent surtout une preuve de concept. Le modèle a été construit à partir d'un jeu de données public et d'un groupe hospitalier relativement restreint, et l'étude n'a pas directement démontré la survenue de disulfidptose dans les tissus oculaires. Néanmoins, c'est la première étude à relier cette nouvelle voie de mort cellulaire à la rétinopathie diabétique et à proposer un ensemble de gènes sanguins reliés à la fois aux lésions vasculaires et au déséquilibre immunitaire. Si ces observations sont confirmées dans des cohortes plus larges et diversifiées, ces profils géniques pourraient devenir la base d'un test sanguin peu coûteux permettant d'identifier les individus à haut risque de perte de vision alors que leurs yeux semblent encore normaux, ouvrant la voie à une surveillance plus précoce et à des stratégies de prévention personnalisées.
Citation: Hao, Y., Zhang, XX., Wang, XY. et al. Study on the differential expression of disulfidptosis-related genes and their association with immune regulation in patients with diabetic retinopathy. Sci Rep 16, 7654 (2026). https://doi.org/10.1038/s41598-026-38671-9
Mots-clés: rétinopathie diabétique, disulfidptose, biomarqueurs, cellules immunitaires, modèle de risque génétique