Clear Sky Science · fr
ConvAHKG : graphe de connaissances hybride basé sur l’action avec une approche convolutionnelle à double canal pour le repositionnement de médicaments
Trouver de nouvelles utilisations pour d’anciens médicaments
Mettre sur le marché un médicament entièrement nouveau peut prendre plus d’une décennie et coûter des milliards de dollars, et de nombreux candidats échouent en cours de route. Cette étude explore un raccourci plus intelligent : utiliser les données et l’intelligence artificielle pour découvrir de nouvelles maladies que des médicaments existants et déjà approuvés pourraient traiter en toute sécurité. Les auteurs présentent un cadre, appelé ConvAHKG, qui tisse ensemble plusieurs types d’informations biomédicales dans une carte connectée unique, puis utilise un réseau neuronal moderne pour repérer des associations prometteuses médicament–maladie — offrant une voie plus rapide et moins coûteuse vers de nouvelles thérapies.
Une carte riche des interactions entre médicaments et maladies
Au cœur de ce travail se trouve un « graphe de connaissances hybride », une carte géante qui relie médicaments, maladies, protéines, effets secondaires, structures chimiques et voies biologiques. Plutôt que de stocker uniquement des liens simples oui–non (par exemple, « le médicament A traite la maladie B »), la carte enregistre comment un médicament agit sur une protéine : s’il l’active, l’inhibe ou s’y lie — et comment les protéines interviennent dans les maladies, par exemple comme biomarqueurs ou par des variations d’activité. Le graphe contient plus de 11 000 entités et 59 types de relations, incluant des informations détaillées sur les classifications de médicaments, les effets indésirables, les contacts protéine–protéine et les sous-structures chimiques. En capturant ces multiples couches de contexte, le graphe peut refléter davantage la complexité biologique réelle sous-jacente aux effets thérapeutiques et aux réactions indésirables. 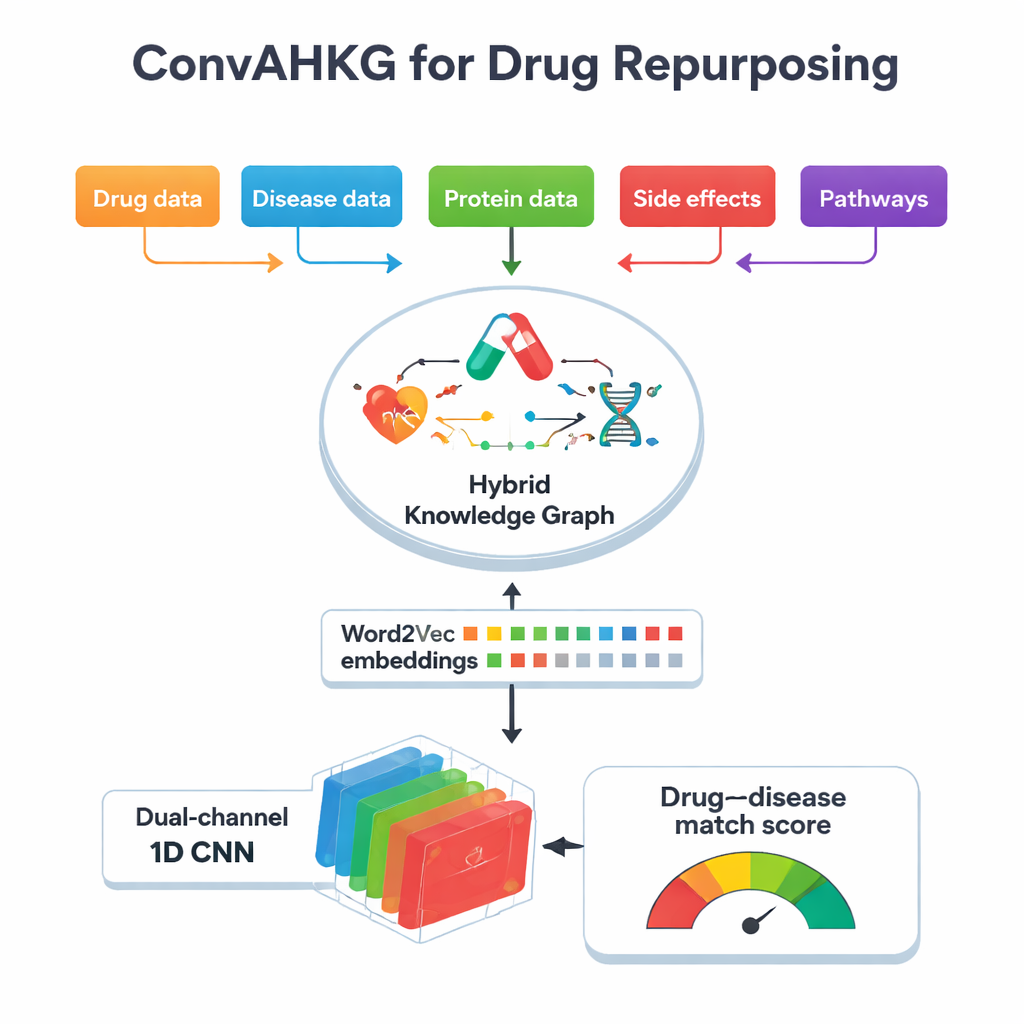
Apprendre à l’ordinateur le langage de la biologie
Pour rendre cette carte complexe exploitable par l’apprentissage automatique, l’équipe convertit chaque connexion du graphe en une simple « phrase » en trois parties : une tête (par exemple une maladie), une relation (par exemple biomarqueur) et une queue (par exemple une protéine). Ils appliquent ensuite Word2Vec, une méthode initialement développée pour le traitement du langage naturel, afin d’apprendre des « embeddings » numériques pour chaque médicament, maladie et protéine. Les éléments qui apparaissent fréquemment ensemble dans ces « phrases » se retrouvent proches les uns des autres dans cet espace mathématique, un peu comme des mots partageant des sens similaires dans un texte. Cette approche est bien plus simple et rapide que de nombreuses techniques d’embedding spécifiques aux graphes, tout en capturant des motifs subtils. Dans des tests face à plusieurs méthodes d’embedding de graphes populaires, Word2Vec a égalé ou dépassé leur pouvoir prédictif tout en nécessitant beaucoup moins de temps de calcul.
Une voie neuronale double pour des décisions traitant/ou‑non
Une fois chaque médicament et chaque maladie traduits en vecteurs numériques, ConvAHKG les injecte dans un réseau neuronal convolutionnel unidimensionnel à double canal. Un canal traite le vecteur du médicament et l’autre traite le vecteur de la maladie en utilisant une séquence de filtres convolutionnels qui détectent des motifs locaux et des motifs plus larges, s’inspirant de conceptions issues de la reconnaissance d’images telles qu’InceptionNet et AlexNet. Après ce traitement séparé, les deux flux sont fusionnés et transitent par plusieurs couches entièrement connectées qui produisent une seule probabilité : cette paire médicament–maladie représente-t-elle un traitement probablement efficace, ou plutôt un effet secondaire nuisible ? Pour gérer le fait que les paires positives connues sont beaucoup plus rares que les négatives, les auteurs introduisent une fonction de perte pondérée qui pénalise davantage les traitements vrais manqués, améliorant les performances sur ces cas difficiles à trouver. 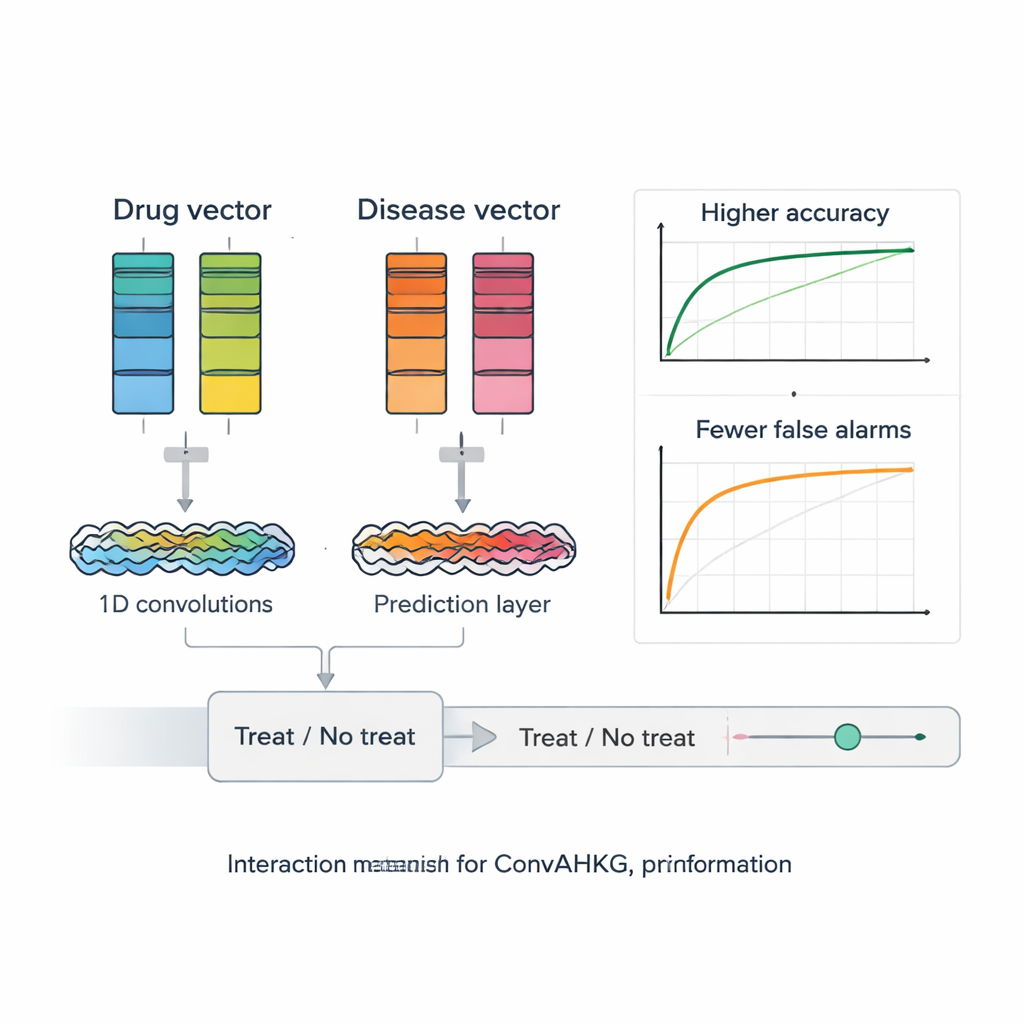
Surpasser les méthodes existantes et repérer des candidats contre le cancer
Les chercheurs testent rigoureusement leur cadre face à plusieurs outils de repositionnement de médicaments à la pointe, qui utilisent la factorisation de matrices, les graph neural networks et les autoencodeurs profonds. ConvAHKG obtient une aire sous la courbe ROC de 0,9836 et une aire sous la courbe précision–rappel de 0,9686, surpassant toutes les approches concurrentes sur le même jeu de données de référence. Ils appliquent ensuite le modèle au cancer du poumon non à petites cellules, la forme la plus courante et la plus mortelle de cancer du poumon dans le monde. ConvAHKG met en évidence plusieurs médicaments non précédemment étiquetés comme traitements pour cette maladie, notamment l’anticorps trastuzumab, qui cible la protéine HER2 et dispose déjà de preuves cliniques en cancer du poumon, ainsi que d’autres agents biologiques et même l’antibiotique classique benzylpénicilline. Des simulations de docking suggèrent que la benzylpénicilline pourrait se lier fortement à l’ADN et à la topoisomérase II alpha, une enzyme souvent surexprimée dans ces tumeurs, évoquant un possible mécanisme anticancéreux qui mérite désormais des tests en laboratoire.
Pourquoi cela compte pour les patients
En termes simples, ConvAHKG agit comme un entremetteur hautement informé entre des médicaments existants et des maladies, utilisant une carte détaillée des actions biologiques et un moteur puissant de reconnaissance de motifs pour prédire quels anciens médicaments pourraient fonctionner dans de nouveaux contextes. En considérant des médicaments déjà validés en matière de sécurité comme des blocs réutilisables plutôt que comme des outils à usage unique, ce cadre pourrait accélérer la découverte de thérapies pour des affections telles que le cancer du poumon, en particulier lorsque le développement pharmaceutique conventionnel est trop lent ou trop coûteux. Bien que les prédictions nécessitent encore une validation expérimentale et clinique rigoureuse, l’étude montre que la combinaison d’une connaissance biologique riche et d’une IA moderne peut réduire fortement l’espace de recherche, rapprochant plus rapidement des traitements potentiellement salvateurs.
Citation: Khodadadi AghGhaleh, M., Abedian, R., Zarghami, R. et al. ConvAHKG: Action-based hybrid knowledge graph with a dual-channel convolutional approach for drug repurposing. Sci Rep 16, 7592 (2026). https://doi.org/10.1038/s41598-026-38656-8
Mots-clés: repositionnement de médicaments, graphe de connaissances, apprentissage profond, cancer du poumon, découverte de médicaments