Clear Sky Science · fr
Effet de la sonication et des inhibiteurs de protéase sur la quantification par ELISA de protéines sélectionnées dans des homogénats de tissu de pis bovin
Pourquoi de petites protéines du lait comptent
Derrière chaque verre de lait se cache une usine complexe dans le pis de la vache, où des milliers de protéines coopèrent pour produire un lait sûr et nutritif. Les scientifiques mesurent souvent ces protéines pour surveiller la santé du pis et comprendre des maladies comme la mammite, une infection coûteuse dans les troupeaux laitiers. Cette étude pose une question apparemment simple mais aux conséquences pratiques importantes : la manière dont nous préparons les échantillons de tissu avant un test courant de laboratoire, appelé ELISA, fausse-t‑elle discrètement les résultats sur lesquels nous nous appuyons pour prendre des décisions ?
Comment la manipulation en laboratoire peut modifier ce que nous voyons
Pour mesurer des protéines, les chercheurs doivent d’abord ouvrir les tissus et en libérer le contenu. Dans ce travail, les scientifiques ont étudié des fragments de tissu du pis provenant de 22 vaches, la moitié saines et l’autre moitié infectée par un type de bactérie pouvant provoquer la mammite. Ils ont ensuite mesuré trois protéines importantes liées à la production laitière et à la santé du pis : l’alpha‑caséine (une protéine majeure du lait), la lactoferrine (une protéine liée à l’immunité) et la phosphatase alcaline (une enzyme associée à l’activité tissulaire). Toutes les mesures ont été réalisées par ELISA sandwich, une méthode largement utilisée pour détecter de très faibles quantités de protéines spécifiques. La subtilité est que le même tissu a été traité de quatre manières différentes avant l’analyse, pour évaluer dans quelle mesure la seule préparation pouvait modifier les valeurs finales.
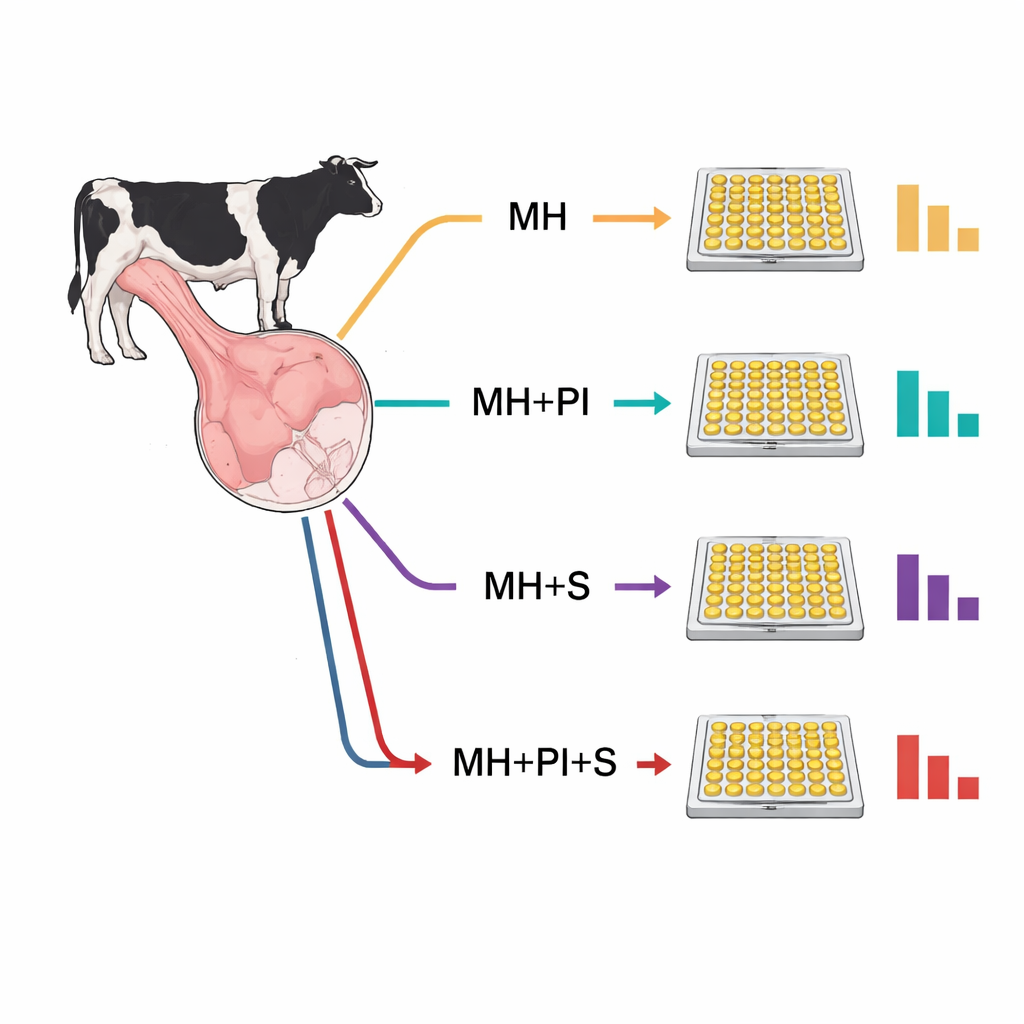
Quatre façons de traiter le même tissu
L’équipe a comparé une étape basique d’homogénéisation mécanique — broyage physique du tissu dans un tampon liquide — à trois versions plus élaborées. L’une ajoutait un cocktail d’inhibiteurs de protéases, des produits chimiques destinés à bloquer les enzymes protéolytiques libérées lors de la rupture cellulaire. Une autre incluait la sonication, des impulsions d’ondes ultrasonores qui perturbent davantage les cellules. La quatrième combinait inhibiteurs de protéases et sonication. En principe, ces étapes supplémentaires devraient soit protéger les protéines, soit mieux les libérer. En pratique, elles ont produit l’effet inverse : chaque étape additionnelle a conduit à des niveaux mesurés de protéines plus faibles par rapport à l’homogénéisation seule, et la combinaison inhibiteurs plus sonication a donné les valeurs les plus basses pour les trois protéines.
Certaines protéines diminuent plus que d’autres
Les réductions n’étaient pas égales selon les protéines. L’alpha‑caséine s’est montrée la plus résiliente, affichant la plus petite baisse lorsque des étapes de traitement supplémentaires étaient utilisées. La lactoferrine et la phosphatase alcaline, en revanche, ont chuté beaucoup plus fortement, en particulier lorsque la sonication était impliquée. Ce schéma suggère que certaines protéines sont plus vulnérables aux perturbations physiques, à la chaleur ou aux interférences chimiques, même lorsque les protocoles sont soigneusement refroidis et standardisés. L’état de santé des vaches a également joué un rôle, mais seulement pour l’alpha‑caséine : les pis infectés par des staphylocoques coagulase‑positifs présentaient des niveaux plus élevés de cette protéine du lait, tandis que la lactoferrine et la phosphatase alcaline ne différaient pas nettement entre animaux sains et infectés. Il est crucial de noter toutefois que le sens et l’ampleur des baisses liées au traitement étaient similaires dans les groupes sains et infectés.
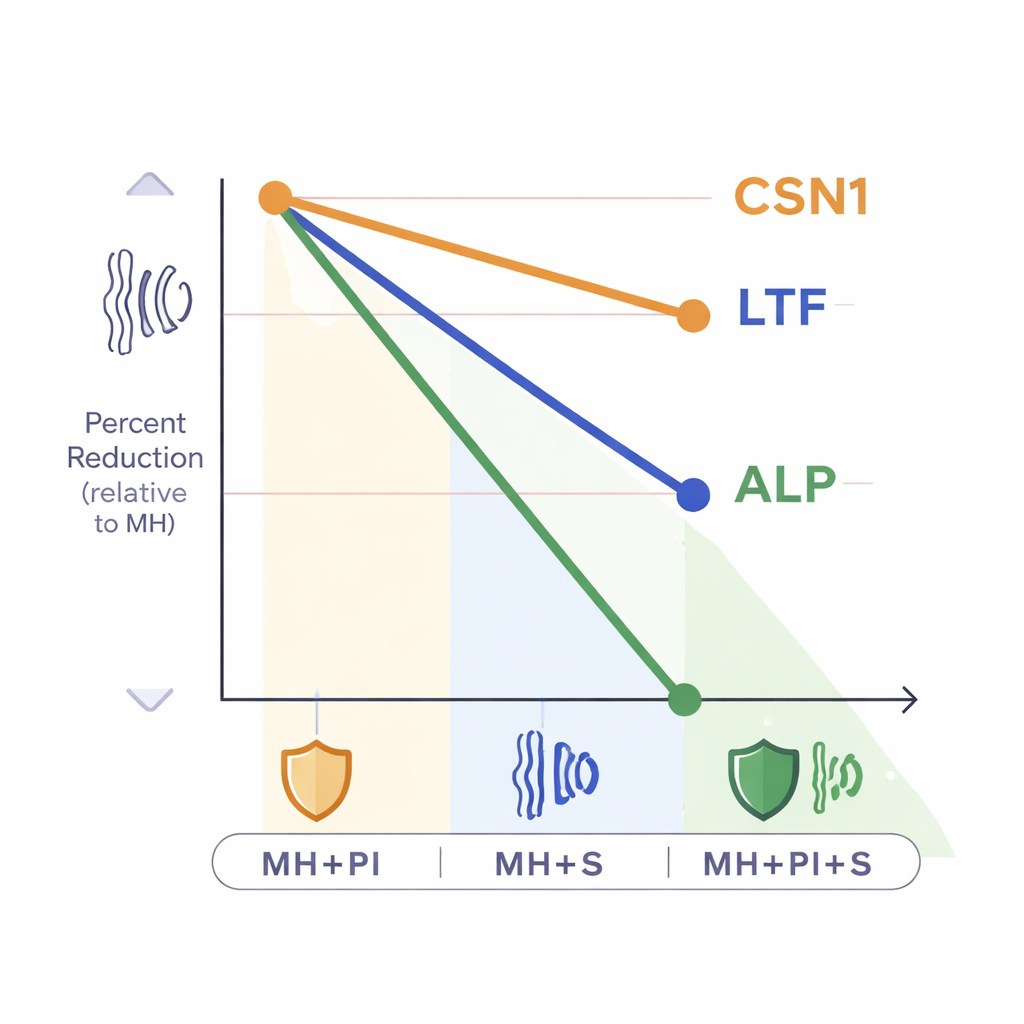
Quand la protection se retourne contre nous
Pourquoi des étapes conçues pour aider — comme les inhibiteurs de protéase et la sonication — conduiraient-elles à des niveaux mesurés plus faibles ? L’étude n’a pas disséqué les raisons moléculaires exactes, mais elle évoque plusieurs possibilités. La sonication peut générer de la chaleur et des forces physiques intenses qui endommagent partiellement les protéines ou altèrent les épitopes reconnus par les anticorps de l’ELISA. Les inhibiteurs de protéase, tout en bloquant les enzymes naturels, peuvent eux‑mêmes interférer avec l’essai en se liant de manière non spécifique ou en affectant la chimie de détection. Quel que soit le mécanisme, le message est clair : ces compléments largement recommandés peuvent systématiquement abaisser les mesures ELISA, et ils le font à des degrés différents selon les protéines.
Ce que cela signifie pour la recherche laitière et le diagnostic
Pour les éleveurs, les vétérinaires et les experts en sécurité alimentaire, les résultats ELISA guident les décisions sur la santé animale, la qualité du lait et la sécurité des procédés. Cette étude montre que le simple choix d’un protocole de préparation plus complexe peut faire paraître les protéines cibles nettement plus rares qu’elles ne le sont réellement. Dans le tissu du pis bovin, la méthode la plus simple — l’homogénéisation mécanique seule — a en fait fourni les concentrations de protéines les plus élevées et les plus comparables. Pour les non‑spécialistes, la conclusion est nette : avant d’interpréter des quantités de protéines comme un signe de maladie, de qualité du lait ou d’efficacité d’un traitement, les chercheurs doivent standardiser avec soin la manipulation des échantillons. Sans cela, les différences de résultats peuvent refléter davantage la brutalité des étapes de préparation en laboratoire que la biologie réelle à l’intérieur de la vache.
Citation: Szprynca, A., Czopowicz, M., Zalewska, M. et al. Effect of sonication and protease inhibitors on Elisa quantification of selected proteins in bovine udder tissue homogenates. Sci Rep 16, 7366 (2026). https://doi.org/10.1038/s41598-026-38653-x
Mots-clés: Préparation d'échantillons ELISA, mammite bovine, protéines du tissu mammaire, effets de la sonication, inhibiteurs de protéase