Clear Sky Science · fr
Transfert de protons induit par la lumière dans des eaux de structures différentes : une approche RMN électronique pour résoudre un problème classique
Pourquoi les voyages cachés des protons comptent
Chaque fois que vous respirez, réfléchissez ou convertissez la lumière du soleil en énergie utile dans une cellule solaire, de minuscules particules chargées positivement appelées protons sont en mouvement. La façon dont ces protons se déplacent dans l'eau est une énigme vieille de plusieurs siècles, posée pour la première fois par le scientifique Theodor Grotthuss en 1806. Cette nouvelle étude utilise une combinaison astucieuse de lumière et de mesures magnétiques pour observer le déplacement des protons dans des eaux de structures différentes : des solutions salées et encombrées aux mélanges vitreux et glacés, et même à l'intérieur d'une protéine membranaire. Le travail propose une manière nouvelle de tester les idées classiques sur le mouvement des protons et d'explorer des environnements difficiles à étudier par d'autres méthodes.
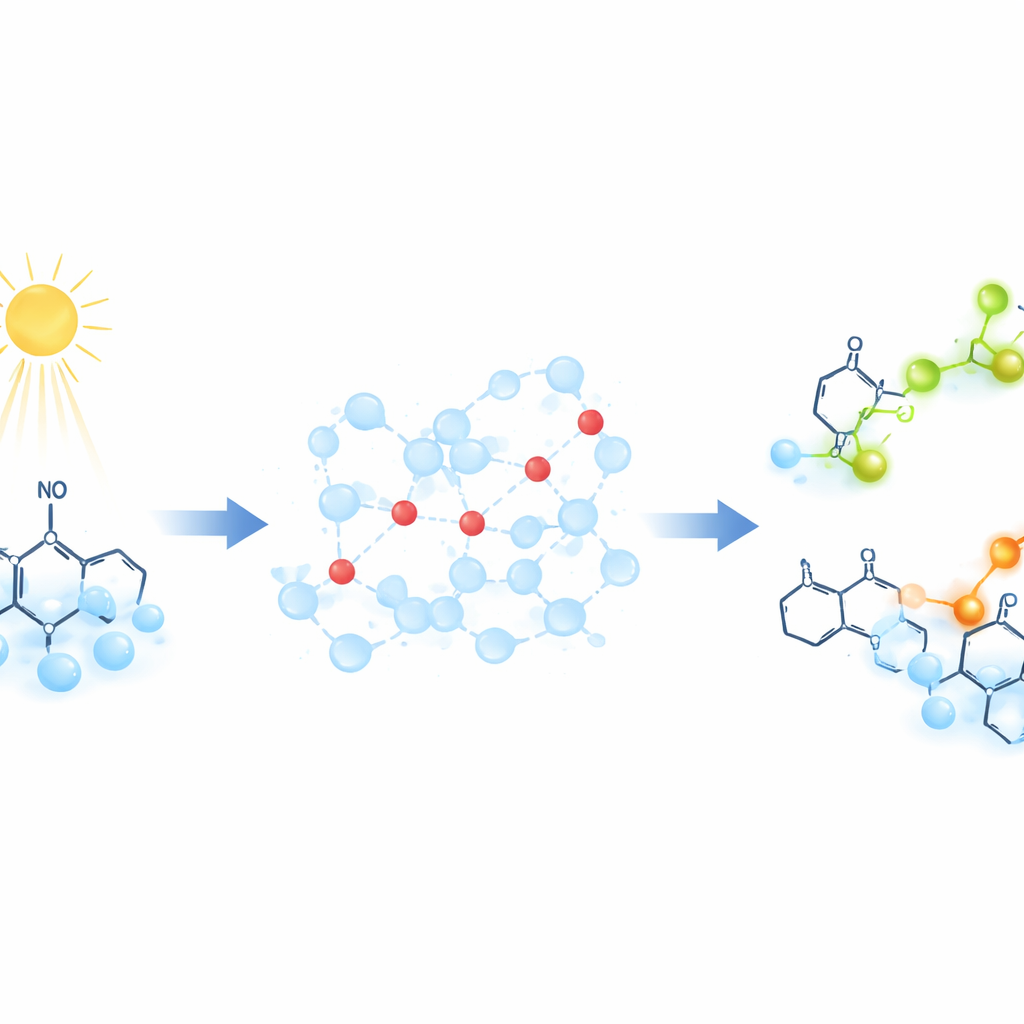
Une nouvelle façon d’observer les protons en mouvement
Plutôt que de suivre les protons directement, les chercheurs utilisent des molécules « sondes » spéciales qui modifient leur signature magnétique lorsqu’elles captent un proton. Ces sondes sont des radicaux organiques stables dont l’électron non apparié produit un signal bien défini en résonance paramagnétique électronique (EPR), une technique qui détecte la réponse des électrons non appariés à un champ magnétique. Pour déclencher le mouvement des protons à la demande, l’équipe éclaire un composé appelé 2‑nitrobenzaldéhyde. Cette réaction photo‑induite libère une rafale de protons en moins d’un milliardième de seconde, abaissant soudainement le pH de la solution. À mesure que les protons se propagent dans l’eau et se lient aux sondes, le signal EPR se décale de façon dépendante du temps, ce qui permet aux scientifiques de suivre la vitesse du transfert de protons.
Comment le voisinage de l’eau ralentit ou accélère le flux
L’eau existe rarement seule ; elle est généralement encombrée d’ions dissous ou d’autres molécules qui réarrangent subtilement son réseau de liaisons hydrogène. L’équipe a testé l’effet de ces additifs sur le mouvement des protons en comparant l’eau pure à des solutions contenant du chlorure de potassium, de l’urée ou du chlorhydrate de guanidinium, toutes à haute concentration. En ajustant les variations EPR à des modèles cinétiques simples, ils ont extrait des vitesses apparentes de transfert de protons. Ils ont constaté que dans 6 molaires de chlorhydrate de guanidinium, le transfert de protons était environ 40 fois plus lent que dans l’eau pure, tandis que 8 molaires d’urée n’entraînaient qu’un ralentissement modeste, et le chlorure de potassium produisait des effets intermédiaires. Comme la vitesse à laquelle les protons réagissent avec les sondes est limitée par leur déplacement dans le réseau de liaisons hydrogène, ces différences indiquent des changements substantiels dans la structure de l’eau autour des ions et molécules ajoutés.
Mouvement des protons dans la glace vitreuse et à l’intérieur des protéines
La méthode ne se limite pas à l’eau liquide ordinaire. Les auteurs ont aussi étudié un mélange eau–glycérol refroidi à 160 kelvins, où il forme un verre rigide. La diffusion libre des molécules y est essentiellement figée, pourtant le signal EPR montrait toujours que les sondes étaient protonées après exposition à la lumière. Cela suggère que le transfert de protons peut se produire sans diffusion classique, possiblement par effet de tunnel quantique le long d’une chaîne de liaisons hydrogène, ce qui fait écho aux raffinements modernes de l’idée de Grotthuss. Pour explorer la pertinence biologique, l’équipe a fixé un radical sensible au pH à un site précis de la protéine membranaire bactériorhodopsine, à la frontière entre la protéine et l’eau environnante. Lorsqu’ils ont déclenché la libération de protons par la lumière, ils ont observé une réponse EPR dépendante du temps en ce site marqué, démontrant que leur approche peut surveiller la livraison de protons à une position définie sur la surface d’une protéine.
Relier structure, eau et autoroutes protoniques
Pour mieux comprendre pourquoi la sonde liée à la protéine se comportait de manière très similaire à celle dans l’eau en vrac, les chercheurs ont exécuté des simulations informatiques de la bactériorhodopsine dans une membrane et d’un petit peptide en solution. Ils ont calculé comment les molécules d’eau entourent le groupe nitroxyle de l’étiquette de spin et ont trouvé des schémas d’hydratation locale presque identiques dans les deux cas, avec seulement un léger blindage dû à l’environnement membranaire. Cela signifie que, du moins pour le site étudié, les protons ont accès par une couche d’eau qui ressemble étroitement à l’eau liquide ordinaire. Les auteurs montrent également que leurs sondes peuvent être utilisées dans des expériences EPR résolues en temps, ouvrant la porte au suivi conjoint du mouvement des protons et des électrons dans des réactions où les deux sont étroitement couplés.
Ce que ce travail nous dit en termes simples
Essentiellement, cette étude transforme la lumière en un coup de départ net pour le mouvement des protons, puis utilise des sondes magnétiques sensibles pour observer la rapidité avec laquelle ces protons atteignent différentes cibles. En comparant des solutions salines simples, des dénaturants denses, des mélanges vitreux et une protéine membranaire, les chercheurs montrent que le flux de protons est fortement façonné par l’agencement des molécules d’eau et par l’environnement environnant. Leur approche soutient non seulement l’idée que les protons sautent le long de réseaux de liaisons hydrogène, mais révèle aussi que ce saut peut persister même lorsque le mouvement moléculaire ordinaire est presque figé. Cette nouvelle boîte à outils pourrait aider les scientifiques à disséquer comment les protons se déplacent dans les enzymes, les systèmes de conversion d’énergie et les matériaux innovants, nous rapprochant du contrôle de ces porteurs de charge minuscules mais puissants.
Citation: Barbon, A., Savitsky, A., Grigoriev, I. et al. Photoinduced proton transfer in differently structured water: an EPR approach to solving a classic problem. Sci Rep 16, 7983 (2026). https://doi.org/10.1038/s41598-026-38650-0
Mots-clés: transfert de protons, structure de l'eau, résonance paramagnétique électronique, réseau de liaisons hydrogène, bactériorhodopsine