Clear Sky Science · fr
Prolifération et effets anti-apoptotiques induits par DNMT3A p.R882C dans les cellules du cancer du pancréas
Pourquoi cette recherche est importante pour le cancer du pancréas
Le cancer du pancréas est tristement célèbre pour être souvent diagnostiqué tard, se propager rapidement et répondre faiblement aux traitements. La plupart des patients reçoivent un diagnostic d’adénocarcinome canalaire pancréatique (PDAC), une forme particulièrement agressive de la maladie. Cette étude se concentre sur une modification minime d’un seul gène, appelé DNMT3A, et pose une grande question : cette altération subtile peut‑elle aider à expliquer pourquoi certains cancers du pancréas croissent plus vite et résistent à la mort cellulaire ? Comprendre de tels changements pourrait ouvrir la voie à une détection plus précoce et à des thérapies ciblées plus précises.
Un examen approfondi d’un cancer mortel
Le PDAC représente plus de 90 % des cancers du pancréas et affiche un taux de survie à cinq ans inférieur à 13 %. Il est généralement entraîné par des gènes cancéreux bien connus comme KRAS et TP53, mais de nombreux patients ne bénéficient toujours pas des traitements ciblés actuels. Des travaux récents suggèrent que, au‑delà des mutations géniques, des changements « épigénétiques » — des marquages chimiques sur l’ADN qui contrôlent l’activation ou la désactivation des gènes — jouent un rôle clé dans ce cancer. DNMT3A est l’une des principales enzymes qui écrivent ces marques chimiques, et ses défauts ont déjà été associés à des cancers du sang comme la leucémie myéloïde aiguë.
À la recherche de modifications dangereuses de l’ADN
Les chercheurs ont collecté des échantillons tumoraux et des tissus non cancéreux adjacents chez trois patients atteints d’un PDAC modérément à mal différencié. Ils ont utilisé le séquençage de l’exome complet, une technique qui lit toutes les régions codantes du génome, puis appliqué des filtres informatiques stricts pour distinguer les variations d’ADN bénignes de celles susceptibles d’altérer le comportement cellulaire. Parmi des centaines d’altérations, ils ont réduit la liste à 68 changements à haut risque. Parmi ceux‑ci, une variante rare de DNMT3A, connue sous le nom p.R882C, s’est distinguée car elle apparaît presque jamais dans les grandes bases de population et était systématiquement considérée comme délétère par plusieurs outils de prédiction.
Ce que fait cette mutation à l’intérieur des cellules
DNMT3A est une protéine de 912 acides aminés qui aide à établir les motifs de méthylation de l’ADN — des étiquettes chimiques qui fonctionnent comme des interrupteurs d’activation ou d’inhibition des gènes. La substitution p.R882C se situe dans une région de travail cruciale de DNMT3A, où elle pourrait perturber l’activité de l’enzyme. À l’aide de modèles informatiques 3D, l’équipe a constaté que la conformation globale de la protéine ne changeait pas de manière spectaculaire, ce qui suggère que le problème pourrait résider dans le fonctionnement de l’enzyme plutôt que dans son repliement. Pour tester cela, ils ont modifié génétiquement des lignées cellulaires du cancer du pancréas (PANC‑1 et PaTu 8988t) afin qu’elles produisent soit le DNMT3A normal, soit la version p.R882C, et les ont comparées à des cellules portant un vecteur témoin vide.
Croissance accélérée, mobilité accrue, mort cellulaire réduite
De manière surprenante, la mutation p.R882C n’a pas modifié la quantité de DNMT3A produite au niveau de l’ARN ou de la protéine ; la quantité d’enzyme est restée à peu près la même. Cependant, sa présence a eu des effets frappants sur le comportement cellulaire. Dans des tests de formation de colonies et de prolifération, les cellules porteuses du DNMT3A mutant ont formé davantage de colonies et montré des signaux de croissance plus élevés que celles exprimant la version normale. Les tests de cicatrisation (wound‑healing) et de Trans‑well, qui mesurent la vitesse de migration des cellules, ont révélé que les cellules mutant‑porteuses migraient plus rapidement. Lorsque l’équipe a examiné la mort cellulaire programmée (apoptose) par cytométrie en flux, les cellules portant la mutation p.R882C présentaient nettement moins de cellules en train de mourir, aux stades précoces comme tardifs de l’apoptose, indiquant un avantage de survie marqué.
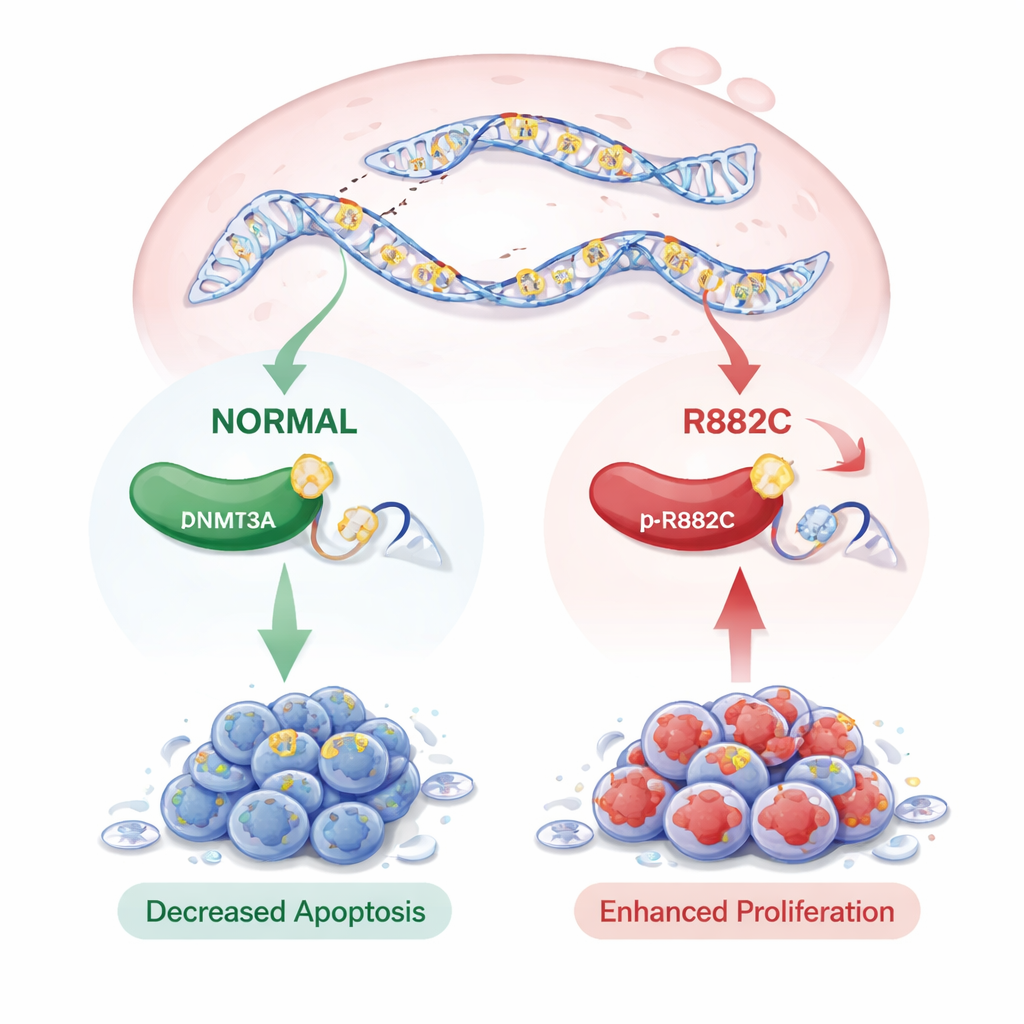
Ce que cela pourrait signifier pour les soins futurs
En synthèse, l’étude suggère que la rare mutation DNMT3A p.R882C favorise la croissance plus rapide des cellules du cancer du pancréas, augmente leur mobilité et les rend résistantes à l’autodestruction — des caractéristiques qui peuvent contribuer à la progression tumorale. Bien que la mutation n’augmente pas le niveau de DNMT3A, elle modifie probablement l’activité de l’enzyme et le motif de marquages de l’ADN à l’échelle du génome, rappelant des observations faites dans certains cancers du sang. Les auteurs soulignent que cette altération est peu fréquente et n’a pas encore montré de lien clair avec la survie des patients dans les bases de données publiques, en partie parce que les études disponibles sont petites et incluent souvent pas DNMT3A. Néanmoins, la découverte de cette mutation dans le PDAC met en lumière un acteur potentiellement important de la maladie et ouvre la possibilité que, à l’avenir, DNMT3A p.R882C puisse servir de marqueur de risque ou de cible pour des traitements plus personnalisés.
Citation: Qu, Z., Mao, J., Qian, Y. et al. DNMT3A p.R882C driven proliferation and anti-apoptotic effects in pancreatic cancer cells. Sci Rep 16, 7659 (2026). https://doi.org/10.1038/s41598-026-38613-5
Mots-clés: cancer du pancréas, mutation DNMT3A, PDAC, méthylation de l'ADN, thérapie ciblée