Clear Sky Science · fr
Édition du génome chez les espèces de Dictyostelia permettant la génétique fonctionnelle comparative des amibes sociales
Comment des cellules seules se rassemblent
La plupart du temps, les amibes sont de petits solitaires qui rampent dans le sol et mangent des bactéries. Pourtant certaines d’entre elles, appelées amibes sociales, peuvent soudainement se regrouper pour former un organisme multicellulaire avec une « tête » et une « tige » primitives. Ce mode de vie polymorphe offre aux scientifiques une rare fenêtre sur la manière dont des cellules simples apprennent à coopérer et à se spécialiser — des étapes clés dans l’évolution du vivant complexe. La nouvelle étude décrit une boîte à outils d’édition du génome qui permet enfin aux chercheurs d’étudier ces comportements non seulement dans l’espèce modèle habituelle, mais à travers plusieurs espèces d’amibes éloignées.
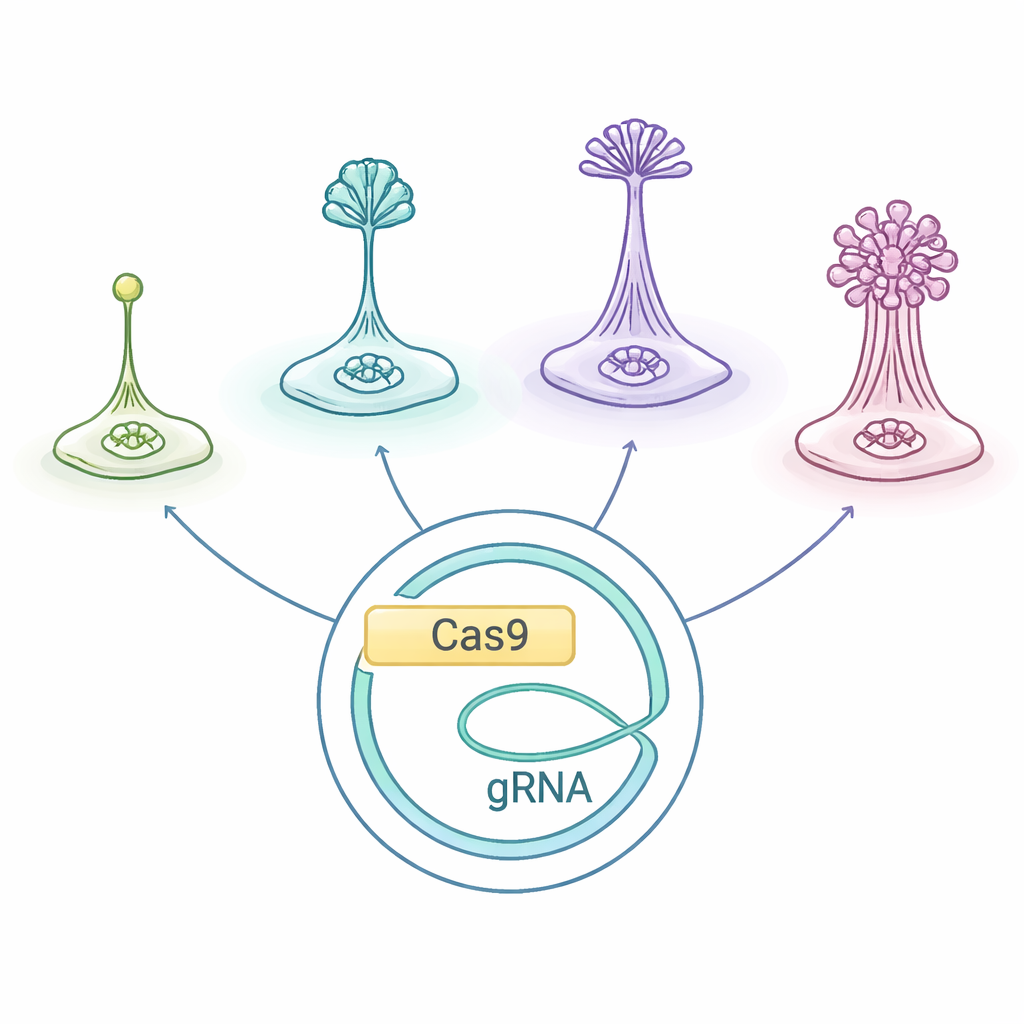
De minuscules créatures au riche sociabilité
Les amibes sociales, regroupées sous le nom de Dictyostelia, vivent comme des cellules individuelles quand la nourriture est abondante. Lorsqu’elles sont privées de nutriments, elles émettent des signaux chimiques de détresse et migrent les unes vers les autres, formant un monticule qui construit un petit « corps fructifère » : une colonne de cellules sacrifiées qui élève des spores résistantes dans l’air. Différentes lignées de Dictyostelia bâtissent ces structures de façons variées et avec des ensembles de types cellulaires différents, ce qui en fait un laboratoire naturel pour comprendre comment apparaissent les corps multicellulaires et la division du travail.
Une espèce modèle ne suffisait pas
Jusqu’à présent, presque tout le travail moléculaire s’est concentré sur une seule espèce, Dictyostelium discoideum, parce que ses gènes sont relativement faciles à modifier. Cela a laissé plus d’une centaine d’autres espèces connues — certaines représentant des branches plus anciennes de l’arbre des Dictyostelia — largement inexplorées. Ces espèces négligées ont des histoires de vie, des systèmes de signalisation et des plans corporels distincts. Pour comprendre comment la multicellularité a évolué au fil du temps, les scientifiques doivent pouvoir manipuler les mêmes gènes dans beaucoup de ces espèces et comparer les résultats côte à côte.
Adapter le CRISPR à une famille diversifiée d’amibes
Les chercheurs ont adapté un système d’édition CRISPR/Cas9 initialement optimisé pour D. discoideum et ont testé s’il fonctionne à travers l’arbre des Dictyostelia, incluant des espèces à embranchements précoces et des espèces plus dérivées. Ils ont utilisé un plasmide — un petit ADN circulaire supplémentaire — qui porte les instructions pour les « ciseaux moléculaires » Cas9, l’ARN guide qui oriente Cas9 vers un gène choisi, et un marqueur de résistance aux médicaments. L’introduction de ce plasmide dans différentes amibes a permis à l’équipe de couper deux gènes bien étudiés, nommés stlA et pkaC, importants pour les signaux qui coordonnent l’agrégation et la formation correcte du corps fructifère. Chez l’amibe du sol Polysphondylium violaceum, cette stratégie a produit de manière fiable des mutants présentant des défauts développementaux nets, montrant que le système emprunté peut fonctionner en dehors du modèle habituel.
Tester des gènes à travers les espèces
Ensuite, l’équipe est passée à des espèces plus éloignées, notamment Heterostelium pallidum du groupe 2 et Cavenderia fasciculata du groupe 1 — des lignées qui se sont séparées plus tôt au cours de l’évolution. En utilisant le même design de plasmide, ils ont perturbé le gène pkaC dans les deux espèces et ont constaté que les mutants ne parvenaient pas à s’agréger ni à construire des corps fructifères normaux, reproduisant les défauts sévères observés chez D. discoideum. Parce que les mutations CRISPR créées par cette méthode ne laissent pas de gros cassettes de sélection, les souches obtenues étaient « sans marqueur ». Cela a rendu simple l’ajout d’une version du gène provenant de D. discoideum pour tester si elle pouvait remplacer la version locale. Dans tous les cas, le pkaC étranger a pu restaurer l’étape initiale d’agrégation mais pas la phase ultérieure de sculpture d’un corps fructifère mature — preuve que l’outillage de signalisation de base est partagé, tandis que le contrôle fin du timing et de la position a évolué de manière spécifique à chaque espèce.
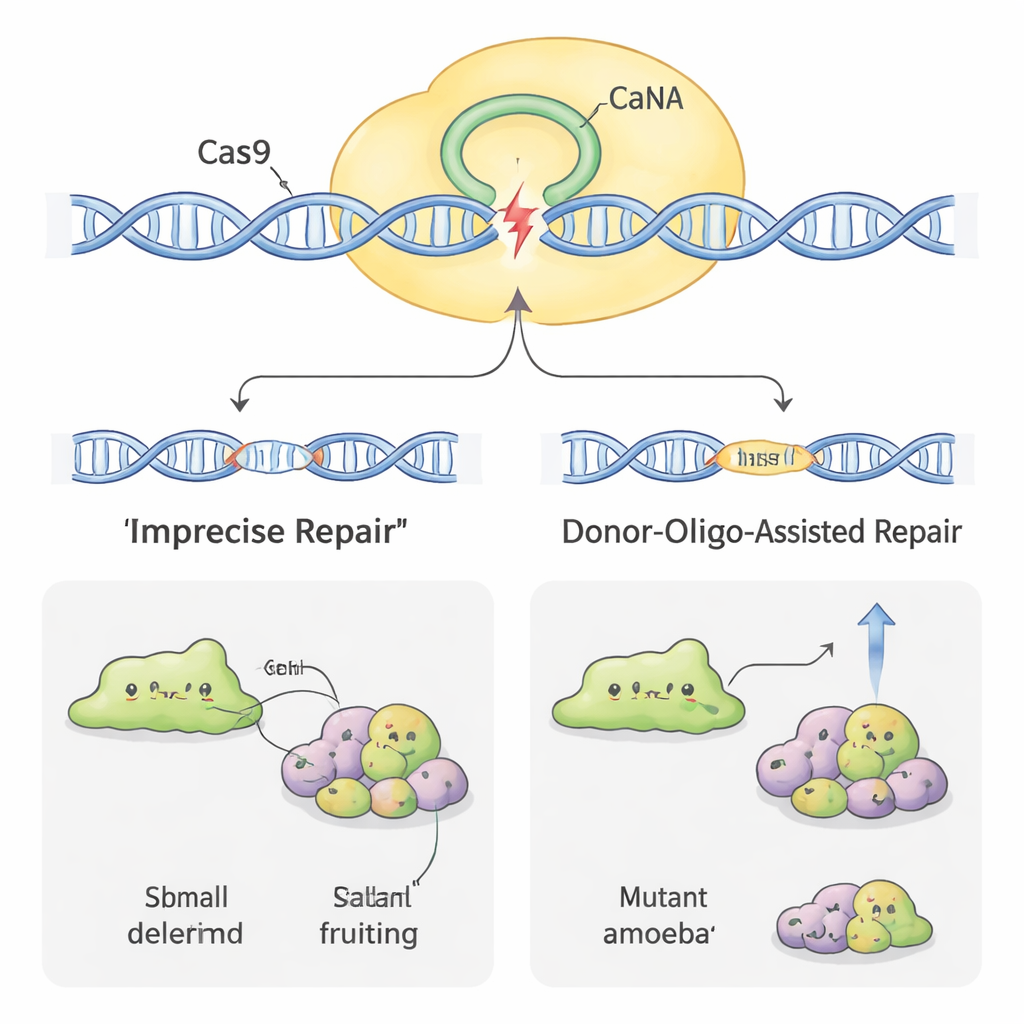
Rendre l’édition plus efficace
Toutes les amibes ne se sont pas laissées modifier par l’édition du génome avec la même facilité. Dans certaines espèces, comme H. pallidum, le taux de réussite initial était très bas. Pour améliorer l’efficacité, les scientifiques ont emprunté une autre astuce : ajouter de courts fragments d’ADN « donneur » en même temps que le plasmide CRISPR. Ces donneurs portent une petite étiquette et un signal d’arrêt entourés de courtes régions correspondant au gène cible. Lorsque la cellule répare la coupure causée par Cas9 en utilisant le donneur comme matrice, elle inactive de manière fiable le gène d’une manière reconnaissable. Chez D. discoideum, cela a augmenté la proportion de clones défectueux et a même permis à l’équipe d’obtenir des mutants sans recourir à une sélection continue par médicament. Chez le plus récalcitrant H. pallidum, la combinaison d’ADN donneur et de quelques jours de traitement médicamenteux a augmenté les taux de mutation d’à peu près un ordre de grandeur, transformant des événements auparavant rares en quelque chose de presque routinier.
Ouvrir une fenêtre sur les origines de la complexité
Pour un non-spécialiste, les détails des designs de plasmides et des matrices de réparation peuvent paraître techniques, mais le bénéfice est vaste : une boîte à outils CRISPR flexible qui fonctionne à travers plusieurs branches de l’arbre des amibes sociales. Grâce à elle, les scientifiques peuvent désormais comparer comment un même gène façonne le développement dans différentes espèces, et comment de subtiles modifications de la régulation génétique ou de la structure protéique contribuent à l’émergence de nouveaux types cellulaires et plans corporels. En d’autres termes, ce travail fournit aux chercheurs les outils génétiques nécessaires pour observer, en détail vivant, comment l’évolution a bricolé des organismes unicellulaires pour construire des sociétés multicellulaires coopératives.
Citation: Oishi, S., Doi, S., Sekida, T. et al. Genome editing across Dictyostelia species enables comparative functional genetics of social amoebas. Sci Rep 16, 7457 (2026). https://doi.org/10.1038/s41598-026-38605-5
Mots-clés: amibes sociales, édition du génome CRISPR, évolution de la multicellularité, Dictyostelium, différenciation cellulaire