Clear Sky Science · fr
PLOD2 favorise la prolifération, la migration et l'invasion des cellules du cancer colorectal via la voie de signalisation PI3K-AKT-GSK3β
Pourquoi le voisinage autour d’une tumeur compte
Le cancer colorectal est l’un des cancers les plus fréquents dans le monde, et de nombreuses personnes sont diagnostiquées seulement après que la maladie a déjà progressé. Cette étude regarde au‑delà des seules cellules cancéreuses pour examiner leur « voisinage » de tissus de soutien. Les chercheurs se concentrent sur une enzyme peu connue appelée PLOD2 et montrent comment elle aide les tumeurs colorectales à croître et à se propager en modifiant à la fois l’environnement tissulaire et des signaux de croissance clés à l’intérieur des cellules.
Un constructeur caché dans l’armature de la tumeur
Nos organes sont soutenus par un réseau de protéines appelé matrice extracellulaire, dont le collagène est le principal composant structurel. PLOD2 est une enzyme qui modifie chimiquement le collagène, favorisant la formation de liaisons croisées solides et de fibres rigides. L’équipe a analysé de larges bases de données génétiques et protéiques puis examiné des échantillons de tissus provenant de 75 patients. Ils ont constaté que les niveaux de PLOD2 étaient bien plus élevés dans les tissus de cancer colorectal que dans les tissus normaux adjacents. Un fort taux de PLOD2 était associé à des tumeurs plus avancées, à une propagation aux ganglions lymphatiques et à une invasion le long des nerfs, et les patients dont les tumeurs présentaient davantage de PLOD2 avaient tendance à vivre moins longtemps. Ces résultats désignent PLOD2 comme un marqueur candidat d’une maladie agressive.
Comment PLOD2 rend les cellules cancéreuses plus agressives
Pour aller au‑delà des corrélations observées dans les échantillons de patients, les chercheurs ont modifié génétiquement des lignées cellulaires de cancer colorectal en laboratoire. Dans un type cellulaire, ils ont augmenté la production de PLOD2 ; dans un autre, ils l’ont supprimée. Les cellules surexprimant PLOD2 se multipliaient plus vite, formaient davantage de colonies et refermaient plus rapidement des « plaies » artificielles en culture, montrant une mobilité accrue. Elles migrèrent aussi plus facilement à travers des membranes poreuses et envahirent plus aisément un gel reproduisant une barrière tissulaire que les cellules témoins. Lorsque PLOD2 était silencé, tous ces comportements s’affaiblissaient. Ensemble, ces expériences montrent que PLOD2 stimule activement la croissance, la migration et l’invasion des cellules cancéreuses, plutôt que d’être un simple témoin.
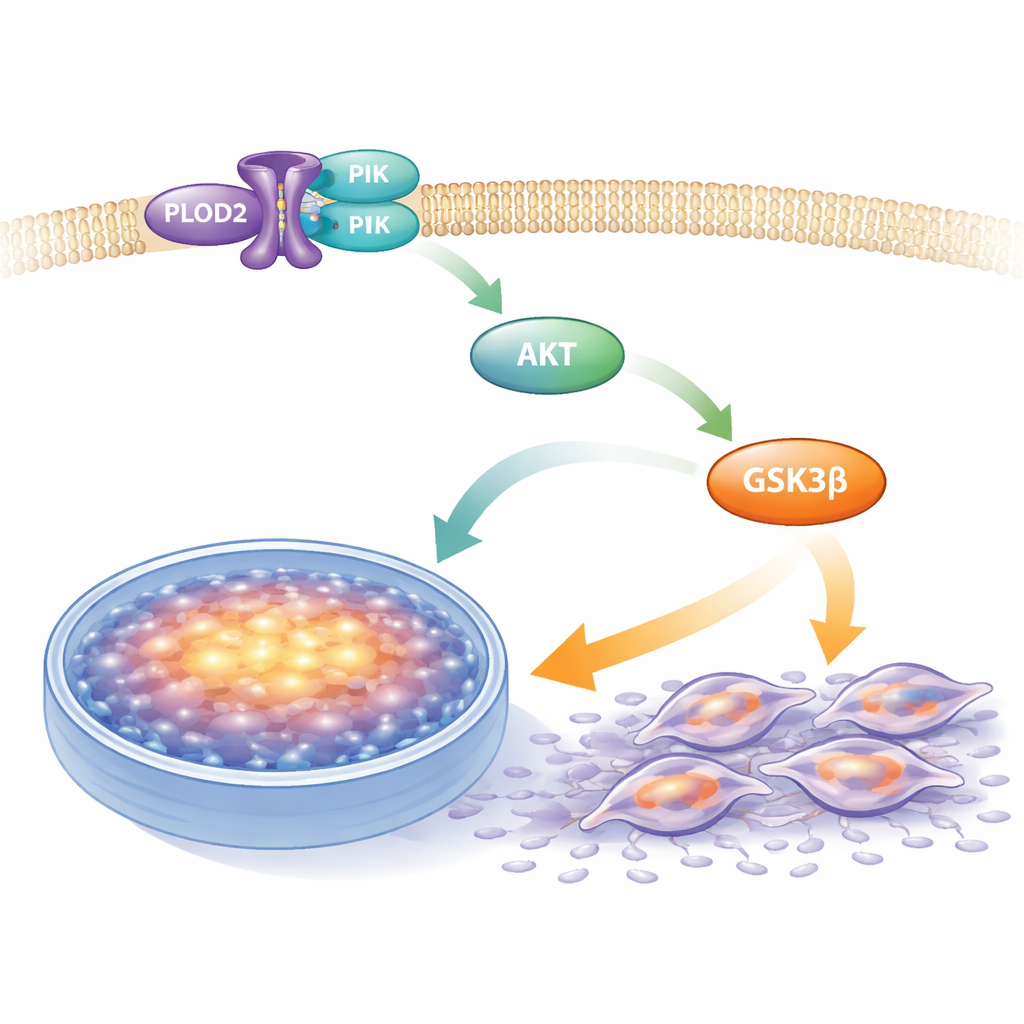
Activation d’une chaîne de signaux favorisant le cancer
À l’intérieur des cellules cancéreuses, de nombreux processus sont contrôlés par des chaînes de signalisation interconnectées. Une chaîne centrale, connue sous le nom de voie PI3K–AKT–GSK3β, aide les cellules à survivre, à se diviser et à adapter leur métabolisme. Grâce à l’exploration de données et à des tests biochimiques, les chercheurs ont découvert que PLOD2 est étroitement lié à cette voie. Ils ont montré que PLOD2 se lie physiquement à PI3K, l’enzyme « démarreur » de la chaîne. Lorsque les niveaux de PLOD2 étaient élevés, les formes activées (phosphorylées) de PI3K, AKT et GSK3β augmentaient, bien que la quantité totale de chaque protéine restât la même. Quand PLOD2 était réduit, l’activation de cette voie diminuait, suggérant que PLOD2 agit comme un interrupteur qui met en marche ce système de croissance et de motilité.
Tester la voie avec des outils chimiques
Pour confirmer que les effets délétères de PLOD2 dépendent de cette chaîne de signalisation, l’équipe a utilisé des médicaments qui bloquent ou stimulent PI3K. Dans les cellules surexprimant PLOD2, un inhibiteur de PI3K a atténué l’activation d’AKT et de GSK3β et ralenti la prolifération, la migration et l’invasion cellulaires. Dans les cellules où PLOD2 avait été silencé, un activateur de PI3K a restauré l’activité de la voie et partiellement récupéré la capacité des cellules à proliférer et à migrer. Bien que la restauration ne fût pas complète — ce qui laisse entendre que PLOD2 peut aussi influencer d’autres voies — ces expériences soutiennent fortement l’idée que PLOD2 favorise la malignité principalement en alimentant l’axe de signalisation PI3K–AKT–GSK3β.
Ce que cela signifie pour les patients
Pour un non‑spécialiste, ces détails moléculaires se résument en une histoire simple : PLOD2 aide les cellules du cancer colorectal à durcir et remodeler leur environnement tout en appuyant sur l’accélérateur de circuits internes de croissance clés. En agissant sur ces deux plans, il rend les tumeurs plus susceptibles de croître agressivement et de se propager. L’étude suggère que la mesure de PLOD2 pourrait aider à identifier les patients à haut risque et que des médicaments ciblant directement PLOD2 — ou la chaîne de signalisation qu’il déclenche — pourraient un jour faire partie de traitements plus personnalisés contre le cancer colorectal. Des travaux supplémentaires chez l’animal et dans des cohortes de patients plus larges seront nécessaires, mais PLOD2 se distingue désormais comme une nouvelle piste prometteuse contre une maladie difficile.
Citation: Fang, H., Zheng, J., Ren, S. et al. PLOD2 promotes proliferation, migration and invasion of colorectal cancer cells via PI3K-AKT-GSK3β signaling pathway. Sci Rep 16, 8118 (2026). https://doi.org/10.1038/s41598-026-38593-6
Mots-clés: cancer colorectal, PLOD2, microenvironnement tumoral, signalisation PI3K AKT, métastase cancéreuse