Clear Sky Science · fr
Les lymphocytes T activés induisent l’apoptose des cellules d’adénocarcinome pulmonaire A549 via une entrée calcique médiée par TRPV4
Pourquoi cette recherche est importante pour le cancer du poumon
Le cancer du poumon reste l’un des cancers les plus meurtriers, en partie parce que les tumeurs apprennent souvent à résister aux traitements standards comme la chimiothérapie et la radiothérapie. Ces dernières années, l’exploitation du système immunitaire de l’organisme a ouvert de nouvelles perspectives. Cette étude explore un angle inédit de cette approche : elle montre comment un type précis de cellule immunitaire, les lymphocytes T activés, peut pousser les cellules cancéreuses pulmonaires vers l’autodestruction en les forçant à absorber du calcium via une « porte » moléculaire appelée TRPV4. Comprendre cette voie pourrait aider les chercheurs à concevoir des immunothérapies plus puissantes et plus ciblées.
Les soldats du système immunitaire face aux cellules tumorales pulmonaires
Les chercheurs se sont concentrés sur des cellules d’adénocarcinome pulmonaire humain connues sous le nom de cellules A549, un modèle largement utilisé du cancer bronchique non à petites cellules. Ils ont mis en présence ces cellules cancéreuses et des cellules Jurkat, représentant les lymphocytes T cytotoxiques, qui cherchent normalement à détruire les cellules infectées ou malignes. En activant chimiquement les cellules Jurkat, l’équipe a simulé l’état d’alerte élevé des lymphocytes T engagés dans une véritable réponse immunitaire. Ils ont ensuite mélangé des lymphocytes T activés ou inactifs avec les cellules cancéreuses à différents ratios et observé l’évolution sur un à trois jours, en surveillant notamment la survie des cellules cancéreuses et la fréquence de la mort cellulaire programmée, l’apoptose.
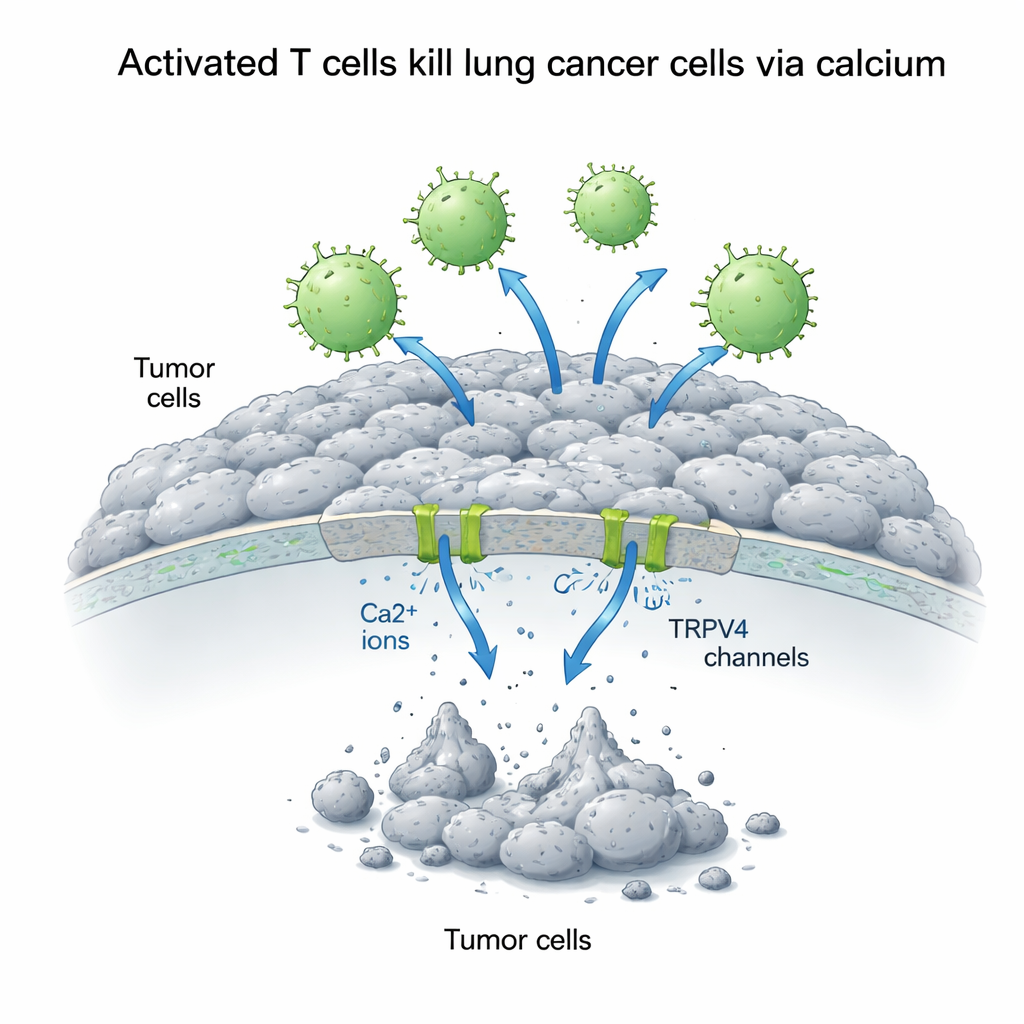
Le calcium, signal à double tranchant pour les cellules cancéreuses
Le calcium intracellulaire agit comme un interrupteur signal polyvalent qui peut soit favoriser la croissance soit déclencher la mort, selon sa gestion. Les scientifiques ont augmenté la concentration de calcium à l’extérieur des cellules A549 et mesuré l’impact sur l’affrontement entre lymphocytes T et cellules tumorales. De façon surprenante, un excès de calcium seul favorisait la croissance des cellules pulmonaires cancéreuses, suggérant que, en conditions calmes, le calcium alimente des voies de survie. Mais en présence de lymphocytes T activés, la situation s’inverse : un calcium externe élevé renforce de manière spectaculaire la capacité de destruction des lymphocytes T. Sur 72 heures, la survie des cellules cancéreuses chutait à moins d’un tiers de la normale lorsque lymphocytes T activés et calcium supplémentaire étaient combinés, alors que les lymphocytes T inactifs avaient peu d’effet et pouvaient même soutenir la croissance en présence de calcium ajouté.
Une « porte » calcique liée au stress et à la mort cellulaire
Pour comprendre comment ce basculement de la croissance vers la mort se produit, l’équipe s’est intéressée à TRPV4, un canal protéique de la membrane cellulaire qui permet l’entrée de calcium. Par analyse protéique, ils ont constaté que les niveaux de TRPV4 augmentaient fortement lorsque les cellules A549 étaient exposées à du calcium ajouté, que des lymphocytes T soient présents ou non, et qu’ils étaient les plus élevés lorsque le calcium et les lymphocytes T activés étaient combinés. Parallèlement, les cellules cancéreuses montraient des signes nets de stress oxydatif : l’équilibre basculait au détriment des antioxydants protecteurs (capacité antioxydante totale plus faible) et en faveur des oxydants nocifs (statut oxydant total plus élevé). La cytométrie en flux, une technique qui marque les cellules avec des colorants fluorescents, a confirmé que les lymphocytes T activés provoquaient une augmentation des stades précoces et tardifs de l’apoptose, surtout lorsque le calcium était abondant. Ensemble, ces observations suggèrent une chaîne d’événements dans laquelle les canaux TRPV4 laissent entrer davantage de calcium, ce qui induit un stress chimique intracellulaire et pousse la cellule vers la mort.
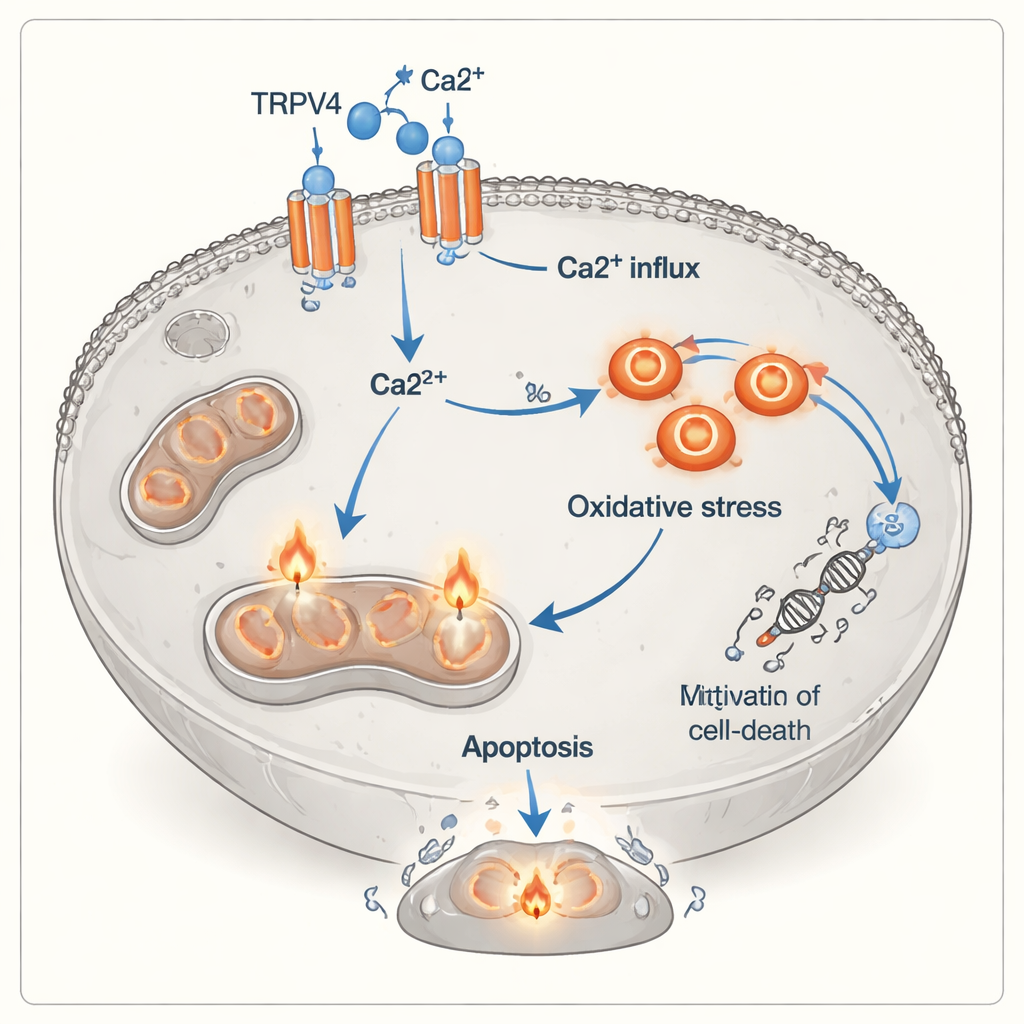
Un nouvel éclairage sur la manière dont les cellules immunitaires tuent les tumeurs
Classiquement, les lymphocytes T cytotoxiques détruisent leurs cibles en libérant des protéines toxiques ou en déclenchant les récepteurs de mort à la surface des cellules cancéreuses. Cette étude suggère une voie supplémentaire, plus indirecte : les signaux émis par les lymphocytes T activés — y compris des molécules inflammatoires et le contact étroit cellule à cellule — semblent rendre les cellules cancéreuses pulmonaires plus dépendantes de TRPV4 et plus vulnérables à une surcharge calcique et aux dommages oxydatifs. Dans cette optique, TRPV4 agit comme un interrupteur de sensibilisation qui transforme un calcium normalement promoteur de croissance en un signal létal. Bien que les expériences aient été réalisées in vitro et sur une seule lignée cellulaire cancéreuse, elles mettent en lumière un lien potentiellement important entre l’attaque immunitaire, les canaux ioniques et les mécanismes de stress intracellulaire des cellules tumorales.
Ce que cela pourrait signifier pour les traitements futurs
Pour les non-spécialistes, l’idée principale est que le succès de l’immunothérapie pourrait dépendre non seulement du renforcement des lymphocytes T, mais aussi du fait de rendre les cellules cancéreuses plus faciles à éliminer. En ciblant TRPV4 ou des canaux calciques apparentés, les cliniciens pourraient un jour renforcer la capacité des lymphocytes T à éliminer les tumeurs pulmonaires ou ajuster les traitements pour éviter d’endommager les tissus sains. Les travaux en sont encore à un stade précoce, et les auteurs soulignent la nécessité d’expériences complémentaires chez l’animal et dans des modèles plus complexes. Néanmoins, la découverte d’un axe TRPV4–calcium–stress oxydatif ajoute une cible prometteuse à l’arsenal pour améliorer les thérapies immunitaires contre le cancer du poumon.
Citation: Alavi, F., Kazemi-Lomedasht, F., Eftekhari, Z. et al. Activated T cells induce apoptosis in A549 lung adenocarcinoma cells via TRPV4-mediated calcium influx. Sci Rep 16, 7155 (2026). https://doi.org/10.1038/s41598-026-38589-2
Mots-clés: immunothérapie du cancer du poumon, lymphocytes T, signalisation calcique, canal TRPV4, stress oxydatif