Clear Sky Science · fr
Des microparticules de silicium mésoporeux renforcent l’immunité antivirale et la mémoire contre le SARS‑CoV‑2
Pourquoi de minuscules particules de silicium comptent pour les vaccins futurs
À mesure que le monde va au‑delà de la première vague de vaccins contre la COVID‑19, les chercheurs cherchent des moyens d’allonger la durée de protection et d’améliorer l’efficacité contre les formes sévères. Cette étude explore un allié inattendu : des particules microscopiques en silicium, en forme d’éponge, qui peuvent être mélangées à des protéines du coronavirus. Ces particules servent de stimulant pour le système immunitaire, visant à créer des défenses plus fortes et de plus longue durée que de nombreux adjuvants actuels, tout en restant sûres et faciles à produire.
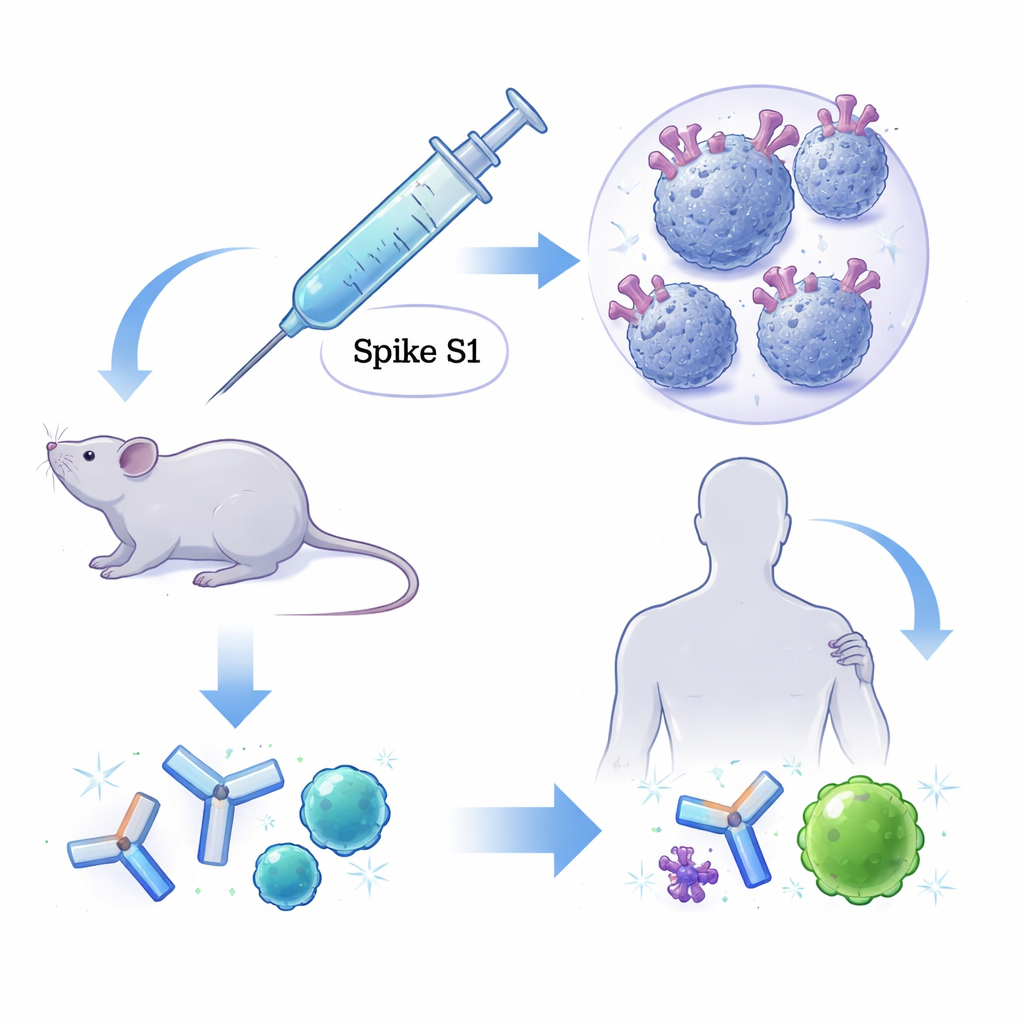
Concevoir un meilleur adjuvant vaccinal
La plupart des vaccins modernes n’utilisent pas des virus entiers ; ils reposent plutôt sur des fragments purifiés, comme la protéine de pointe (spike) du SARS‑CoV‑2. Pris seuls, ces fragments peuvent être trop faibles pour susciter une défense durable, ils sont donc combinés à des adjuvants qui alertent et éduquent le système immunitaire. Les sels d’aluminium remplissent ce rôle depuis près d’un siècle, mais ils tendent à favoriser une seule branche de la réponse et ne sont pas idéaux pour induire une mémoire antivirale robuste. L’équipe à l’origine de ce travail a développé des « microparticules de silicium mésoporeux » — fragments granuleux de silicium remplis de minuscules pores — qui peuvent être chargés de la portion S1 de la protéine spike. Leur taille, leur grande surface et leur comportement à libération lente sont conçus pour en faire des cibles attractives pour les cellules immunitaires qui patrouillent dans l’organisme.
Des anticorps plus forts et plus durables chez la souris
Les chercheurs ont comparé des formulations vaccinales à base de silicium à des formulations standards à base d’aluminium chez la souris. Sur plus de six mois, les deux versions ont produit des niveaux d’anticorps similaires contre la protéine S1 de la spike, dépassant nettement la spike administrée seule. Fait important, après une dose de rappel tardive, la formulation à base de silicium a déclenché une augmentation marquée d’un type d’anticorps associé aux réponses antivirales et cytotoxiques, et ces anticorps bloquaient particulièrement bien l’attachement de la spike au récepteur humain ACE2 — la première étape de l’infection. Si les anticorps de souris neutralisaient efficacement les variants originel, Beta et Delta, ils neutralisaient mal Omicron, ce qui reflète l’éloignement de la spike de ce variant par rapport à la souche originale utilisée pour l’immunisation.
Mobiliser les défenseurs cellulaires de l’organisme
Les anticorps ne racontent qu’une partie de l’histoire ; la protection à long terme contre les virus dépend aussi des cellules T capables de reconnaître et détruire les cellules infectées. Lorsque les scientifiques ont examiné les cellules immunitaires des souris vaccinées, ils ont constaté que celles ayant reçu la formulation à base de silicium produisaient davantage de l’interféron‑gamma, un messager antiviral, en particulier de la part des cellules T associées à la mise à mort directe des cellules infectées. Cela indiquait une forte réponse cellulaire qui a perduré au moins sept mois et était plus prononcée qu’avec l’aluminium. Dans un test strict réalisé chez des souris génétiquement modifiées hautement sensibles au SARS‑CoV‑2, tant les vaccins à base de silicium que d’aluminium ont protégé la plupart des animaux d’un défi létal, réduisant fortement les niveaux de virus dans les poumons et le cerveau par rapport aux témoins non vaccinés.
Indices obtenus sur des cellules immunitaires humaines
Pour savoir si ces particules pouvaient aussi bénéficier à l’immunité humaine, l’équipe a prélevé des cellules sanguines de volontaires ayant été infectés ou vaccinés contre le SARS‑CoV‑2. En laboratoire, ils ont exposé ces cellules à des fragments dérivés de la spike, soit libres, soit attachés aux particules de silicium. Lorsque les fragments viraux étaient portés par le silicium, davantage de cellules T de donneurs vaccinés se sont mises à produire de l’interféron‑gamma, en particulier lorsqu’elles étaient soutenues par des cellules dendritiques — les sentinelles professionnelles du système immunitaire. Ces résultats suggèrent que les particules peuvent aider à raviver la mémoire immunitaire existante et pourraient convenir pour potentialiser les réponses chez des personnes ayant déjà rencontré le virus ou un vaccin antérieur.
Ce que cela pourrait signifier pour les vaccins à venir
Dans l’ensemble, les données chez la souris et sur cellules humaines dépeignent les microparticules de silicium mésoporeux comme des adjuvants prometteurs de nouvelle génération. Elles égalent les sels d’aluminium en production globale d’anticorps, les surpassent après un rappel différé pour générer des types d’anticorps antiviraux puissants, et soutiennent mieux des réponses à médiation par les cellules T durables — tout en étant fabriquées à partir d’un matériau biodégradable, peu toxique et produit à grande échelle. Pour un non‑spécialiste, la conclusion est que des miettes de silicium soigneusement conçues pourraient aider les vaccins futurs non seulement à dresser des boucliers plus élevés contre des virus comme le SARS‑CoV‑2, mais aussi à enseigner au système immunitaire à se souvenir de ces menaces de façon plus profonde et plus durable.
Citation: López-Gómez, A., Real-Arévalo, I., Mayol-Hornero, E. et al. Mesoporous silicon microparticles enhance antiviral immunity and memory responses against SARS-CoV-2. Sci Rep 16, 7355 (2026). https://doi.org/10.1038/s41598-026-38583-8
Mots-clés: Vaccins COVID-19, adjuvants vaccinaux, microparticules de silicium, immunité antivirale, mémoire immunitaire