Clear Sky Science · fr
Analyse fractale de la vascularisation du carcinome hépatocellulaire montre des différences régionales indépendantes de l’invasion vasculaire
Observer le cancer à travers ses vaisseaux sanguins
Les médecins savent que les cancers construisent leur propre réseau chaotique de vaisseaux sanguins, et que l’organisation de ce réseau peut influencer l’efficacité des traitements. Dans le cancer du foie, les médicaments qui ciblent l’apport sanguin font déjà partie des soins standard, mais les mesures de laboratoire actuelles comptent surtout le nombre de vaisseaux et non leur agencement. Cette étude pose une question simple mais puissante : peut-on capturer le « motif » des vaisseaux tumoraux par quelques nombres seulement, et ces motifs diffèrent-ils entre la tumeur, les tissus avoisinants et le reste du foie ?
Des motifs cachés dans les réseaux ramifiés
Les chercheurs se sont concentrés sur le carcinome hépatocellulaire, le cancer primaire du foie le plus fréquent. Ils ont examiné des prélèvements de 29 patients dont les coupes hépatiques avaient été colorées de sorte que l’endothélium des vaisseaux apparaisse brun au microscope. Plutôt que de se limiter au comptage des vaisseaux, ils ont analysé la manière dont les vaisseaux remplissent collectivement l’espace, en utilisant des outils mathématiques souvent appliqués à des formes naturelles complexes comme les côtes ou les branches d’arbre. Deux mesures clés ont été utilisées : l’une décrivant la « complexité » du réseau de vaisseaux, l’autre décrivant la répartition des espaces vides entre les vaisseaux. Ensemble, ces chiffres condensent la complexité visuelle du réseau vasculaire en une forme comparable entre différentes régions du foie.
Transformer des images microscopiques en cartes mesurables
Pour cela, l’équipe a d’abord dû séparer de manière fiable les vaisseaux du tissu de fond sur de grandes lames numériques. Ils ont construit une chaîne automatique de traitement d’image qui identifiait les vaisseaux colorés en brun, éliminait le bruit et comblait les intérieurs vasculaires, produisant des cartes binaires nettes des réseaux de vaisseaux. Ces segmentations automatiques ont été vérifiées par un pathologiste hépatique et se sont révélées en bon accord, notamment pour les mesures globales d’organisation vasculaire. Les lames ont ensuite été découpées en nombreuses tuiles plus petites, chacune assignée à l’une des trois régions : tumeur, tissu immédiatement entourant la tumeur (péri-tumoral) ou foie non tumoral distant. Les tuiles contenant du tissu nécrotique ou des artefacts majeurs ont été soigneusement exclues, car ils peuvent imiter des motifs vasculaires denses et irréalistes.
Comment les régions tumorales diffèrent du reste
Sur des milliers de tuiles, l’étude a révélé des différences claires et statistiquement fortes dans les motifs vasculaires entre les trois régions du foie. Le tissu hépatique non tumoral présentait la plus grande complexité, se comportant presque comme une toile remplissant l’espace à des échelles plus larges. Le tissu péri-tumoral se situait au milieu, tandis que les régions tumorales montraient systématiquement une complexité plus faible. Une mesure connexe de la disposition des espaces vides entre les vaisseaux augmentait également du non tumoral au péri-tumoral puis à la tumeur, indiquant que les vaisseaux associés à la tumeur sont plus regroupés et plus spatialement corrélés. Fait important, le fait que la tumeur ait commencé ou non à envahir les vaisseaux voisins — un signe clinique d’alerte majeur — n’altérait pas de façon mesurable ces motifs globaux. L’architecture du réseau vasculaire était principalement modelée par la présence même de la tumeur, et non par cette étape d’invasion.
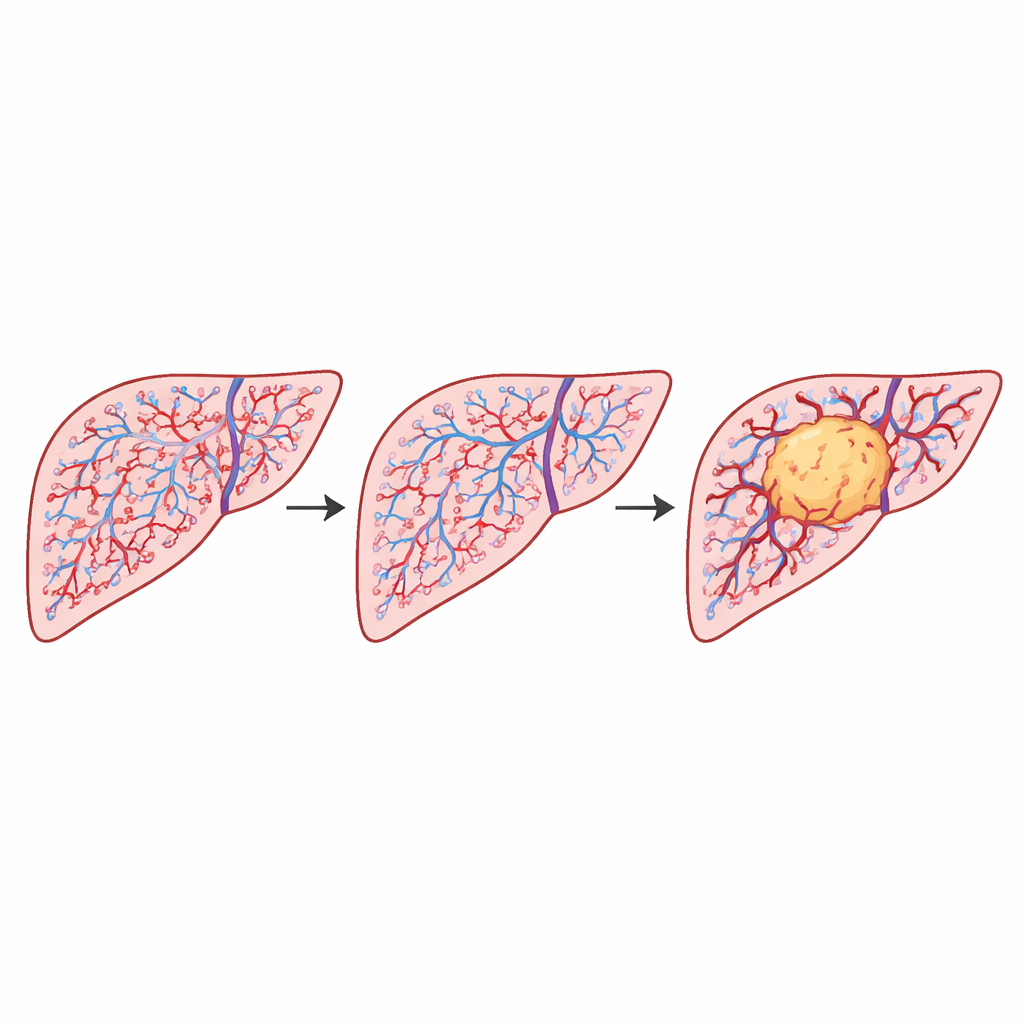
Pourquoi la forme et la taille des vaisseaux comptent
Pour comprendre ce qui sous-tendait ces différences numériques, les auteurs ont examiné de plus près les formes et tailles des vaisseaux individuels. Dans le foie sain, on observait une accumulation marquée de nombreux petits vaisseaux ronds, avec quelques gros vaisseaux. Dans les régions tumorales, la surface vasculaire totale était similaire, mais les vaisseaux étaient répartis plus uniformément entre les tailles et étaient plus souvent allongés ou irréguliers. Des modèles simples ont montré qu’un réseau riche en nombreux petits vaisseaux ronds nécessite l’utilisation de davantage de petites boîtes lors du « recouvrement » du motif, ce qui augmente sa mesure de complexité. En revanche, un réseau avec moins de petits vaisseaux et des tailles plus uniformes paraît moins intricate, même s’il contient à peu près la même surface vasculaire totale. Ce changement géométrique correspond à la baisse observée de la complexité au sein des tumeurs et explique comment de subtiles modifications de la distribution des formes de vaisseaux peuvent remodeler le motif vasculaire global.
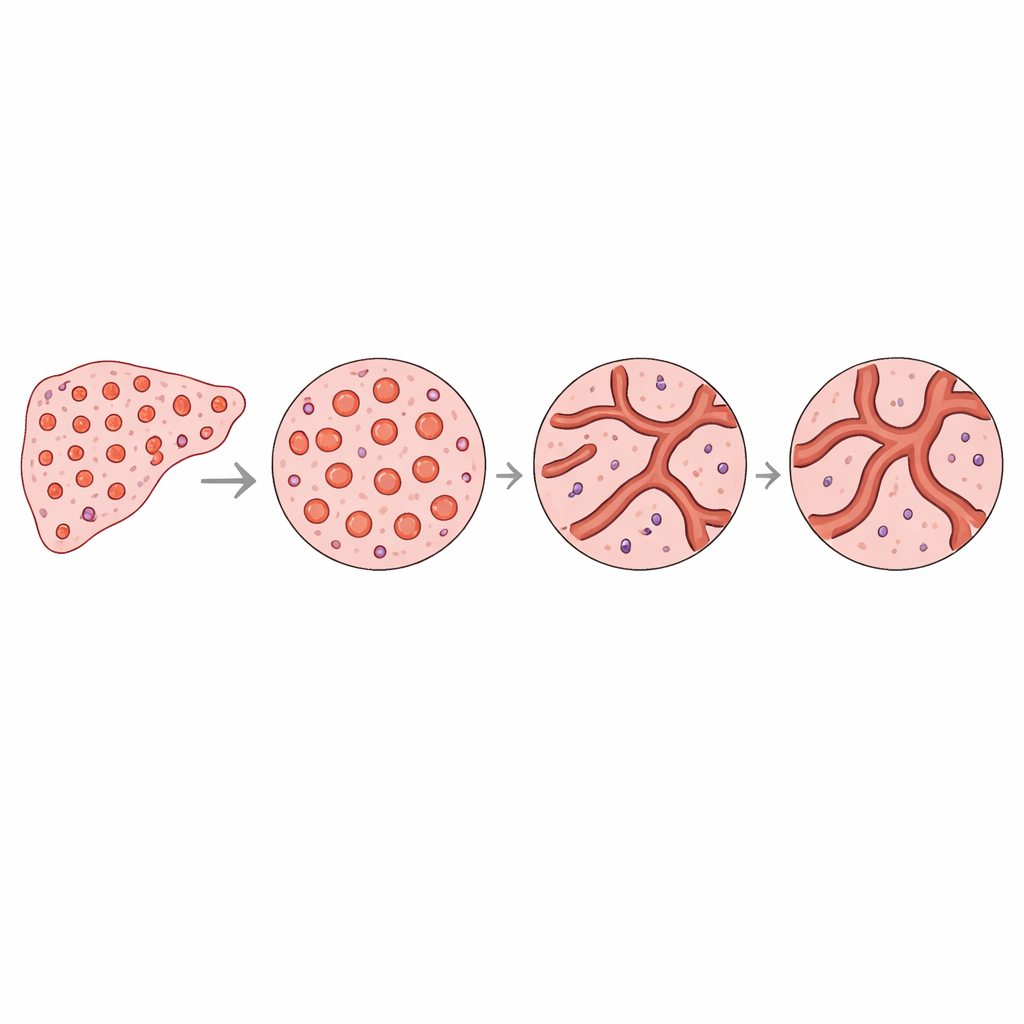
Ce que cela pourrait signifier pour les examens futurs
Pour les non-spécialistes, la conclusion principale est que les tumeurs hépatiques ne se contentent pas de produire davantage de vaisseaux ; elles les réorganisent d’une manière distincte et mesurable qui s’étend au tissu environnant. Ces différences peuvent être capturées par des descripteurs mathématiques compacts qui résument la disposition des vaisseaux et des espaces entre eux. Les travaux suggèrent que, à l’avenir, des méthodes d’imagerie avancées pourraient estimer ces descripteurs sans biopsie, fournissant de nouveaux biomarqueurs non invasifs de l’étendue de l’influence tumorale et de l’organisation de son approvisionnement sanguin. En même temps, l’étude montre que l’invasion microscopique des vaisseaux voisins ne laisse pas nécessairement d’empreinte reconnaissable sur le motif vasculaire à grande échelle, soulignant que tous les comportements tumoraux dangereux ne sont pas visibles à travers l’architecture vasculaire seule.
Citation: Penney, J., Nardon, V., Beaufrere, A. et al. Fractal analysis of hepatocellular carcinoma vasculature shows regional differences independent of vascular invasion. Sci Rep 16, 11049 (2026). https://doi.org/10.1038/s41598-026-38580-x
Mots-clés: vascularisation du cancer du foie, architecture fractale des vaisseaux, carcinome hépatocellulaire, microenvironnement tumoral, biomarqueurs d’imagerie non invasifs