Clear Sky Science · fr
Optimisation d'agents se liant à la galectine‑3 par synthèse multiple in situ et spectrométrie de masse native
Pourquoi cela importe pour les médicaments de demain
De nombreux médicaments modernes agissent en se fixant sur des protéines de notre organisme, mais trouver une petite molécule qui se lie fortement et de façon sélective au bon site est long, coûteux et souvent frustrant. Cette étude présente une méthode plus rapide pour affiner ces molécules directement en présence de la protéine cible, puis identifier les meilleures à l'aide d'une technique de pesée très sensible. Les auteurs illustrent leur approche sur la galectine‑3, une protéine impliquée dans la progression du cancer, et aboutissent à un candidat prometteur de type médicament qui se lie aussi fortement que certains des meilleurs composés existants, mais dans une poche inattendue à la surface de la protéine.

Repenser la recherche de meilleurs candidats‑médicaments
L'optimisation traditionnelle des médicaments ressemble à un jeu de devinettes coûteux. Les chimistes modifient un composé de départ pas à pas, testent chaque version et espèrent améliorer l'affinité pour la protéine cible. Mais les surfaces protéiques sont flexibles, l'eau interfère et l'événement de liaison peut lui‑même remodeler la protéine, rendant les prédictions informatiques peu fiables. Même lorsqu'une structure haute résolution est disponible, rien ne garantit qu'une modification proposée sera bénéfique. Les méthodes « guidées par la cible » existantes cherchent à laisser la protéine choisir ses partenaires parmi un ensemble de blocs de construction, mais ces approches reposent encore sur des analyses complexes et des signaux indirects pour déduire quel composé se lie réellement le mieux.
Laisser la protéine choisir, puis peser les gagnants
Les chercheurs ont combiné deux idées en un flux de travail simplifié. D'abord, ils ont utilisé une réaction chimique réversible qui relie un noyau commun à base de sucre à de nombreuses pièces latérales différentes dans un seul tube, formant un mélange de molécules apparentées. En ajustant soigneusement les ratios de départ, les produits résultants atteignent un état d'équilibre gouverné par des règles de concentration simples, ce qui aide à égaliser leurs abondances malgré des réactivités brutes différentes. Ensuite, ils ont exposé ce mélange à la galectine‑3 et l'ont analysé par spectrométrie de masse native, une forme de spectrométrie de masse qui préserve les paires protéine–molécule intactes dans une solution douce, proche de l'eau. Comme chaque candidat a une masse distincte, l'instrument peut détecter directement quelles molécules sont effectivement liées à la protéine, sans étiquettes ni témoins.
Des mélanges encombrés à un ligand remarquable
Avec ce dispositif, l'équipe a créé des dizaines de ligands de la galectine‑3 en attachant divers groupes latéraux à un noyau sucre inspiré d'un inhibiteur connu, GB1107. Ils ont réparti 35 hydrazides différents en groupes gérables, formé toutes les combinaisons in situ, puis ajouté la galectine‑3. La spectrométrie de masse native a mis en évidence les composés qui voyageaient le plus souvent avec la protéine, les signalant comme principaux candidats. Un test de stabilité thermique de suivi, qui mesure comment un composé stabilise la protéine lors du chauffage, a filtré les faux positifs causés par des artefacts de la mesure en phase gazeuse. Trois candidats de tête sont restés, et des mesures détaillées de liaison basées sur la chaleur ont montré que l'un d'eux, appelé GalAldBZ20, se liait particulièrement fortement à la galectine‑3, dans la plage sous‑micromolaire.
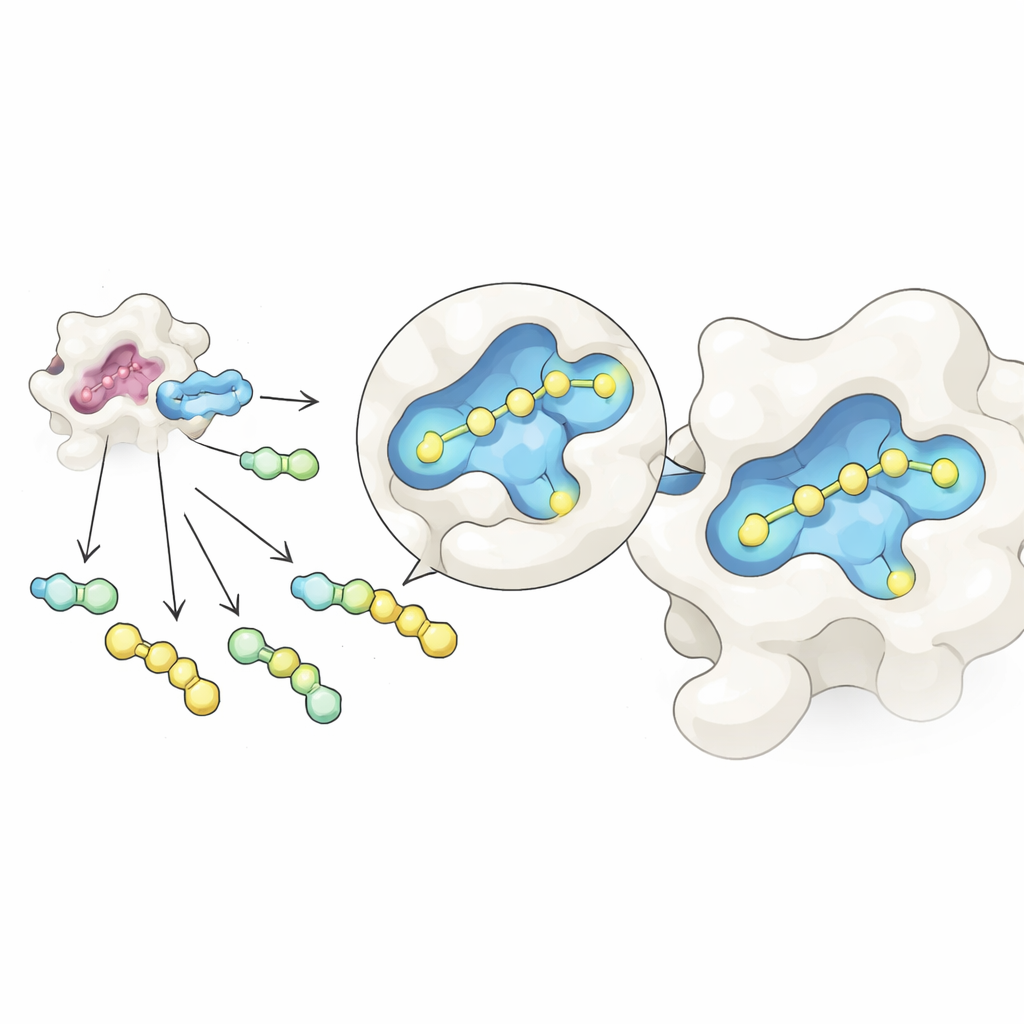
Découverte d'une poche cachée et renforcement de la liaison
La surprise suivante est survenue lorsque l'équipe a examiné comment GalAldBZ20 se positionnait à la surface de la galectine‑3. La plupart des ligands connus utilisent une poche « alpha » proche du site de liaison du sucre, mais les méthodes structurales et les simulations informatiques ont indiqué que GalAldBZ20 préférait plutôt une poche voisine « bêta ». La cristallographie aux rayons X l'a suggéré, la résonance magnétique nucléaire en solution a révélé plusieurs conformations locales près de cette poche, et des simulations de dynamique moléculaire ont soutenu un modèle où un anneau porteur d'un groupe nitro sur la molécule s'insère dans le site bêta. En raisonnant qu'ils pouvaient verrouiller cet arrangement de manière plus ferme, les chimistes ont redesigné le lien chimique entre le sucre et l'anneau nitro pour favoriser de nouveaux contacts polaires avec la protéine et réduire la flexibilité.
Transformer un criblage ingénieux en un candidat puissant
Fort de cette compréhension, l'équipe a synthétisé un petit ensemble de molécules de suivi plus rigides qui conservaient le même sucre et l'anneau nitro mais changeaient le connecteur entre eux. Une version, une N‑galactoside (composé 5), s'est distinguée : elle se liait à la galectine‑3 environ dix fois plus fortement que le coup de départ, atteignant une affinité comparable à GB1107, tout en préférant toujours la poche bêta. Une structure cristalline à ultra‑haute résolution a montré une densité nette pour l'anneau nitro niché dans cette poche, soutenu par plusieurs liaisons hydrogène et un contact cation‑π avec des acides aminés clés. Lorsque le groupe nitro a été retiré ou remplacé par un simple groupe méthyle, la liaison s'est fortement affaiblie, soulignant son importance. Parce que la galectine‑1, une protéine apparentée, manque de cette poche bêta, le nouveau composé pourrait finalement offrir une meilleure sélectivité, une caractéristique très recherchée en conception de médicaments.
Ce que cela signifie pour la découverte de médicaments
En termes accessibles, ce travail montre qu'il est possible de mélanger de nombreuses molécules apparentées, de laisser une protéine liée à la maladie « choisir » ses favorites, puis de peser directement ces paires protéine–molécule pour voir quelles sont les plus adhérentes. Appliquée à la galectine‑3, cette stratégie a trouvé de manière inattendue puis renforcé la liaison à une poche peu explorée, produisant un composé qui rivalise avec certains des meilleurs inhibiteurs existants et pourrait servir de base à de nouveaux médicaments anticancéreux. Plus largement, l'association de la chimie in situ et de la spectrométrie de masse native offre un raccourci général pour affiner des candidats‑médicaments contre des protéines présentant plusieurs sites de liaison possibles, ce qui peut faire gagner du temps, des matières et des efforts aux premières étapes de la découverte de médicaments.
Citation: Hoshi, K., Konuma, T., Taguchi, R. et al. Optimization of galectin-3 binding agents by in situ multiple compound synthesis and native mass spectrometry. Sci Rep 16, 8453 (2026). https://doi.org/10.1038/s41598-026-38570-z
Mots-clés: inhibiteurs de la galectine‑3, spectrométrie de masse native, découverte de médicaments basée sur des fragments, synthèse guidée par la cible, candidats médicaments anticancéreux