Clear Sky Science · fr
Comparaison et combinaison de xevinapant avec l’inhibition d’ATR et de PARP pour la radiosensibilisation de cellules de CHNC HPV-négatives
Pourquoi renforcer la radiothérapie est important
La radiothérapie est un traitement central des cancers de la bouche et de la gorge, mais de nombreuses tumeurs y résistent, obligeant les médecins à utiliser des doses élevées qui peuvent endommager les tissus normaux. Cette étude pose une question pratique aux implications majeures pour les patients : parmi plusieurs médicaments anticancéreux modernes conçus pour rendre les cellules tumorales plus vulnérables, lesquels fonctionnent réellement le mieux avec la radiothérapie contre des cancers difficiles de la tête et du cou HPV‑négatifs cultivés en laboratoire ?
Traitement actuel et ses limites
Les patients atteints de carcinome épidermoïde localement avancé de la tête et du cou sont souvent traités par une combinaison de radiothérapie et du chimiothérapeutique cisplatine, ou par chirurgie suivie de radiothérapie. Si cette approche peut contrôler le cancer, elle laisse fréquemment des effets indésirables graves et durables tels que des difficultés à avaler, la sécheresse buccale, des problèmes d’audition et des lésions rénales. De nombreux patients âgés ou fragiles ne tolèrent pas du tout le cisplatine. Cela a suscité un vif intérêt pour les « radiosensibilisateurs » — des médicaments qui rendent les cellules tumorales plus faciles à tuer par la radiothérapie afin que le traitement soit plus efficace ou, potentiellement, plus doux.
Un médicament prometteur qui a déçu
L’un de ces médicaments, le xevinapant, a d’abord été salué comme une percée. Il mime une protéine naturelle appelée SMAC et bloque des molécules qui aident les cellules cancéreuses à éviter la mort cellulaire programmée. Dans des travaux antérieurs, l’ajout de xevinapant à la chimioradiothérapie standard a amélioré les résultats dans un essai clinique de phase 2 pour les cancers de la tête et du cou, suscitant l’espoir qu’il puisse devenir un nouveau standard de soins. Mais un essai beaucoup plus vaste de phase 3, appelé TrilynX, a été arrêté prématurément lorsque des données intermédiaires ont montré non seulement une absence de bénéfice, mais même une survie inférieure et plus d’effets secondaires dans le groupe xevinapant. Cet échec inattendu a créé un besoin urgent de réévaluer dans quelle mesure le xevinapant aide réellement la radiothérapie, et de le comparer à d’autres stratégies plus récentes.
Comparer trois stratégies tête‑à‑tête
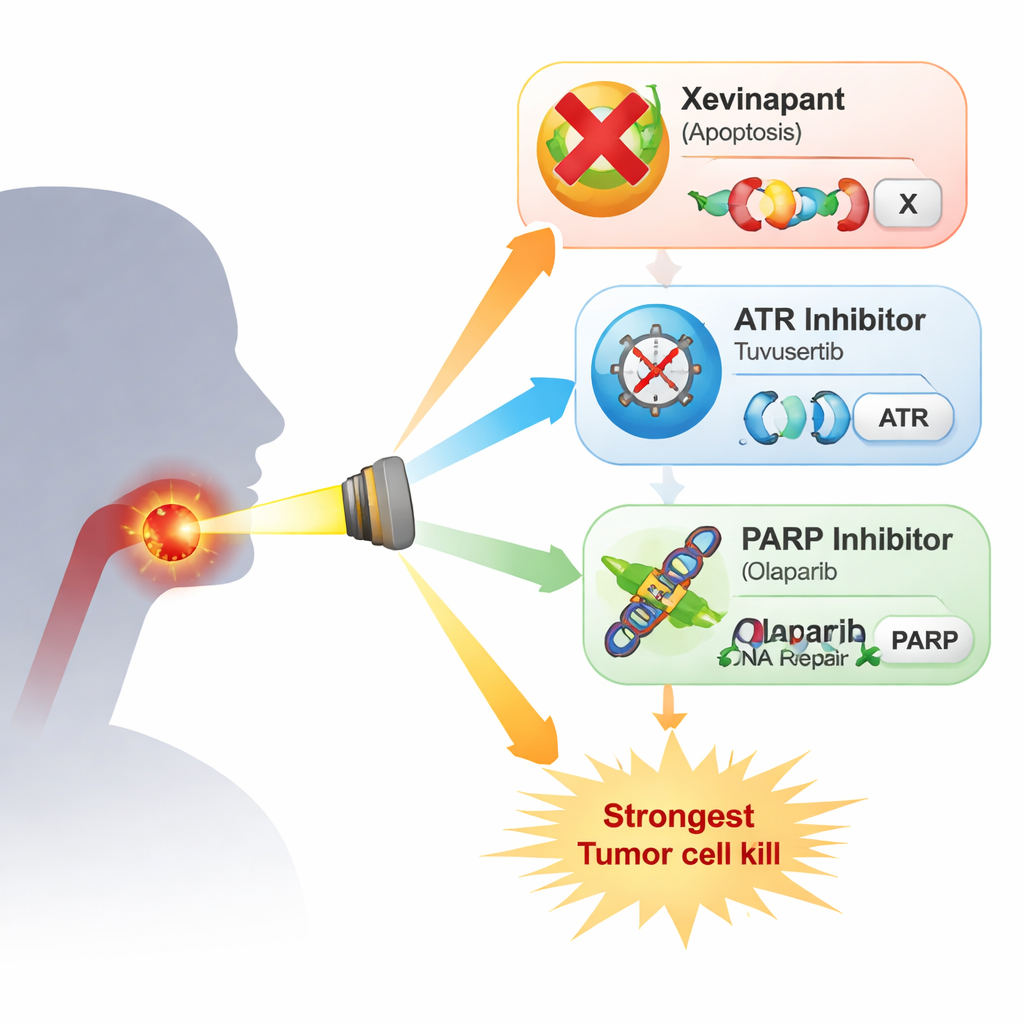
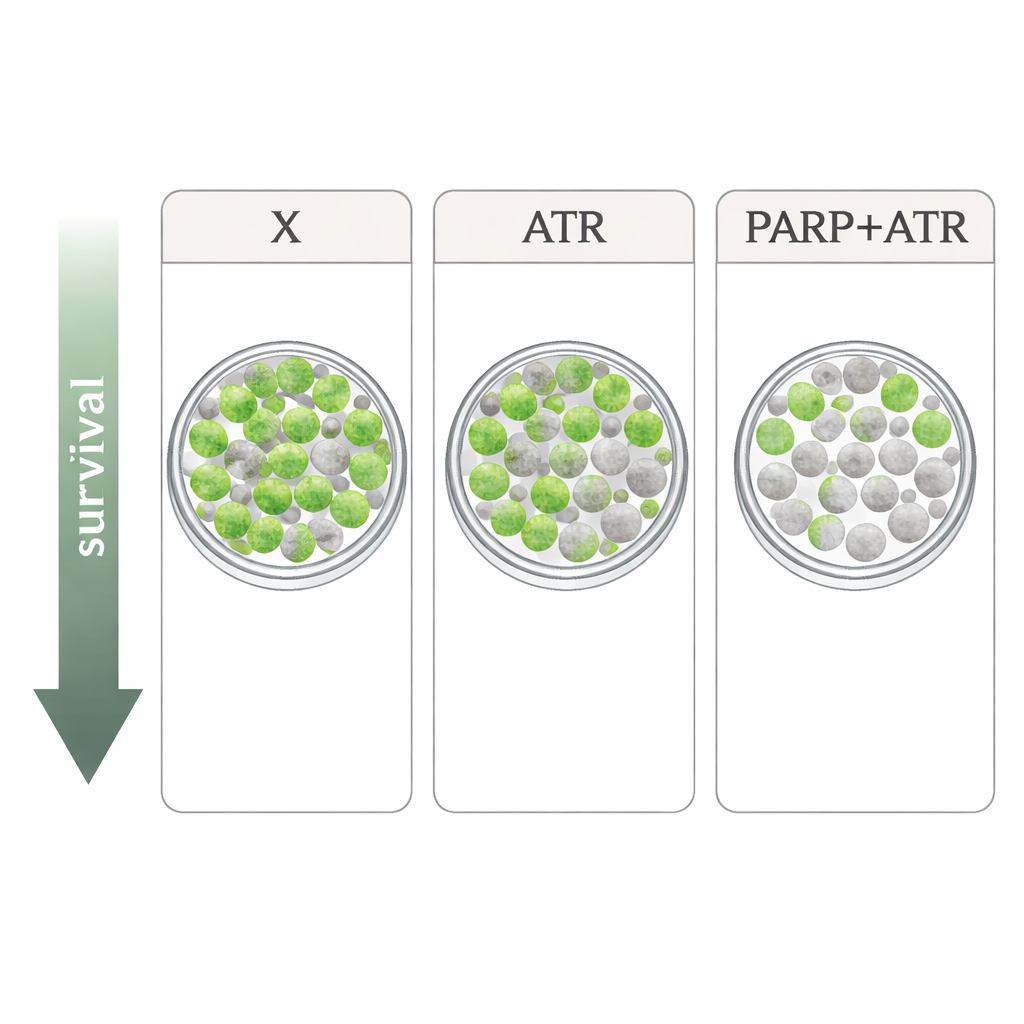
Les chercheurs ont étudié quatre lignées cellulaires de cancers de la tête et du cou HPV‑négatives et résistantes à la radiothérapie. Ils ont comparé le xevinapant à deux médicaments ciblant la réponse aux dommages de l’ADN : l’inhibiteur d’ATR tuvusertib et l’inhibiteur de PARP olaparib, tous deux utilisés à des doses proches de celles réalisables chez l’homme. ATR et PARP sont des acteurs clés qui aident les cellules à arrêter le cycle cellulaire et à réparer l’ADN après des dommages tels que ceux causés par les rayons X. Dans des tests simples de prolifération, chaque médicament seul ralentissait la croissance cellulaire de façon modeste seulement, avec des profils différents selon les lignées. Lorsqu’ils ont été combinés avec la radiothérapie dans l’essai le plus exigeant — le comptage du nombre de cellules uniques capables de repousser en colonies — le tableau s’est clarifié : le xevinapant n’a donné qu’un effet supplémentaire léger ou nul dans plusieurs lignées, alors que tuvusertib et olaparib rendaient systématiquement la radiothérapie plus létale. L’impact le plus fort provenait de la combinaison d’inhibition d’ATR et de PARP, qui a provoqué des baisses particulièrement prononcées de la survie en colonies dans trois des quatre lignées.
Les signaux de mort cellulaire ne racontent pas toute l’histoire
Parce que le xevinapant est conçu pour déclencher la mort cellulaire, l’équipe a également mesuré combien de cellules devenaient apoptotiques ou lysées après le traitement, avec et sans radiothérapie. Ces marqueurs de mort ont augmenté de façon notable dans certains contextes — en particulier dans une lignée appelée HSC4 et lorsque les médicaments étaient combinés — mais n’étaient pas des indicateurs fiables de l’efficacité réelle de la radiothérapie sur la survie à long terme. Autrement dit, les lectures de mort à court terme prédisaient mal la véritable radiosensibilisation. Ce décalage souligne une leçon clé pour le développement de médicaments : seuls des tests qui suivent les cellules suffisamment longtemps pour voir si elles peuvent repousser — comme les essais de formation de colonies — peuvent juger correctement si un radiosensibilisateur est efficace.
Ce que cela signifie pour les traitements futurs
À partir de ces expériences en laboratoire, le xevinapant possède une certaine capacité à potentialiser la radiothérapie dans les cellules de cancers de la tête et du cou HPV‑négatives, mais son impact était plus faible et moins cohérent que les approches qui interfèrent directement avec la gestion des dommages à l’ADN via ATR et PARP. L’association d’inhibiteurs d’ATR et de PARP a produit l’effet le plus puissant, suggérant que des combinaisons de ces médicaments, dosées avec soin avec la radiothérapie, pourraient offrir une voie plus prometteuse que la poursuite du xevinapant, du moins pour ce type de cancer. La traduction de ces résultats en clinique ne sera pas simple, car ces médicaments peuvent aussi affecter les tissus normaux à division rapide et ont déjà nécessité des réductions de dose lors d’essais précoces. Néanmoins, ce travail oriente cliniciens et chercheurs vers des stratégies ciblant la réparation de l’ADN comme candidats plus convaincants pour rendre la radiothérapie à la fois plus efficace et, potentiellement, plus sûre pour les patients qui ne peuvent pas recevoir la chimiothérapie standard.
Citation: Roehrle, J., Perugachi-Heinsohn, A., Gatzemeier, F. et al. Comparing and combining xevinapant with ATR and PARP inhibition for the radiosensitization of HPV-negative HNSCC cells. Sci Rep 16, 5882 (2026). https://doi.org/10.1038/s41598-026-38550-3
Mots-clés: cancer de la tête et du cou, radiothérapie, inhibiteurs de la réparation de l’ADN, xevinapant, radiosensibilisation