Clear Sky Science · fr
Les adaptations thermorégulatrices au froid chez les souris C3H/HeJ sont indépendantes du signalement ADRB3
Pourquoi les souris « amatrices de froid » comptent pour la santé humaine
Rester au chaud ne semble pas être un sujet médical de pointe, et pourtant la manière dont l’organisme gère le froid concerne entièrement l’utilisation et la combustion de l’énergie. Cette étude compare deux souches courantes de souris de laboratoire et pose une question étonnamment importante : lorsqu’elles sont exposées au froid, activent-elles leurs « fourneaux » internes de la même façon que les humains ? La réponse aide à expliquer pourquoi certains médicaments anti-obésité efficaces chez la souris ont échoué chez l’humain — et met en lumière un modèle murin plus proche de la physiologie humaine pour étudier le métabolisme.
Deux types de souris, un même défi frigorifique
Les chercheurs ont comparé les souris standard C57BL/6J, pilier de la recherche métabolique, à une souche moins utilisée appelée C3H/HeJ. Les deux groupes ont d’abord été maintenus autour de 30 °C, une température à laquelle les souris dépensent à peine d’énergie pour rester au chaud. Les animaux ont ensuite été refroidis progressivement jusqu’à 10 °C, et leur poids corporel, consommation alimentaire et dépense énergétique ont été mesurés avec précision dans des cages métaboliques de haute technologie. Fait intéressant, les deux souches présentaient quasiment le même « point de confort » pour une dépense énergétique minimale — autour de 29–30 °C — ce qui signifie qu’elles partaient d’une base similaire avant l’exposition au froid.
Quand le froid arrive, une souche fournit plus d’effort
Lorsque la température a baissé, les deux types de souris ont augmenté leur dépense énergétique, comme attendu. Mais les souris C3H ont brûlé plus d’énergie que les C57, bien qu’elles aient consommé des quantités similaires de nourriture. Cette combustion accrue n’était pas seulement une réaction transitoire : elle a persisté pendant les premières heures puis les jours suivant l’exposition au froid. Malgré cela, les C3H étaient plus légères et présentaient moins de tissu adipeux brun global, suggérant que leur graisse existante travaillait plus intensément plutôt que d’augmenter en volume. Des analyses sanguines ont aussi indiqué que les C3H mobilisaient davantage de combustibles, comme le glycérol, pour alimenter cette production de chaleur supplémentaire.
Le tissu adipeux brun et blanc se joignent à la production de chaleur
Pour comprendre ce qui se passait à l’intérieur, l’équipe a examiné le tissu adipeux brun — le tissu classique générateur de chaleur — ainsi que deux types de tissu adipeux blanc. Chez les souris C3H, le froid augmentait fortement l’activité des gènes liés à la production de chaleur dans le tissu brun, et des protéines clés soutenant la combustion de carburant et l’activité mitochondriale étaient plus fortement activées. La microscopie a révélé des modifications structurelles compatibles avec un tissu plus actif. Le tissu adipeux blanc racontait une histoire similaire : en particulier, un dépôt autour des testicules, habituellement lent à se convertir en cellules productrices de chaleur, montrait une activation marquée chez les C3H. Cela suggère que chez ces animaux, non seulement le tissu adipeux brun mais aussi la graisse dite « de stockage » peut être réquisitionnée pour aider à maintenir la température corporelle.
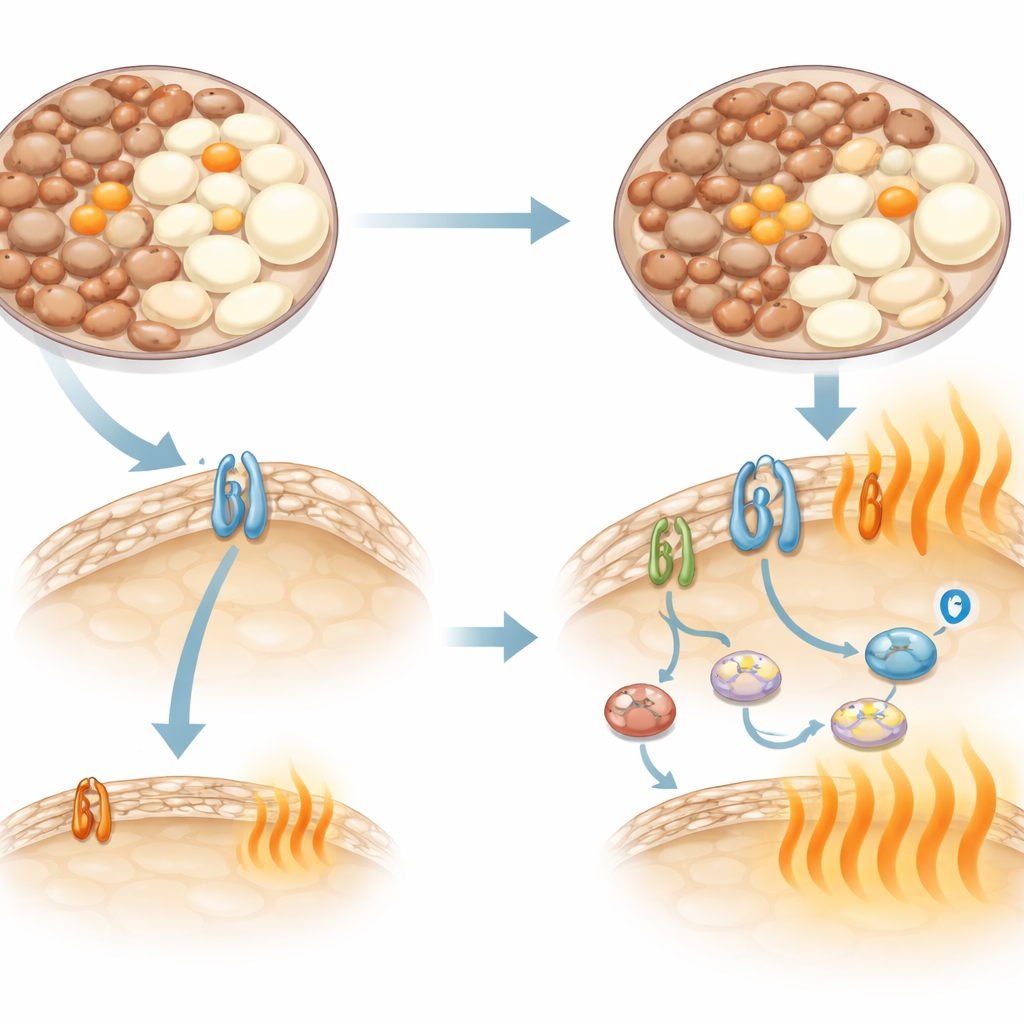
Une connexion nerveuse différente entre nerfs et graisse
La production de chaleur dans la graisse est normalement pilotée par des signaux du système nerveux agissant via les récepteurs bêta-adrénergiques des adipocytes. Chez les souris C57 classiques, un récepteur nommé bêta‑3 joue un rôle majeur, et les médicaments qui le stimulent augmentent fortement la dépense énergétique. Les chercheurs l’ont confirmé : un composé sélectif ciblant le bêta‑3 a provoqué une hausse importante et soutenue de la dépense énergétique chez les C57. Mais chez les C3H, ce même médicament n’a eu qu’un effet faible et bref. L’analyse des gènes explique pourquoi : ces souris exprimaient à peine le récepteur bêta‑3 dans leur tissu adipeux. Pourtant, lorsqu’on a administré de la noradrénaline, un signal naturel qui active plusieurs récepteurs apparentés, les C3H ont tout de même augmenté leur dépense énergétique. Le blocage des récepteurs bêta‑1 et bêta‑2 a largement effacé les différences entre souches, indiquant que les C3H s’appuient sur ces récepteurs alternatifs et sur d’autres voies non classiques de thermogenèse plutôt que sur le bêta‑3.
Ce que cela signifie pour l’étude du métabolisme humain
Les humains, comme les C3H, dépendent principalement des récepteurs bêta‑1 et bêta‑2 dans leur tissu adipeux brun, et non du bêta‑3. Cela peut expliquer pourquoi des médicaments ciblant le bêta‑3 ont fonctionné chez certaines souches de souris mais déçu en essais cliniques. En montrant que les C3H peuvent déclencher une thermogenèse froide puissante avec presque aucune signalisation bêta‑3, cette étude met en avant cette souche comme modèle plus proche de l’humain pour étudier la combustion énergétique par la graisse. Pour le lecteur, la leçon est que toutes les souris ne se valent pas : bien choisir la souche et la température d’hébergement peut rendre la recherche préclinique beaucoup plus pertinente pour la santé humaine réelle et pour le développement futur de thérapies contre l’obésité et les maladies métaboliques.
Citation: Beji, S., Mouchiroud, M., Gélinas, Y. et al. Thermoregulatory adaptations to cold in C3H/HeJ mice are independent of ADRB3 signaling. Sci Rep 16, 7859 (2026). https://doi.org/10.1038/s41598-026-38538-z
Mots-clés: tissu adipeux brun, adaptation au froid, signalisation adrénergique, modèles murins, dépense énergétique