Clear Sky Science · fr
Évaluation de kits commerciaux et d'approches de purification pour l'extraction d'ADN à partir d'échantillons atmosphériques pour le séquençage de 3e génération sans amplification
Pourquoi l'air que nous respirons recèle des indices cachés
L'air qui nous entoure est rempli de vie invisible : grains de pollen, spores fongiques, bactéries, voire des traces de virus. Ces passagers aéroportés peuvent déclencher des allergies, propager des maladies et façonner discrètement les écosystèmes. Pour les comprendre, les scientifiques cherchent à lire leur ADN directement à partir d'échantillons d'air — mais il y a généralement très peu de matière biologique disponible. Cette étude pose une question pratique aux grandes implications : comment extraire au mieux de l'ADN fragile des filtres d'air usuels afin qu'il puisse être lu par des appareils de séquençage long reads modernes sans étapes d'amplification supplémentaires ?
Capturer la vie sur la poussière invisible
Les réseaux de surveillance de la qualité de l'air collectent déjà des particules sur de grands filtres en fibre de verre pour suivre la pollution. Les auteurs y voient une opportunité : utiliser ces mêmes filtres pour étudier la matière biologique atmosphérique. Le problème est que ces filtres contiennent typiquement des quantités d'ADN beaucoup plus faibles que le sol ou l'eau, et de nombreux organismes présents dans l'air — comme le pollen ou les bactéries desséchées — sont difficiles à lyser. L'équipe avait précédemment mis au point une méthode performante mais encombrante qui utilisait des produits chimiques agressifs pour purifier l'ADN de ces filtres. Elle fonctionnait bien, même lorsque l'ADN était rare, mais elle était lente, gourmande en main-d'œuvre et reposait sur des réactifs dangereux peu adaptés à une surveillance de routine.

Construire une routine de laboratoire plus sûre et plus rapide
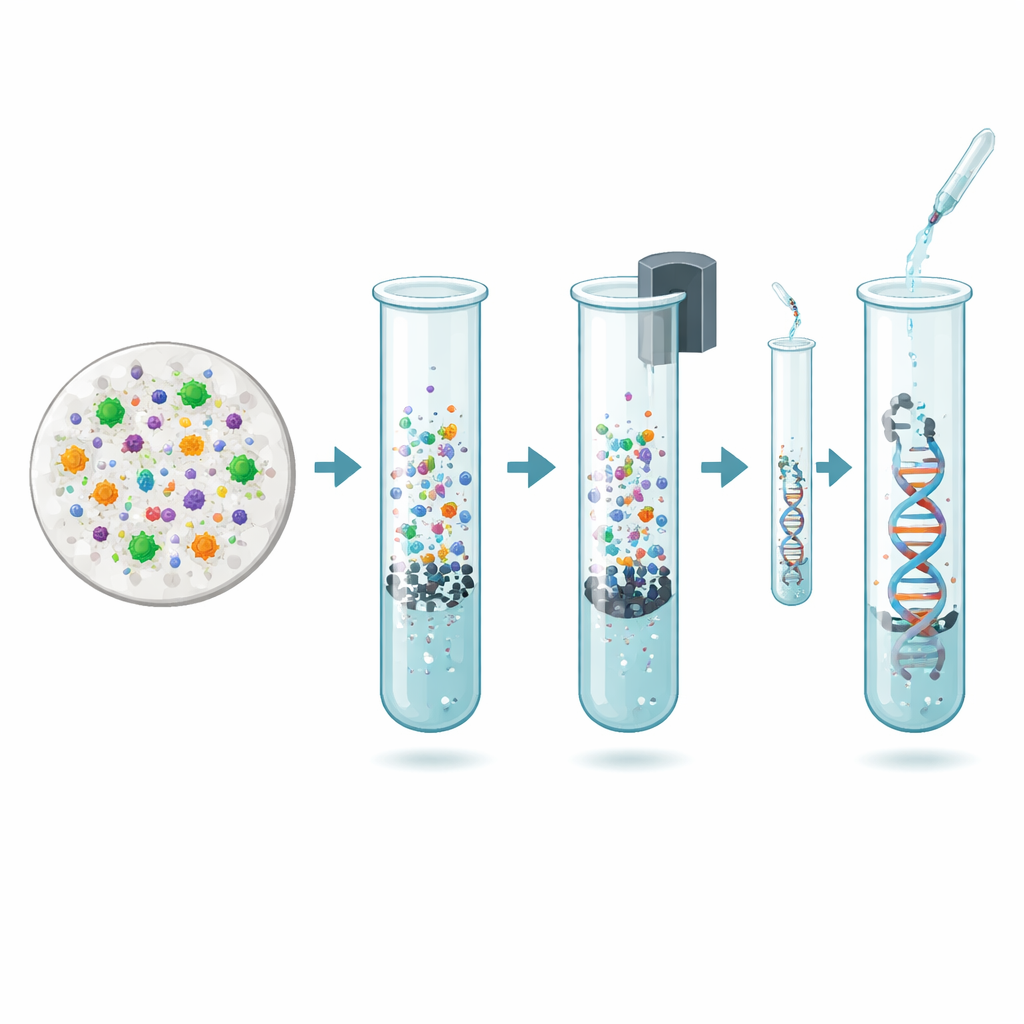
Le travail présenté ici vise à mettre à jour ce protocole antérieur pour le rendre plus sûr, plus simple et mieux adapté aux études de grande ampleur. Les auteurs ont conçu une méthode améliorée interne qui conserve la dégradation cellulaire soignée en plusieurs étapes — utilisant des enzymes, des détergents et un chauffage doux — mais remplace l'étape dangereuse de purification par solvants par des billes magnétiques. Ces petites billes sont fonctionnalisées pour retenir les molécules d'ADN et peuvent être retirées de la solution à l'aide d'un aimant, laissant de nombreux contaminants derrière elles. Les chercheurs ont ensuite comparé cette méthode mise à jour avec leur protocole original et avec cinq kits commerciaux populaires utilisant des approches de purification sur colonne initialement optimisées pour des échantillons de plantes ou de sols.
Mettre les méthodes d'extraction à l'épreuve
Pour garantir une comparaison équitable, l'équipe a utilisé des filtres archivés collectés sur le toit de l'Institut météorologique finlandais à Helsinki durant une campagne sur les bioaérosols. Ils ont choisi un filtre connu pour contenir des quantités d'ADN relativement élevées et un autre beaucoup plus pauvre, puis les ont découpés en morceaux identiques afin que chaque méthode traite le même matériau de départ. Ils ont évalué chaque approche en mesurant la quantité d'ADN produite, la propreté de cet ADN et la reproductibilité des résultats entre tests répétés. Deux des méthodes internes — le protocole original à base de solvants et la nouvelle méthode aux billes magnétiques — ainsi qu'un kit pour sols se sont distingués par des rendements plus élevés sur le filtre riche en ADN. Cependant, lorsque le niveau initial d'ADN était faible, seul le protocole original plus agressif a permis de récupérer de manière fiable une quantité suffisante de matériel génétique.
L'ADN extrait reflète-t-il vraiment la réalité ?
La quantité n'est pas la seule préoccupation : l'ADN doit aussi être intact et représentatif de la communauté présente dans l'air. L'équipe a vérifié la propreté des échantillons par des mesures d'absorption lumineuse, puis a introduit des extraits sélectionnés directement dans un séquenceur long reads Oxford Nanopore sans aucune étape de multiplication de l'ADN. C'est important, car l'amplification peut déformer la composition apparente des espèces. Les résultats de séquençage ont montré que la fois la méthode aux billes magnétiques et la méthode originale à solvants pouvaient générer des lectures longues et diversifiées avec une large gamme de compositions en bases, ce que la technologie Nanopore gère bien. En revanche, les deux méthodes n'ont pas retrouvé le même équilibre d'organismes : la méthode aux billes magnétiques avait tendance à favoriser les particules plus résistantes comme le pollen, tandis que la méthode à solvants capturait davantage d'ADN bactérien, probablement en raison de différences dans la facilité de lyse et la préservation des différentes cellules sur les filtres.
Ce que cela signifie pour la surveillance de l'air que nous partageons
Pour la surveillance de la santé publique et les relevés environnementaux, l'étude délivre un message clair et pragmatique. Si le préleveur d'air collecte suffisamment de matière biologique, le nouveau protocole aux billes magnétiques offre une manière plus sûre et plus rapide de préparer les filtres d'air pour le séquençage long reads de pointe. Lorsque l'ADN est rare, la méthode plus exigeante à base de solvants reste nécessaire pour éviter de tout perdre. Les kits commerciaux prêts à l'emploi, bien que pratiques, n'ont pas donné de performances suffisantes pour ces échantillons atmosphériques difficiles. Ensemble, les deux méthodes internes constituent une boîte à outils pratique : l'une adaptée aux travaux courants à haut rendement, et l'autre réservée aux signaux biologiques les plus faibles dans l'air que nous respirons.
Citation: Salokas, J., Sofieva-Rios, S., Paatero, J. et al. Evaluation of commercial kits and purification approaches for DNA extraction from atmospheric samples for 3rd generation sequencing without amplification. Sci Rep 16, 8402 (2026). https://doi.org/10.1038/s41598-026-38534-3
Mots-clés: ADN aéroporté, bioaérosols, métagénomique, séquençage long reads, surveillance environnementale