Clear Sky Science · fr
Inhibition ciblée de HDAC8 avec des composés non-hydroxamates [1,2,4]triazolo[4,3-a]quinoline
Un nouvel espoir pour un cancer pédiatrique
Le neuroblastome est un cancer pédiatrique agressif qui prend naissance dans les cellules nerveuses et qui est souvent difficile à traiter une fois qu’il s’est propagé. Cette étude explore une nouvelle manière de ralentir ou d’éliminer les cellules de neuroblastome en coupant un interrupteur cellulaire clé appelé HDAC8. En développant une nouvelle famille de molécules de type médicament qui agissent très sélectivement sur cet interrupteur, les chercheurs visent à créer des traitements à la fois plus efficaces contre les tumeurs et moins agressifs pour le reste de l’organisme.
Un interrupteur moléculaire au cœur du cancer
À l’intérieur de nos cellules, les gènes sont constamment activés et désactivés. Un système de contrôle important repose sur de petites étiquettes chimiques appelées groupes acétyle qui se lient à des protéines associées à l’ADN. Des enzymes appelées histone désacétylases (HDAC) retirent ces étiquettes, resserrent l’empaquetage de l’ADN et réduisent généralement l’activité des gènes. HDAC8 est un membre de cette famille d’enzymes et a été associé à plusieurs cancers, dont le neuroblastome. Lorsque HDAC8 est hyperactif, les cellules tumorales peuvent proliférer, survivre et se disséminer plus facilement, ce qui en fait une cible attrayante pour de nouveaux médicaments.
Limites des anciens médicaments contre les HDAC
Plusieurs médicaments bloquant les HDAC sont déjà approuvés pour certains cancers du sang, mais ils ont tendance à cibler plusieurs types de HDAC à la fois. La plupart de ces médicaments utilisent un groupe chimique hydroxamate pour lier un ion métallique dans le site actif de l’enzyme. Bien que efficace, ce groupe se lie aux métaux de façon très forte, ce qui peut entraîner des effets secondaires et limite la capacité du médicament à distinguer précisément les différents HDAC. En conséquence, les patients peuvent subir de la toxicité et les cellules normales peuvent être affectées en même temps que les cellules cancéreuses. Les chercheurs ont donc cherché des architectures chimiques alternatives qui conservent les bénéfices antitumoraux tout en réduisant les dommages indésirables.
Conception d’une nouvelle classe d’inhibiteurs ciblés
Dans ce travail, l’équipe a conçu et synthétisé 21 nouveaux composés construits autour d’un échafaudage triazoloquinoline, relié par un lien flexible à une région « α‑amino amide » capable de lier l’atome de zinc dans le site actif de HDAC8. En s’appuyant sur la conception assistée par ordinateur, ils ont choisi cette architecture pour s’insérer dans un étroit « canal de libération de l’acétate » unique à HDAC8, une caractéristique structurale qui favorise une grande spécificité. Des études de docking détaillées et des simulations de dynamique moléculaire ont montré que plusieurs des nouvelles molécules — en particulier celles nommées 9m et 9r — forment des interactions stables et durables dans la poche de HDAC8 et se lient aussi fortement, voire plus fortement, qu’un inhibiteur de référence bien connu. De façon importante, des tests biochimiques ont confirmé que les meilleurs composés bloquent fortement HDAC8 tout en épargnant largement les autres membres de la famille HDAC.
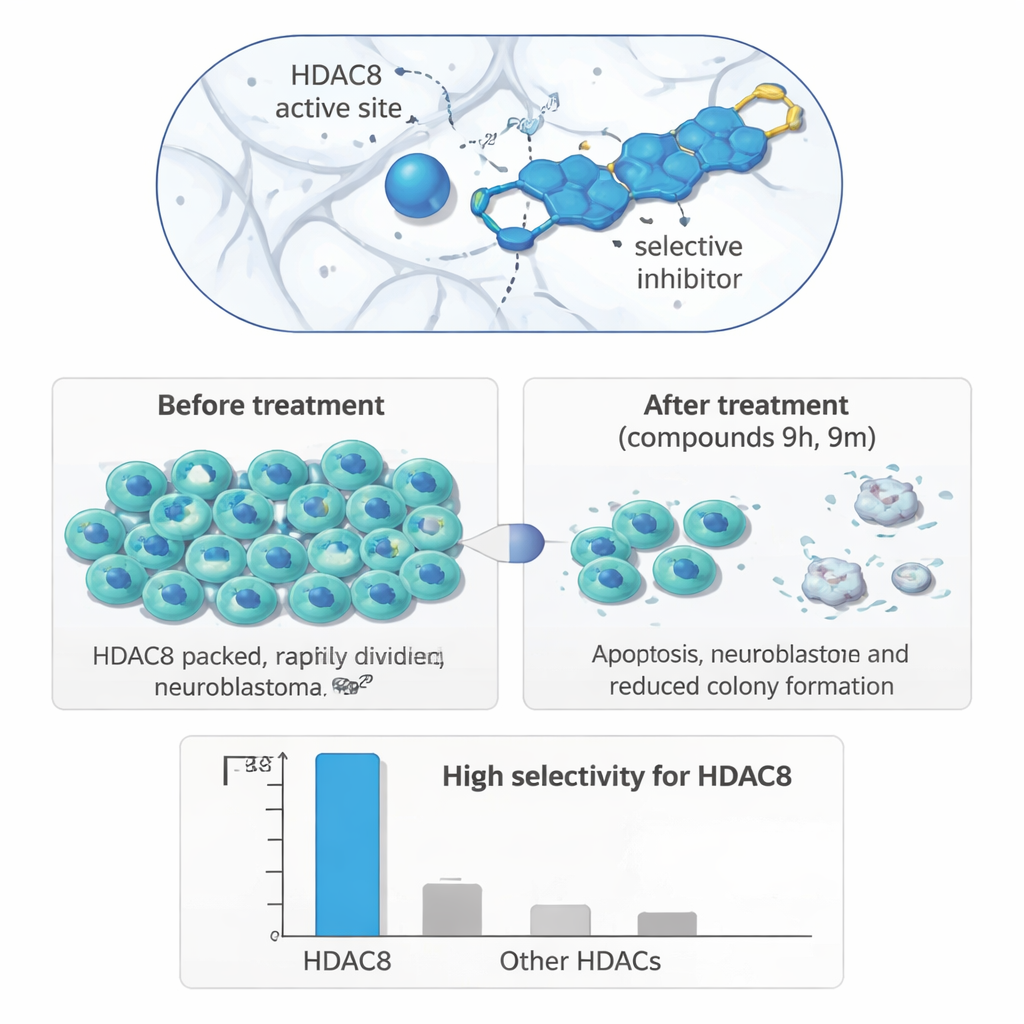
Du tube à essai aux cellules tumorales
Pour vérifier si ce ciblage enzymatique précis se traduit par des effets biologiques utiles, les chercheurs ont testé leurs composés sur un panel de lignées cellulaires humaines. Dans les cellules de neuroblastome (IMR‑32), deux molécules, 9h et 9m, se sont clairement distinguées : elles ont réduit la croissance cellulaire à des concentrations micromolaires et l’ont fait de manière plus marquée dans le neuroblastome que dans des cellules de cancer du sein ou du côlon, ou dans des cellules rénales non cancéreuses. Des expériences de formation de colonies à long terme ont montré que les cellules de neuroblastome traitées perdaient une grande partie de leur capacité à repousser après exposition au médicament. Dans un test de cicatrisation (« wound‑healing »), qui suit la rapidité de migration des cellules pour refermer une éraflure dans une monocouche, les deux composés ont ralenti le déplacement des cellules de neuroblastome, suggérant un potentiel métastatique réduit.
Explorer comment les composés tuent les cellules cancéreuses
Des expériences de cytométrie en flux ont révélé que 9h et 9m déclenchent la mort cellulaire programmée (apoptose) dans les cellules de neuroblastome et provoquent une accumulation de cellules dans une phase du cycle cellulaire associée à des dommages à l’ADN ou à la mort (Sub‑G1). Pour confirmer que ces effets proviennent réellement du blocage de HDAC8, l’équipe a mesuré l’état d’acétylation d’une protéine appelée SMC3, une cible connue de HDAC8 impliquée dans le maintien de l’appariement des chromosomes sœurs pendant la division cellulaire. Lorsque HDAC8 est inhibé, la SMC3 acétylée s’accumule. Après traitement par 9h ou 9m, les niveaux de SMC3 acétylée ont fortement augmenté, tandis que la quantité totale de SMC3 est restée inchangée — une preuve solide que ces composés ciblent directement HDAC8 dans les cellules vivantes et perturbent sa fonction normale dans le contrôle des chromosomes.
Ce que cela pourrait signifier pour les traitements futurs
Pris ensemble, la chimie, la modélisation informatique, les tests enzymatiques et les expériences cellulaires dressent un tableau cohérent : les composés triazoloquinoline nouvellement développés sont des bloqueurs puissants et hautement sélectifs de HDAC8 qui peuvent freiner la croissance et la diffusion des cellules de neuroblastome tout en épargnant les autres enzymes HDAC. Parce qu’ils évitent le groupe hydroxamate conventionnel, ils pourraient offrir une voie plus sûre pour exploiter HDAC8 comme cible thérapeutique. Bien que beaucoup de travail reste à faire — en particulier des études animales et, à terme, des essais cliniques — cette recherche pose une base solide pour développer des médicaments plus précis contre le neuroblastome pédiatrique et, éventuellement, d’autres maladies liées à HDAC8.
Citation: Bandaru, N.V.M.R., Fathima, A., Sengar, S. et al. Targeted HDAC8 inhibition with non-hydroxamate [1,2,4]triazolo[4,3-a] quinoline compounds. Sci Rep 16, 7472 (2026). https://doi.org/10.1038/s41598-026-38490-y
Mots-clés: Inhibiteurs de HDAC8, neuroblastome, thérapie épigénétique, triazoloquinoline, médicaments anticancéreux ciblés