Clear Sky Science · fr
Courants médiés par GluN2A et signal calcique dans des neurones humains dérivés de cellules iPS
Pourquoi de minuscules cellules cérébrales cultivées en laboratoire comptent
Les scientifiques se tournent de plus en plus vers des cellules cérébrales humaines cultivées en laboratoire pour étudier le développement du cerveau et comprendre ce qui dysfonctionne dans des troubles tels que l’autisme, l’épilepsie ou la maladie d’Alzheimer. Cette étude pose une question simple mais cruciale : ces neurones fabriqués en laboratoire arrivent-ils à maturité et se connectent-ils d’une manière réellement comparable au cerveau humain, notamment dans leur gestion d’un signal chimique clé, le glutamate ? La réponse éclaire comment construire des modèles de « mini-cerveau » plus réalistes et indique de nouvelles façons d’examiner la santé et la maladie du cerveau.
Construire des neurones à partir de cellules reprogrammées
Les chercheurs ont commencé avec des cellules souches pluripotentes induites humaines — des cellules ordinaires « reprogrammées » pour retrouver un état de cellule souche. Ils les ont ensuite orientées vers des précurseurs neuronaux, puis en réseaux de neurones et d’astrocytes de soutien, mimant le cortex humain en développement. Ils ont comparé deux protocoles largement utilisés, ou conditions de culture. L’un, appelé milieu BrainPhys, est conçu pour favoriser des neurones actifs et électriquement réactifs et tend à produire davantage d’astrocytes. L’autre, un milieu d’entretien neuronal plus traditionnel, favorise des neurones avec moins d’astrocytes. Sur soixante jours, l’équipe a suivi l’évolution de l’aspect, de l’activité génique et des types cellulaires de ces cultures, constatant que les cultures cultivées en BrainPhys développaient des morphologies neuronales plus élaborées et un rapport neurone/astrocyte plus proche de celui du cerveau humain réel.
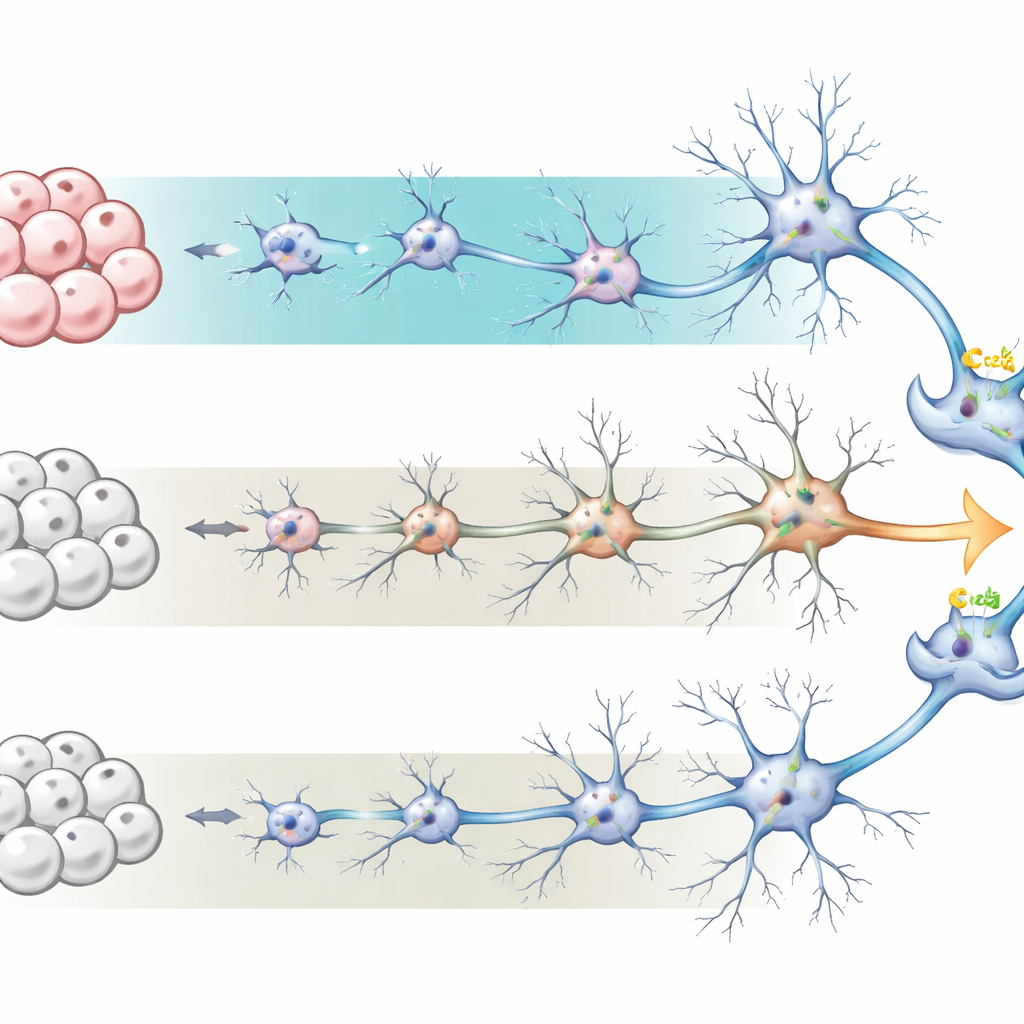
Signes que les cellules mûrissent
Pour évaluer le degré de « maturité » des neurones, l’équipe a mesuré l’activité génique globale par séquençage ARN au jour 60. Les cellules cultivées en BrainPhys présentaient près de deux mille gènes exprimés différemment par rapport au milieu standard, beaucoup étant liés à la différenciation neuronale, à la formation des synapses et à l’activité électrique. Les gènes associés aux fonctions astrocytaires et à l’inflammation étaient également plus élevés, reflétant la population astrocytaire plus importante. Dans l’ensemble, ces profils suggèrent que les cultures BrainPhys reproduisent mieux les stades avancés du développement cérébral, avec des points de communication neuronale plus raffinés et un environnement de soutien qui ressemble davantage au tissu vivant.
Interrupteurs clés dans la communication chimique
Une caractéristique de la maturation cérébrale est le changement dans la composition des récepteurs NMDA — des portes moléculaires sur les neurones qui s’ouvrent en réponse au glutamate et aident à établir des connexions liées à l’apprentissage. Au début du développement, une sous-unité appelée GluN2B domine ; plus tard, GluN2A prend le relais, modifiant la durée et l’intensité d’ouverture des récepteurs. Par microscopie, l’équipe a montré qu’au fil du temps davantage de récepteurs NMDA se localisaient dans les synapses, points de contact entre neurones, en particulier dans les cultures BrainPhys. Des mesures géniques ciblées ont révélé une diminution de la sous-unité « précoce » GluN2B et une augmentation de la sous-unité « tardive » GluN2A, indiquant que les neurones subissaient ce basculement développemental classique.
Suivre les courants et le calcium à l’intérieur des cellules
Des tests fonctionnels ont confirmé que ces changements moléculaires avaient un impact. À l’aide d’électrodes à pointe fine, les chercheurs ont enregistré des courants électriques déclenchés par la NMDA, un composé qui active sélectivement les récepteurs NMDA. Les neurones issus des deux méthodes de culture présentaient des courants robustes, mais le blocage de la sous-unité GluN2A réduisait ces courants d’environ la moitié, démontrant que GluN2A jouait désormais un rôle majeur dans le flux du signal. L’équipe a ensuite suivi le calcium, un messager intracellulaire clé, à l’aide d’un colorant fluorescent. Lors d’une exposition à la NMDA, une fraction bien plus importante de neurones cultivés en BrainPhys montrait de fortes poussées calciques, et l’amplitude du signal était plus grande. L’analyse génique suggère pourquoi : les cultures BrainPhys surexprimaient plusieurs composantes des canaux calciques et des voies de libération, équipant les cellules pour traduire l’activation des récepteurs NMDA en signaux calciques larges et coordonnés.
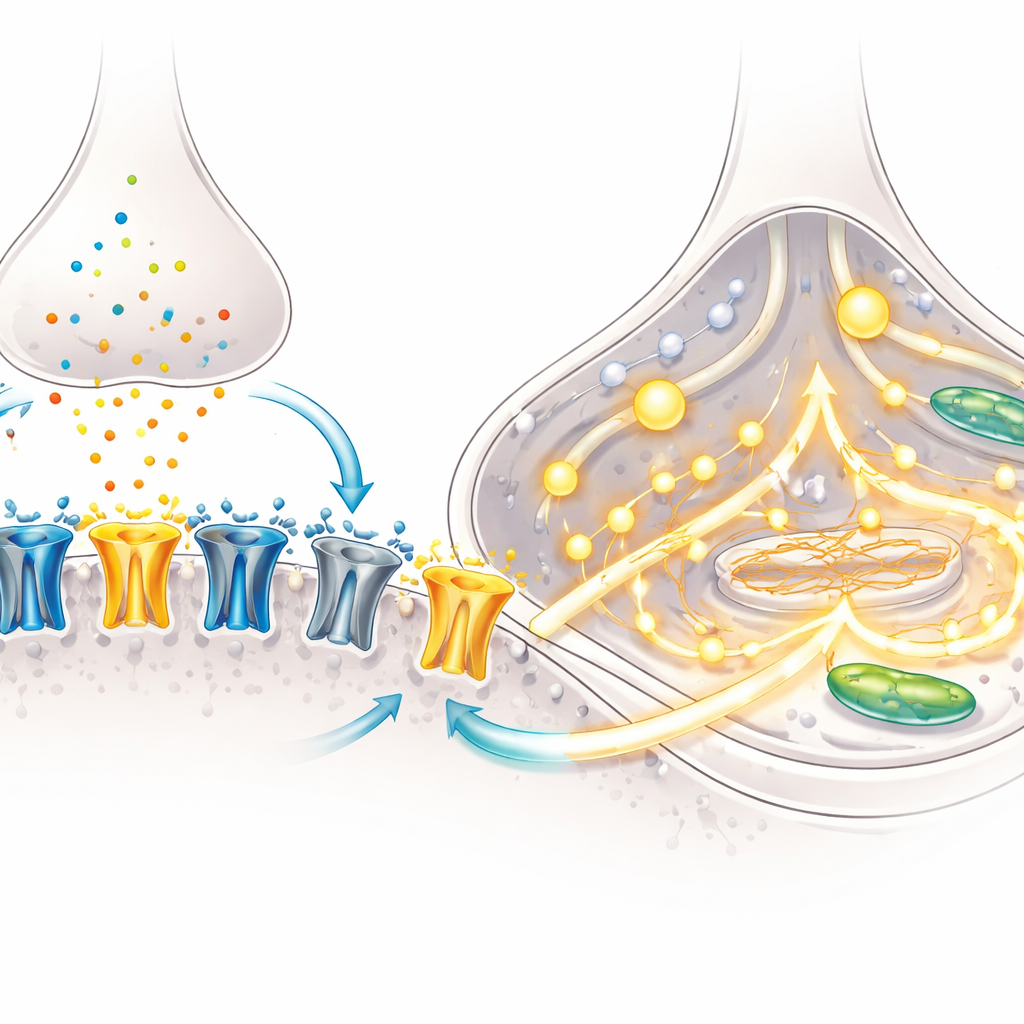
Ce que cela signifie pour l’étude des maladies cérébrales
Ensemble, ces résultats montrent que des neurones humains dérivés de cellules souches peuvent atteindre un état fonctionnellement mature en seulement deux mois, notamment lorsqu’ils sont cultivés dans des conditions favorisant des réseaux actifs et un mélange réaliste de neurones et d’astrocytes. À cet état, la sous-unité « de type adulte » GluN2A domine les courants des récepteurs NMDA et contribue fortement à la signalisation calcique, comme dans le cerveau humain en développement. Pour les non-spécialistes, la conclusion est que les chercheurs disposent désormais d’un modèle de laboratoire plus fidèle de la maturation, de la mise en réseau et de la réponse au glutamate des neurones excitateurs humains. Cela permet d’explorer comment de subtils changements génétiques ou des processus pathologiques perturbent ces basculements finement réglés, ouvrant une fenêtre sur des affections allant de l’épilepsie à la maladie d’Alzheimer et guidant la conception et les tests de futures thérapies.
Citation: Escamilla, S., Avilés-Granados, C., Peralta, F.A. et al. GluN2A-mediated currents and calcium signal in human iPSC-derived neurons. Sci Rep 16, 9736 (2026). https://doi.org/10.1038/s41598-026-38482-y
Mots-clés: Récepteurs NMDA, neurones issus de cellules souches, développement cérébral, signalisation calcique, maturation synaptique