Clear Sky Science · fr
L’inhibiteur double de G9a et antagoniste du récepteur de l’histamine H3 A-366 améliore les comportements répétitifs et sociaux et atténue la neuroinflammation chez la souris BTBR T + tf/J
Pourquoi cette étude sur la souris importe pour l’autisme
Les familles vivant avec un trouble du spectre autistique (TSA) font souvent face à un éventail de traitements qui soulagent seulement quelques symptômes à la fois. Cette étude explore un nouveau composé expérimental, appelé A-366, conçu pour agir simultanément sur deux systèmes biologiques très différents. Dans un modèle murin largement utilisé reproduisant des comportements proches de l’autisme, A-366 a réduit les comportements répétitifs, amélioré l’interaction sociale et calmé l’inflammation cérébrale, suggérant qu’un médicament unique pourrait à l’avenir cibler plusieurs caractéristiques centrales du TSA en même temps.
Une condition aux multiples facettes
Le TSA n’est pas une maladie unique avec une seule cause. Il implique des difficultés de communication sociale, des comportements répétitifs, et souvent d’autres défis comme l’anxiété ou des troubles de l’attention. Derrière ces signes extérieurs se cache un enchevêtrement de modifications de la chimie cérébrale et de la régulation des gènes. Les médicaments actuels, comme l’antipsychotique aripiprazole, ciblent principalement des systèmes messagers cérébraux tels que la dopamine et la sérotonine, et sont approuvés seulement pour des symptômes associés comme l’irritabilité. Parallèlement, la recherche a montré que la manière dont l’ADN est empaqueté et chimiquement marqué à l’intérieur des cellules cérébrales — l’épigénétique — change aussi dans le TSA, tout comme l’activité des réponses immunitaires et inflammatoires du cerveau. Ces multiples couches suggèrent qu’une approche « un target à la fois » peut être trop limitée.
Agir à la fois sur les interrupteurs génétiques et les messagers cérébraux
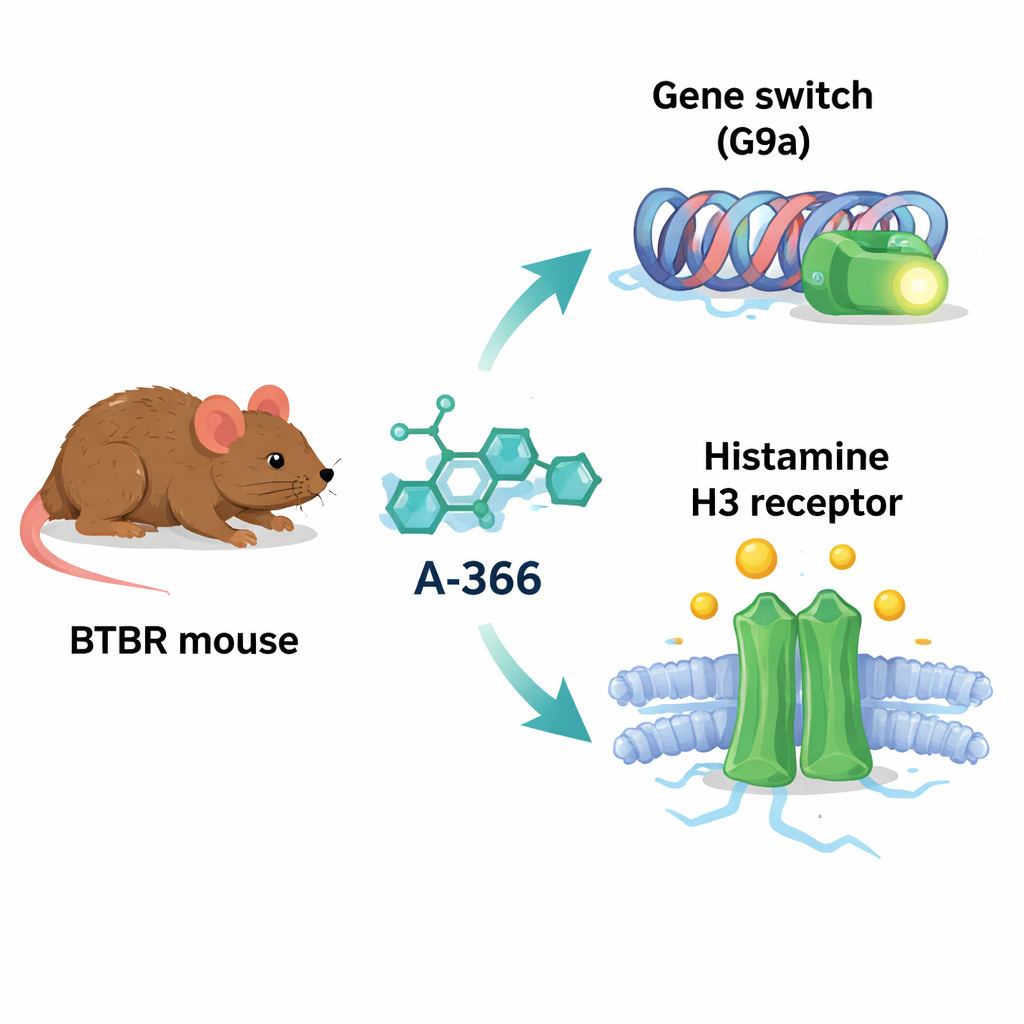
A-366 a été développé initialement pour bloquer une protéine appelée G9a, une enzyme qui ajoute des marques chimiques aux protéines histones et tend à réprimer l’expression de gènes. Dans plusieurs troubles du cerveau, l’activité de G9a et ses marques sont augmentées, pouvant mettre en sourdine des gènes importants pour l’apprentissage, la mémoire et l’organisation saine des circuits cérébraux. De façon intrigante, la forme chimique d’A-366 ressemble aussi à celle de médicaments qui bloquent le récepteur de l’histamine H3, un régulateur qui contrôle la libération d’histamine et d’autres neurotransmetteurs et a été lié à l’attention, à l’éveil et au comportement social. En raison de ce chevauchement, les auteurs ont supposé qu’A-366 pourrait agir comme un « agent double » : alléger la répression génétique nocive via l’inhibition de G9a tout en renforçant la signalisation de l’histamine en bloquant les récepteurs H3.
Mettre A-366 à l’essai chez des souris présentant des traits autistiques
L’équipe a travaillé avec des souris BTBR T+tf/J, une souche qui présente naturellement une sociabilité faible, un toilettage et un creusement répétitifs marqués, ainsi qu’une inflammation cérébrale élevée — des caractéristiques qui font écho à des aspects clés du TSA. Des mâles BTBR ont reçu des injections quotidiennes d’A-366 pendant trois semaines à trois doses différentes, et leur comportement a été comparé à celui de souris C57 typiques et de souris BTBR traitées soit par le pitolisant (un bloqueur standard du récepteur H3), soit par l’aripiprazole. À travers plusieurs tâches, A-366 a réduit de manière dose-dépendante le creusage, le déchiquetage et le toilettage excessifs, et amélioré la performance au test du labyrinthe en Y évaluant la mémoire de travail spatiale. Dans un test social en trois compartiments, A-366 a non seulement rétabli la préférence des souris à passer du temps avec une autre souris plutôt qu’une cage vide, mais à la dose la plus élevée il a porté les scores sociaux au niveau des souris typiques et surpassé les effets du pitolisant et de l’aripiprazole.
Calmer l’inflammation et confirmer les cibles
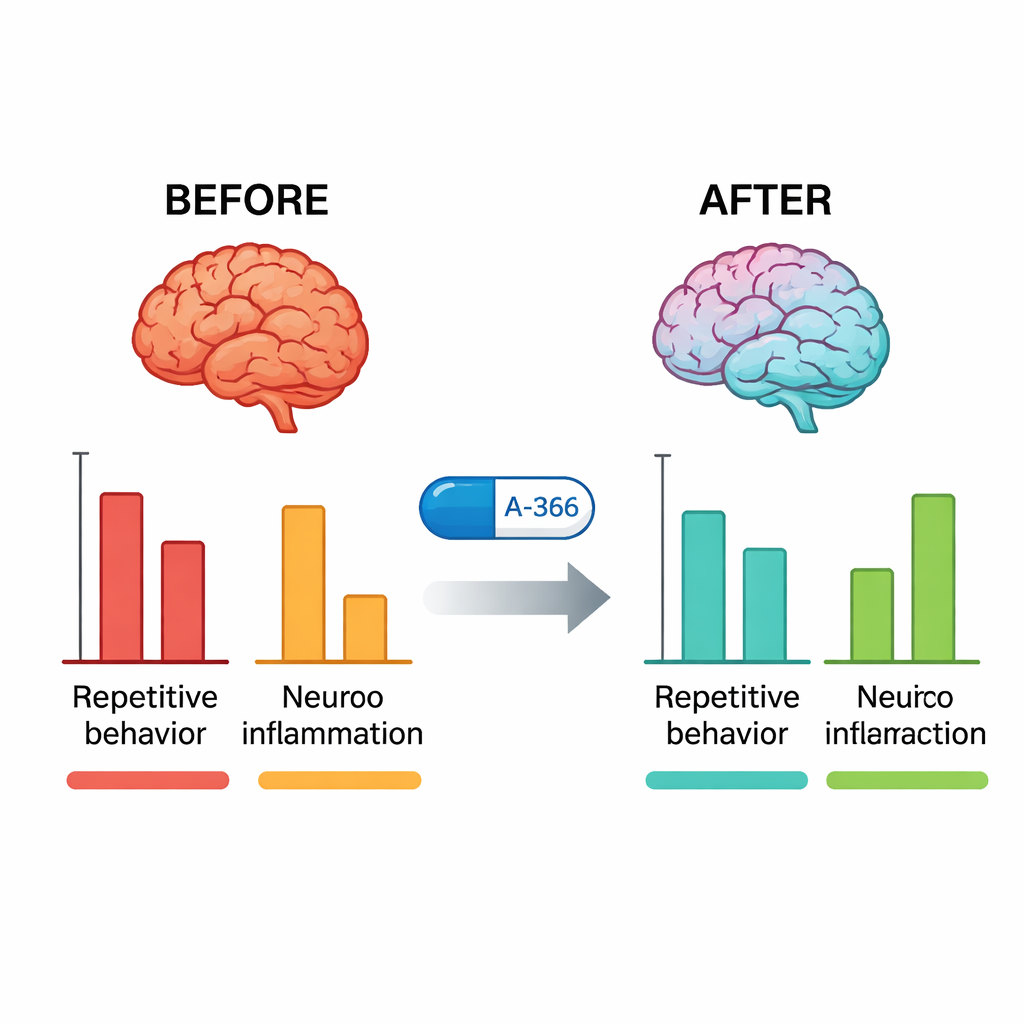
Après les tests comportementaux, les chercheurs ont examiné les cerveaux des souris. Chez les BTBR non traitées, l’activité de G9a dans l’hippocampe et le cervelet était nettement plus élevée que chez les souris typiques. Le traitement par A-366 a fortement réduit cette activité vers des niveaux normaux, tandis que le pitolisant seul ne l’a pas fait, confirmant qu’A-366 atteint bien sa cible épigénétique. Par ailleurs, des molécules inflammatoires clés — TNF-α, IL-6 et IL-1β — étaient fortement élevées chez les BTBR et ont été significativement abaissées par A-366, davantage que par l’aripiprazole. Lorsque les scientifiques ont ajouté un médicament qui active les récepteurs H3 (RAMH) en plus d’A-366, les bénéfices comportementaux et anti-inflammatoires ont été seulement partiellement annulés, et la baisse de l’activité de G9a est demeurée. Ce schéma soutient un mécanisme combiné : un soulagement épigénétique stable via l’inhibition de G9a plus une contribution médiée par l’histamine via le blocage des récepteurs H3.
Ce que cela pourrait signifier pour les traitements futurs
Pour un non-spécialiste, ces résultats suggèrent qu’il pourrait être possible de concevoir des médicaments qui agissent à la fois sur le « logiciel » et sur le « système de messagerie » du cerveau. Dans ce modèle murin de comportements proches de l’autisme, A-366 a atténué les actions répétitives, amélioré l’engagement social et réduit les signes d’inflammation cérébrale chronique en desserrant simultanément des répressions génétiques nocives et en ajustant la signalisation de l’histamine. A-366 lui-même a été développé pour d’autres maladies et nécessiterait une optimisation et des tests de sécurité approfondis avant toute utilisation chez l’humain. Néanmoins, il fournit une feuille de route pour une nouvelle classe de médicaments multi-cibles visant la biologie complexe du TSA, où le fait de n’aborder qu’une seule voie à la fois a jusqu’à présent offert un soulagement limité.
Citation: Hajar, M., Jayaprakash, P., Stark, H. et al. The dual G9a inhibitor and histamine H3 receptor antagonist A-366 improves repetitive and social behaviors and attenuates neuroinflammation in BTBR T + tf/J mice. Sci Rep 16, 7105 (2026). https://doi.org/10.1038/s41598-026-38481-z
Mots-clés: trouble du spectre autistique, thérapie épigénétique, récepteur de l’histamine H3, neuroinflammation, modèle murin