Clear Sky Science · fr
aFGF sauve des fibroblastes sénescents induits par l’hyperglycémie et améliore la cicatrisation des plaies diabétiques en régulant la voie SIRT1/STAT3
Pourquoi les plaies à cicatrisation lente sont importantes
Pour de nombreuses personnes atteintes de diabète, une petite coupure au pied ou à la jambe peut se transformer en une plaie récalcitrante qui persiste pendant des mois, conduisant parfois à une infection voire à une amputation. Ces ulcères chroniques ne sont pas qu’un problème superficiel : les cellules de la peau chargées de reconstruire le tissu endommagé vieillissent souvent prématurément et cessent de fonctionner correctement. Cette étude explore une voie prometteuse pour « rajeunir » certaines de ces cellules en utilisant un signal de réparation naturel, dans le but d’aider les plaies diabétiques à se refermer plus vite et de façon plus complète.
Des cellules qui vieillissent trop tôt
La peau saine repose sur les fibroblastes — des cellules de soutien situées dans les couches profondes de la peau — qui doivent se multiplier, migrer dans la plaie et déposer une charpente fraîche pour le nouveau tissu. Dans le diabète, l’hyperglycémie chronique et les molécules altérées par le sucre poussent ces fibroblastes vers un état appelé sénescence cellulaire. Les fibroblastes sénescents ne se divisent plus correctement, produisent moins des protéines structurales nécessaires à la réparation et libèrent à la place un cocktail de facteurs pro-inflammatoires qui entretiennent l’inflammation. Les auteurs montrent que, chez des rats diabétiques, la peau autour d’une plaie contient davantage de ces fibroblastes vieillissants et moins des protéines de matrice utiles, ce qui corrèle avec une cicatrisation beaucoup plus lente.
Un signal de réparation prometteur
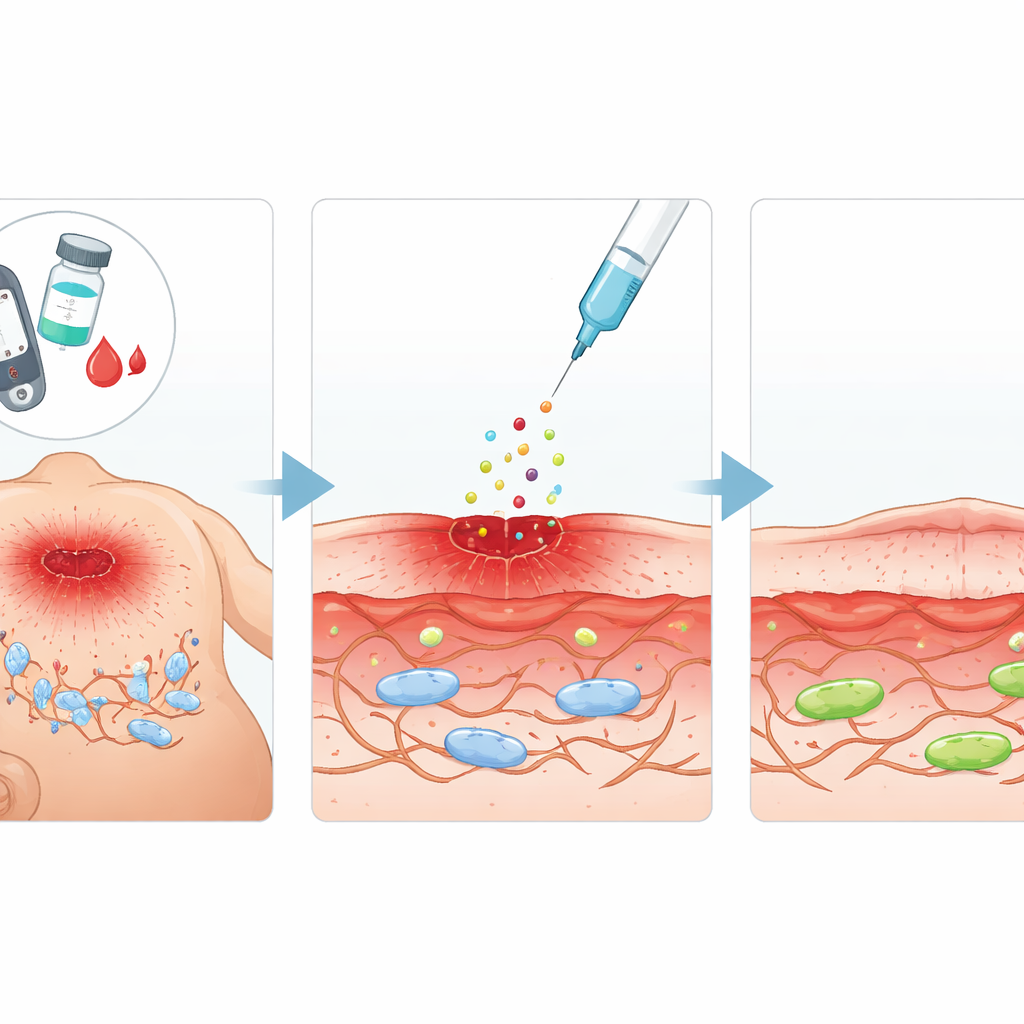
L’équipe s’est concentrée sur le facteur de croissance des fibroblastes acide (aFGF), une protéine naturelle connue pour stimuler la prolifération cellulaire et la réparation tissulaire. Ils ont émis l’hypothèse que l’aFGF pourrait non seulement stimuler l’activité des fibroblastes, mais aussi inverser les changements de type vieillissement induits par l’excès de sucre. Chez des rats diabétiques, ils ont créé des plaies cutanées standardisées et injecté de l’aFGF autour de la zone lésée tous les quelques jours. Par rapport aux animaux diabétiques non traités, les rats traités par aFGF ont montré une réduction plus rapide de la surface de la plaie, une meilleure reconstruction du tissu sous-jacent et des niveaux plus faibles de marqueurs de la sénescence cellulaire. Dans des expériences parallèles en laboratoire sur une lignée de fibroblastes de souris exposée à une très forte glycémie, l’aFGF a restauré la capacité des cellules à se diviser et à migrer — deux comportements essentiels à la fermeture d’une plaie.
Apaiser le stress oxydatif à l’intérieur des cellules
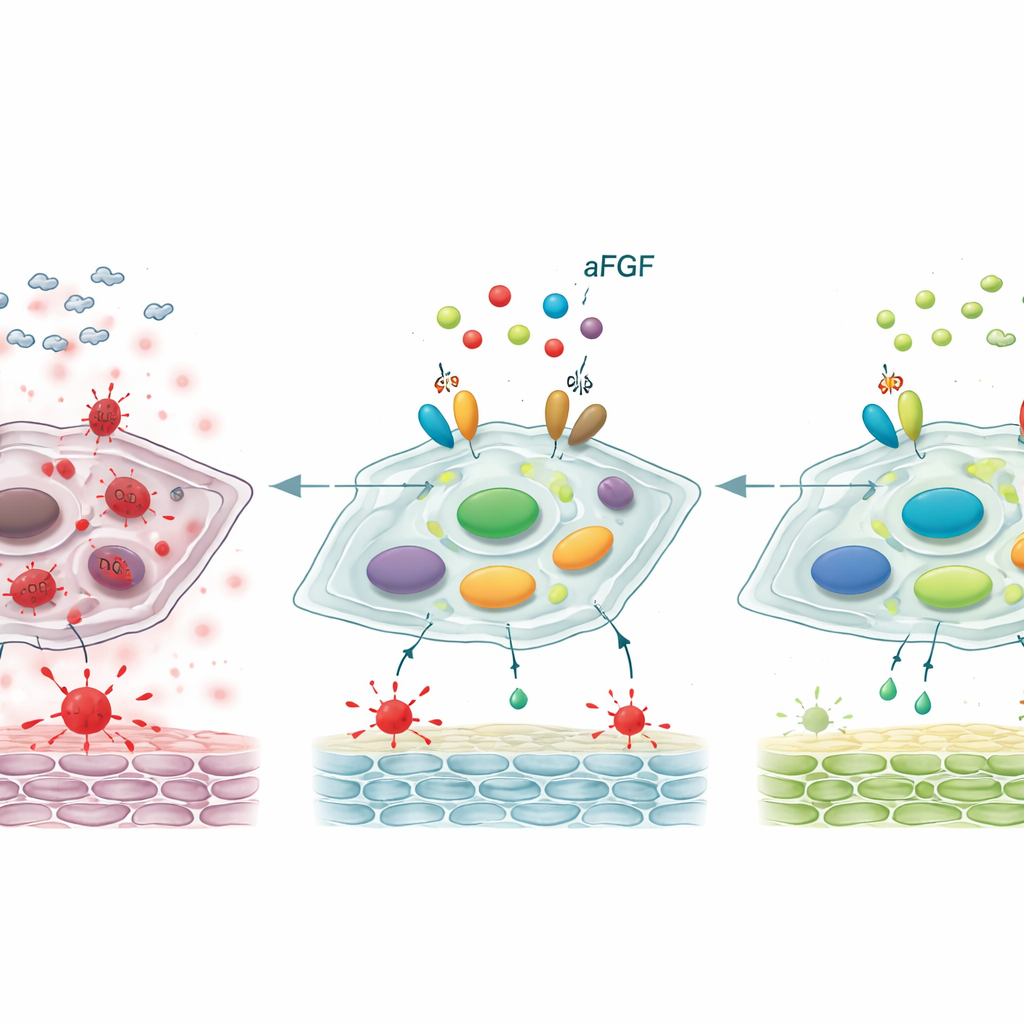
L’hyperglycémie ne se contente pas d’exposer les cellules à un carburant supplémentaire : elle provoque aussi une production excessive d’espèces réactives de l’oxygène, des molécules instables qui endommagent protéines, lipides et ADN. Ce stress oxydatif est un déclencheur majeur de la sénescence des fibroblastes. Les chercheurs ont mesuré plusieurs indicateurs standards de ce stress dans leur modèle cellulaire, incluant des produits de dégradation nocifs et l’activité des enzymes antioxydantes de la cellule. En condition de forte glycémie, les fibroblastes présentaient davantage de dommages et des défenses antioxydantes affaiblies. Lors de l’ajout d’aFGF, l’équilibre a basculé : les marqueurs nocifs ont diminué et les enzymes protectrices sont devenues plus actives. Cela suggère que l’aFGF contribue à restaurer un environnement interne plus sain, réduisant la probabilité que les fibroblastes basculent vers un état de sénescence permanente.
Réinitialiser un interrupteur de contrôle clé
En creusant plus loin, les scientifiques ont examiné un axe de contrôle moléculaire impliquant deux protéines, SIRT1 et STAT3, qui influencent ensemble si les fibroblastes restent jeunes ou deviennent sénescents. Dans les plaies diabétiques et les cellules traitées par forte glycémie, les niveaux de SIRT1, un protecteur associé à la résistance au stress, étaient réduits, tandis que la forme activée de STAT3 — un moteur du vieillissement et du comportement inflammatoire — était augmentée. Le traitement par aFGF a inversé ce schéma : SIRT1 a augmenté et STAT3 activé a diminué. Lorsque l’équipe a bloqué SIRT1 avec un inhibiteur spécifique, l’aFGF a en grande partie perdu sa capacité à réduire le stress oxydatif, atténuer les marqueurs de sénescence et accélérer la fermeture des plaies chez les rats. Ceci indique que les effets bénéfiques de l’aFGF dépendent fortement du réveil de SIRT1, qui à son tour réprime STAT3 et le programme délétère de vieillissement qu’il contrôle.
Ce que cela pourrait signifier pour les patients
Dans l’ensemble, les résultats suggèrent que l’aFGF fait plus que stimuler la prolifération cellulaire. Il semble sauver des fibroblastes surmenés dans les plaies diabétiques d’un cycle destructeur de vieillissement, en réduisant le stress oxydatif et en réinitialisant un interrupteur moléculaire clé pour que ces cellules puissent de nouveau participer à la reconstruction des tissus. Bien que le travail ait été réalisé chez le rat et sur des cellules en culture — et que les plaies diabétiques humaines soient encore plus complexes que les modèles utilisés ici — les résultats désignent l’aFGF comme un candidat prometteur pour des traitements futurs. Si des bénéfices similaires sont confirmés chez l’humain, une thérapie aFGF ciblée pourrait un jour accélérer la guérison des ulcères diabétiques chroniques, réduisant la douleur, le risque d’infection et la probabilité de complications graves.
Citation: Wang, X., Lu, M., Jia, S. et al. aFGF rescues high glucose-induced senescent fibroblasts and improves diabetic wound healing by regulating SIRT1/STAT3 pathway. Sci Rep 16, 7856 (2026). https://doi.org/10.1038/s41598-026-38480-0
Mots-clés: cicatrisation des plaies diabétiques, vieillissement des fibroblastes</keyword;> <keyword>stress oxydatif, thérapie par facteurs de croissance, voie SIRT1 STAT3