Clear Sky Science · fr
Sécurité et efficacité préliminaire de l’ajout de tocilizumab au cisplatine/docétaxel pour le traitement des patientes atteintes d’un cancer du sein triple négatif localement avancé : essai clinique prospectif de phase 1/2
Pourquoi cette étude compte pour les patientes et leurs proches
Le cancer du sein triple négatif est l’une des formes de cancer du sein les plus difficiles à traiter. Il a tendance à croître rapidement, à récidiver plus souvent et il n’exprime pas les récepteurs hormonaux ni HER2 auxquels de nombreux traitements modernes s’adressent. Cette étude a évalué si l’ajout d’un médicament immunomodulateur appelé tocilizumab, déjà utilisé pour l’arthrite et d’autres affections inflammatoires, pouvait améliorer l’efficacité et la sécurité de la chimiothérapie standard chez des patientes présentant un cancer du sein triple négatif localement avancé au niveau du sein et des ganglions voisins.
Un cancer agressif aux options limitées
Le cancer du sein triple négatif représente environ un cas sur cinq, mais il cause une part disproportionnée des décès car il est agressif et dispose de moins de traitements ciblés efficaces. Pour de nombreuses patientes dont les tumeurs sont volumineuses ou ont envahi les ganglions voisins, l’option principale est une chimiothérapie puissante administrée avant la chirurgie pour réduire la taille de la tumeur. Même avec des protocoles modernes incluant des agents à base de platine comme le cisplatine, un nombre significatif de patientes présentent encore des résidus tumoraux après traitement, ce qui est associé à un risque plus élevé de récidive.
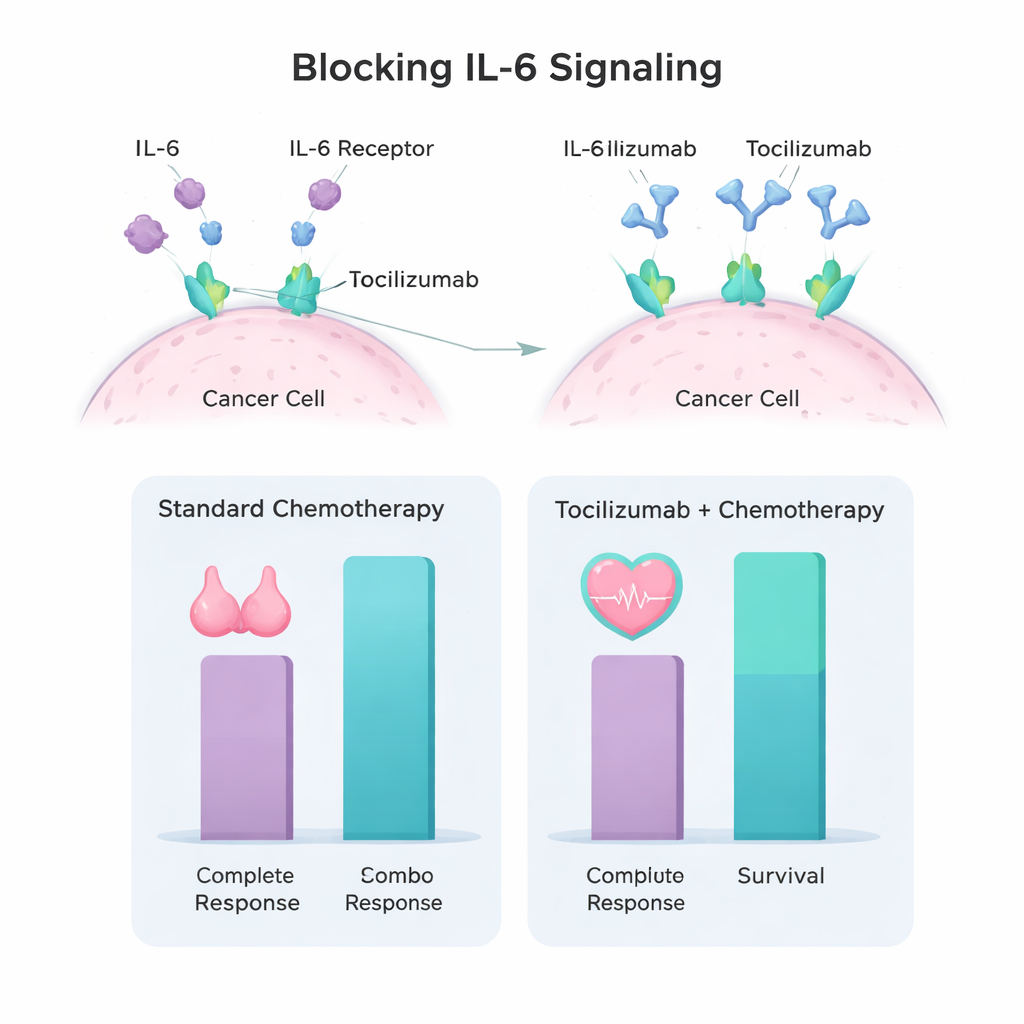
Bloquer un signal nuisible
Des chercheurs ont observé que les tumeurs triple négatif et les cellules qui les entourent produisent souvent de fortes quantités d’une protéine de signalisation appelée interleukine‑6 (IL‑6). L’IL‑6 véhicule un message constant de « croissance et résistance au traitement » pour la tumeur. Le tocilizumab est un anticorps qui bloque le récepteur de l’IL‑6, interrompant ce signal. Des études précliniques et chez l’animal menées par la même équipe ont montré que l’administration de tocilizumab avant le cisplatine rendait les cellules de cancer triple négatif plus sensibles à la chimiothérapie et ralentissait la croissance tumorale. Ces résultats ont conduit l’équipe à concevoir un essai clinique de « premier chez l’humain » afin d’évaluer la sécurité et de rechercher des signes précoces d’efficacité chez des patientes.
Comment l’essai a été mené
L’étude était un essai monocentrique de phase 1/2 à Riyad qui a inclus 30 femmes atteintes d’un cancer du sein triple négatif localement avancé (taille tumorale d’au moins 4 cm, sans métastases à distance). Toutes les patientes ont reçu du tocilizumab par voie intraveineuse le jour 1, suivi de cisplatine et docetaxel le jour 2, tous les quatre semaines pendant six cycles. La première partie de l’essai a utilisé un schéma d’escalade de dose « 3+3 » classique pour identifier une dose sûre de chimiothérapie à associer à une dose fixe de tocilizumab. Une fois cette dose choisie, davantage de patientes ont été traitées dans une phase d’expansion. Après la chimiothérapie, les patientes ont été opérées et des pathologistes ont examiné minutieusement le tissu mammaire et les ganglions lymphatiques pour déterminer s’il restait du cancer invasif. Les objectifs principaux étaient d’évaluer la sécurité et de mesurer combien de patientes obtenaient une réponse pathologique complète — c’est‑à‑dire l’absence de cancer invasif détectable dans le sein ou les ganglions axillaires.
Ce que les chercheurs ont observé
Sur les 30 patientes incluses, 28 ont terminé le traitement et 26 ont été opérées. Le groupe était relativement jeune (âge médian 42 ans), et la plupart présentait une maladie de stade III et une atteinte ganglionnaire au départ — des caractéristiques généralement associées à un pronostic plus défavorable. Globalement, 62 % des patientes n’avaient plus de cancer invasif après le traitement et 81 % n’avaient plus de cancer dans les ganglions. Lorsque les réponses quasi‑complètes (petites zones tumorales résiduelles avec ganglions propres) étaient ajoutées, 81 % des patientes entraient dans la catégorie réponse complète ou quasi‑complète, et aucune de ces patientes n’a présenté de récidive pendant la période de suivi. Les patientes porteuses de mutations héréditaires BRCA1 ou BRCA2 ont particulièrement bien répondu : toutes ont obtenu une réponse complète. Les premiers résultats de survie étaient encourageants, avec une survie sans maladie estimée à trois ans de 80 % et une survie globale de 90 %, malgré le fait que de nombreuses patientes présentaient au départ une maladie locale très avancée.
Effets secondaires et sécurité
La sécurité était un point central car le protocole associait un médicament biologique à une chimiothérapie intensive. Parmi les 28 patientes évaluées, il n’y a eu aucun décès lié au traitement. Les effets secondaires bénins à modérés les plus fréquents étaient nausées, douleurs articulaires et musculaires, vomissements, diarrhée, éruption cutanée et modifications transitoires de l’hémogramme. Les événements plus graves comprenaient des neutropénies fébriles, des élévations des enzymes hépatiques et des augmentations significatives mais contrôlables du cholestérol et des triglycérides — des modifications connues avec le tocilizumab et gérées par des traitements standards. Seules quelques patientes ont nécessité des réductions de dose de chimiothérapie, et les problèmes rénaux liés au cisplatine ont été rares et réversibles, ce qui suggère que la combinaison était globalement tolérable.
Ce que cela pourrait signifier à l’avenir
Pour les patientes et leurs proches confrontés au cancer du sein triple négatif, ces premiers résultats suggèrent que l’ajout d’un bloqueur de l’IL‑6 avant la chimiothérapie standard pourrait augmenter sensiblement les chances de ne retrouver aucun cancer à l’analyse chirurgicale, en particulier chez les personnes porteuses de mutations BRCA, et ce sans ajouter d’effets indésirables dangereux. Toutefois, l’étude était de petite taille, réalisée dans un seul centre et n’autorisait pas certains traitements adjuvants modernes pour les patientes ayant des résidus de maladie. Le tocilizumab a également été arrêté après la chirurgie, de sorte que les bénéfices à plus long terme restent à préciser. Des essais plus larges et randomisés seront nécessaires pour confirmer si cette approche doit être intégrée aux soins standards, mais ce travail ouvre une piste prometteuse : cibler les signaux inflammatoires dans et autour de la tumeur pour aider la chimiothérapie existante à être plus efficace et plus précise contre un cancer très difficile à traiter.
Citation: Al-Tweigeri, T., Tulbah, A., Akhtar, S. et al. Safety and preliminary efficacy of adding tocilizumab to cisplatin/docetaxel for the treatment of locally advanced triple-negative breast cancer patients: prospective phase 1/2 clinical trial. Sci Rep 16, 7029 (2026). https://doi.org/10.1038/s41598-026-38465-z
Mots-clés: cancer du sein triple négatif, tocilizumab, blocage de l’IL-6, chimiothérapie néoadjuvante, réponse pathologique complète