Clear Sky Science · fr
Explorer les profils d’expression génique sous-jacents des phénotypes de différences du développement sexuel par analyse du transcriptome
Pourquoi cette recherche nous concerne tous
La plupart d’entre nous apprennent à l’école que le sexe biologique se détermine de façon simple et binaire : XX donne des ovaires, XY donne des testicules. Cette étude remet en cause cette image simplifiée. En lisant quels gènes sont activés ou réprimés dans les gonades de personnes présentant des différences du développement sexuel (DSD), les chercheurs mettent au jour une histoire plus nuancée dans laquelle le développement sexuel humain ressemble moins à un interrupteur qu’à un continuum. Leur travail éclaire la façon dont les corps se forment, explique pourquoi certaines personnes ne correspondent pas aux catégories mâle ou femelle typiques, et indique comment la médecine pourrait mieux comprendre et prendre en charge ces personnes.
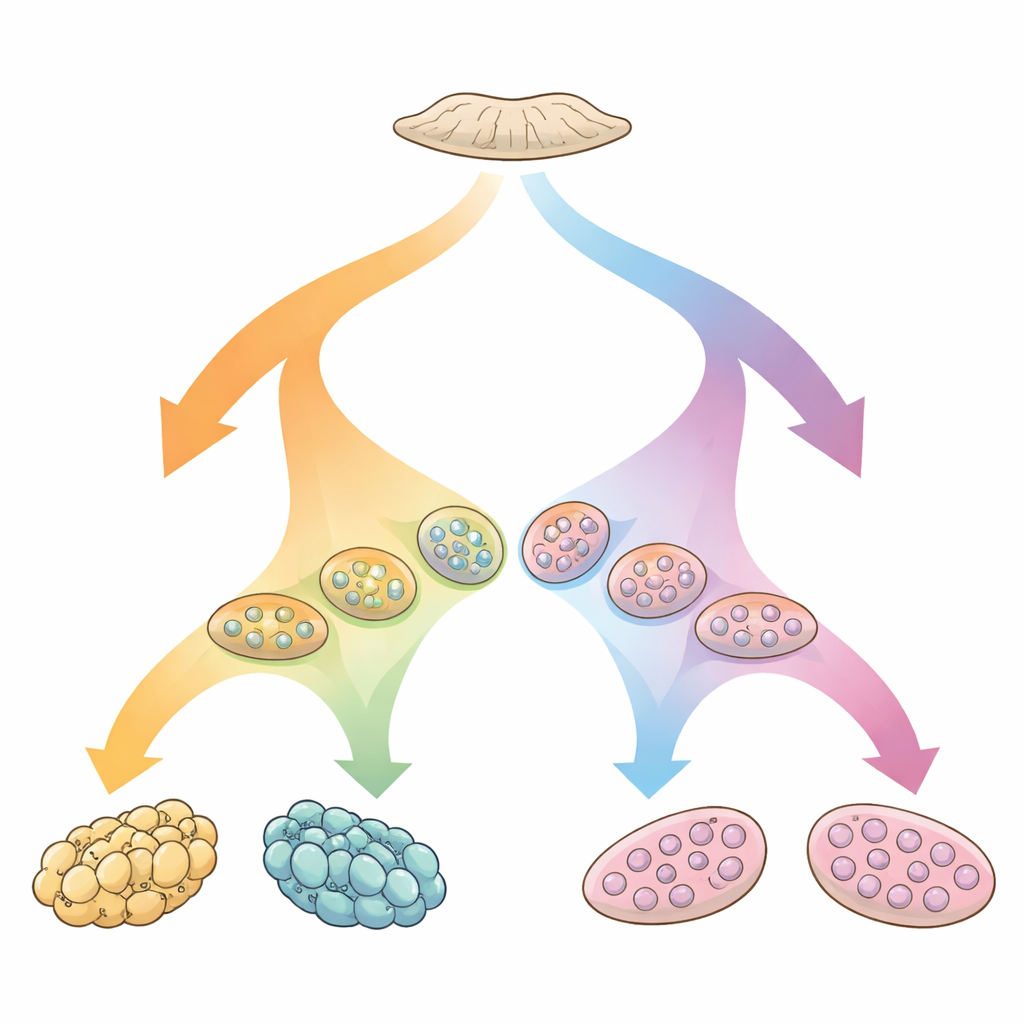
Un point de départ flexible au début de la vie
Les gonades commencent leur développement comme une structure « bipotente » flexible qui peut devenir soit testicules, soit ovaires. Un réseau de gènes et de signaux oriente progressivement ce tissu primitif dans un sens ou dans l’autre, façonnant ensuite la production d’hormones et l’anatomie visible. Lorsqu’une partie de ce réseau est perturbée, le résultat peut être une DSD, où chromosomes, gonades et anatomie ne correspondent pas aux schémas habituels. Beaucoup de ces conditions restent inexpliquées au niveau de l’ADN. L’équipe à l’origine de cette étude a estimé qu’examiner directement l’activité génique dans le tissu gonadal pourrait révéler des motifs que les tests génétiques classiques ne détectent pas, et aider à comprendre comment ces organes choisissent — ou échouent à choisir — une voie de développement.
Écouter l’activité des gènes gonadaux
Les chercheurs ont analysé du tissu gonadal provenant de 11 personnes présentant différentes conditions DSD : dysgénésie gonadique partielle, insensibilité complète aux androgènes, et une forme appelée DSD ovotesticulaire, où une personne porte à la fois des tissus de type testicule et de type ovaire. Grâce au séquençage de l’ARN, ils ont mesuré le niveau d’activité de dizaines de milliers de gènes et comparé ces profils à des données de référence issues de testicules et d’ovaires sains aux stades fœtal, infantile et adulte. Une méthode de visualisation regroupant les échantillons selon la similarité de gènes clés du développement sexuel a montré que les échantillons DSD ne se répartissaient pas nettement en grappes masculines ou féminines. Ils occupaient plutôt une zone intermédiaire, formant une grappe propre située entre testicules et ovaires typiques. Certains échantillons se rapprochaient du groupe testiculaire, d’autres du groupe ovarien, suggérant une gamme graduelle d’identités gonadales.
Signaux mixtes au sein des gonades
Lorsque l’équipe s’est concentrée sur des gènes bien connus qui orientent les gonades vers le testicule ou l’ovaire, elle a constaté que ces « balises » sortaient souvent de leurs plages habituelles. Chez des individus 46,XY atteints de dysgénésie gonadique partielle ou d’insensibilité aux androgènes, les gènes nécessaires au développement testiculaire sain et à la production de spermatozoïdes étaient abaissés, tandis que des gènes de développement plus larges étaient surexprimés, cohérent avec une formation testiculaire ralentie ou incomplète. Chez des personnes 46,XX atteintes de DSD ovotesticulaire, le tableau était encore plus mixte : des gènes qui conduisent habituellement au développement testiculaire étaient partiellement activés, tandis que plusieurs gènes associés aux ovaires étaient diminués. L’analyse à grande échelle des voies biologiques a confirmé ce schéma. Des processus spécifiques au testicule tels que la spermatogenèse, la division cellulaire et le métabolisme énergétique étaient affaiblis dans de nombreux cas 46,XY, alors que les cas 46,XX ovotesticulaires montraient une activation simultanée de voies liées au testicule et à l’ovaire, reflétant les structures mixtes observées au microscope.
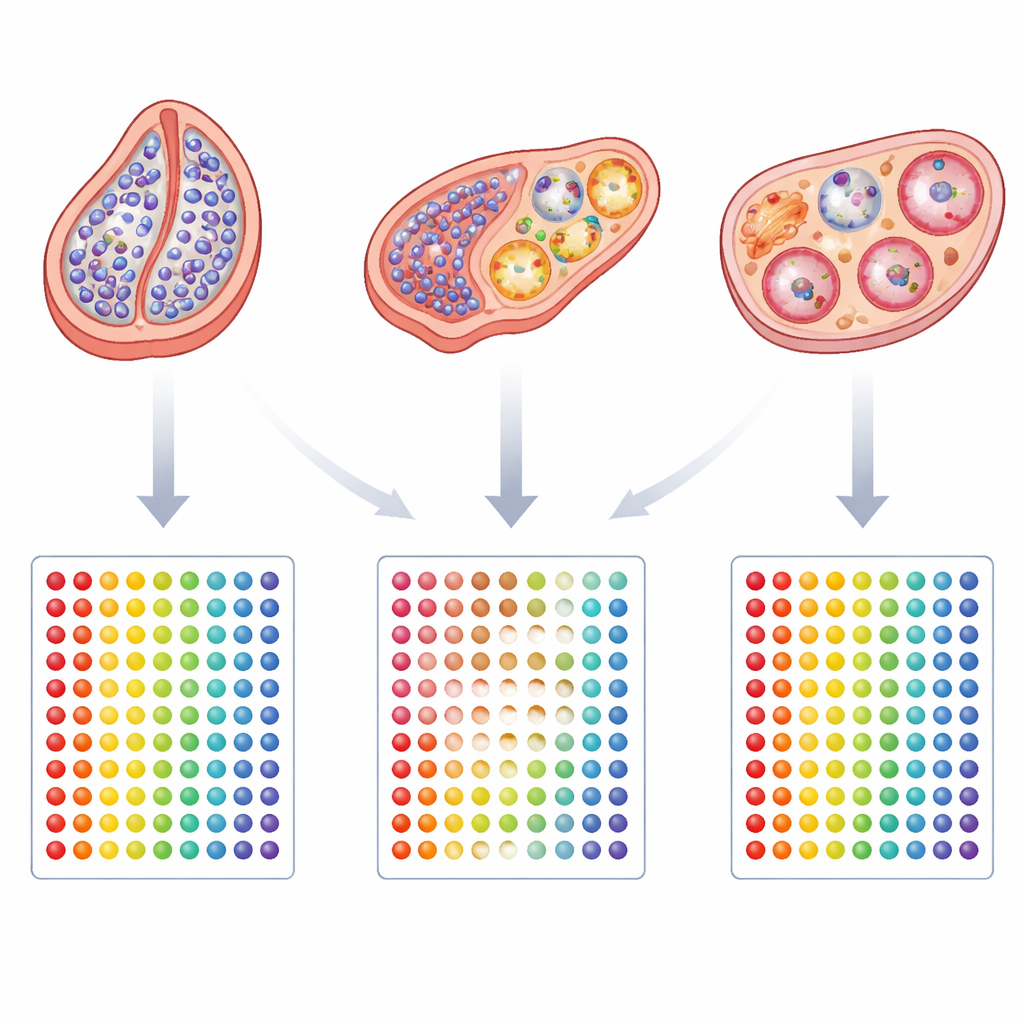
Un thème commun à travers les conditions
Malgré la diversité des présentations cliniques, une caractéristique récurrente est apparue : une activité réduite d’un gène appelé CBX2, qui contribue à organiser le conditionnement de l’ADN et contrôle de larges ensembles de gènes déterminant le sexe. Des expériences animales avaient déjà montré que la perturbation de ce régulateur peut estomper la frontière entre développement testiculaire et ovarien. Sa régulation à la baisse constante dans tous les groupes DSD suggère qu’une instabilité à ce niveau régulatoire peut pousser les gonades à s’éloigner d’une identité clairement testiculaire ou ovarienne et à se stabiliser quelque part entre les deux. L’étude souligne également que certains patients plus jeunes montrent encore des signes de flexibilité développementale, avec des signaux plus marqués dans les voies de croissance et des cellules germinales précoces que chez les adultes, ce qui suggère que le facteur temporel peut influencer la solidité de la détermination gonadale.
Repenser l’interrupteur simpliste
Pour un observateur non spécialiste, cette recherche indique que les gonades humaines ne basculent pas simplement entre deux positions fixes. Elles suivent plutôt un spectre de patrons d’activité génique qui peut aboutir à des états fortement testiculaires, fortement ovariens ou intermédiaires. Pour les personnes atteintes de DSD, cela signifie que l’important biologiquement n’est pas seulement les chromosomes qu’elles portent ou l’apparence extérieure de leur corps, mais aussi la façon dont leur tissu gonadal s’est développé au niveau moléculaire. En cartographiant ces paysages internes, l’étude plaide pour dépasser une vision strictement binaire du développement sexuel et pour ajouter des tests basés sur l’ARN en complément du séquençage de l’ADN dans les travaux cliniques futurs. Ce faisant, elle offre une compréhension plus nuancée et fondée sur la biologie du sexe, mieux adaptée à la diversité réelle observée chez les patients.
Citation: Fabbri-Scallet, H., Calonga-Solís, V., Guerra-Júnior, G. et al. Exploring the underlying gene expression profiles of differences of sex development phenotypes through transcriptome analysis. Sci Rep 16, 8801 (2026). https://doi.org/10.1038/s41598-026-38435-5
Mots-clés: spectrum du développement sexuel, transcriptome gonadal, différences du développement sexuel, profilage de l’expression génique</keyword-profilage> <keyword>DSD ovotesticulaire