Clear Sky Science · fr
Découverte in silico d’un inhibiteur multi‑cible dérivé de composés naturels pour la thérapie de la maladie de Huntington
Un nouvel angle sur une maladie cérébrale dévastatrice
La maladie de Huntington est une affection cérébrale rare mais dévastatrice qui prive peu à peu les personnes de leurs capacités motrices, cognitives et de leur autonomie. Les traitements actuels peuvent soulager certains symptômes, mais ils n’arrêtent ni ne renversent la maladie. Cette étude explore une nouvelle voie pilotée par ordinateur pour rechercher des thérapies, visant un composé naturel unique capable d’agir simultanément sur plusieurs points faibles du processus pathologique — une approche susceptible d’être plus efficace que des médicaments ciblant une seule cible.
Pourquoi la maladie de Huntington est si difficile à traiter
La maladie de Huntington est provoquée par un gène défectueux qui entraîne une dégradation progressive des neurones, en général à partir de l’âge moyen. Au début, les personnes peuvent remarquer des changements d’humeur discrets, de petits mouvements involontaires ou des difficultés légères de planification et d’attention. Sur 10 à 12 ans, cela peut évoluer vers des troubles moteurs sévères, la perte de la parole, une démence et une dépendance totale aux aidants. Les chercheurs savent que de nombreux mécanismes cellulaires sont perturbés dans la Huntington — la production d’énergie faiblit, des protéines toxiques s’agglomèrent et les signaux chimiques entre cellules deviennent délétères. Parce que tant de voies sont altérées en même temps, une stratégie « une protéine, un médicament » a eu du mal à produire des avancées significatives.
Trois points de pression critiques dans le cerveau
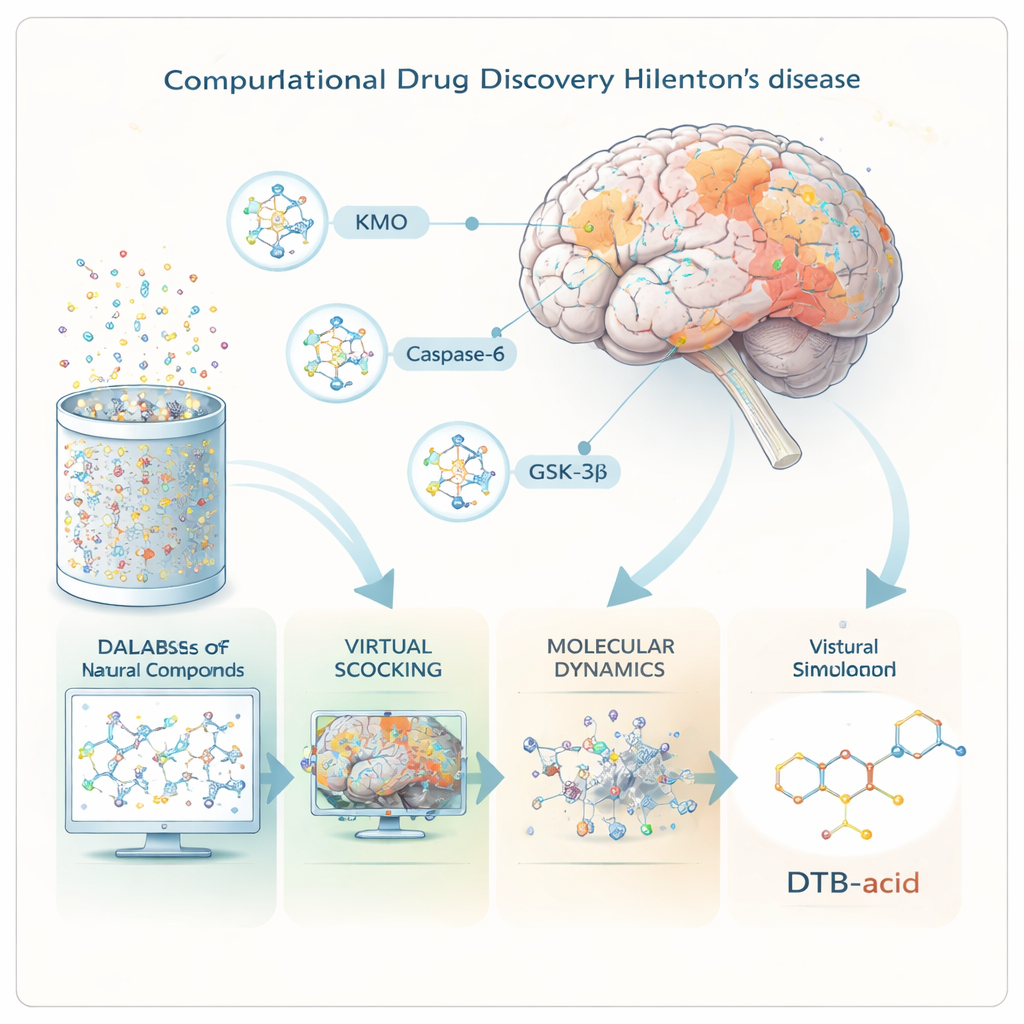
Les chercheurs se sont concentrés sur trois protéines qui occupent des points de contrôle clés dans la maladie de Huntington. La première, KMO, oriente la dégradation de l’acide aminé tryptophane vers des sous‑produits soit toxiques soit protecteurs ; quand cet équilibre penche vers les toxines, les neurones en pâtissent. La seconde, la caspase‑6, coupe la protéine huntingtine mutante en fragments plus petits et très toxiques qui s’accumulent tôt dans la maladie. La troisième, GSK‑3β, est une enzyme de signalisation liée à l’apparition d’agrégats protéiques anormaux et à la mort cellulaire dans plusieurs pathologies cérébrales. En trouvant une molécule capable de réduire l’activité néfaste des trois cibles à la fois, l’équipe espérait concevoir une thérapie mieux adaptée à la complexité de la maladie.
Criblage de la bibliothèque de la nature avec des super‑ordinateurs
Plutôt que de mélanger des produits chimiques en éprouvettes, les scientifiques ont travaillé entièrement « in silico », en utilisant des logiciels avancés pour modéliser le comportement des molécules. Ils ont commencé par plus de 695 000 composés naturels tirés d’une base de données publique, préparant chacun en forme tridimensionnelle. Des outils de criblage virtuel puissants ont ensuite prédit quels composés étaient susceptibles de traverser la barrière hémato‑encéphalique, de se comporter comme de vrais médicaments dans l’organisme et d’éviter des problèmes de sécurité majeurs. Environ 60 000 seulement ont passé ces filtres et ont été testés, sur ordinateur, pour évaluer leur affinité potentielle pour les poches de liaison des trois protéines cibles.
Une molécule remarquable : l’acide DTB
De cette recherche immense, une molécule — appelée acide DTB, un alcaloïde naturel apparenté à l’acide matrine — est sortie du lot. Des études de docking détaillées ont montré que l’acide DTB pouvait établir des contacts forts et bien positionnés à l’intérieur des trois protéines. Ensuite, l’équipe a effectué de longues simulations de dynamique moléculaire, qui imitent le mouvement des atomes en solution au fil du temps, pour vérifier si le composé restait en place plutôt que de se dissocier. Sur 100 milliardièmes de seconde de mouvement simulé, les complexes protéine‑médicament sont demeurés stables. Des calculs énergétiques supplémentaires ont suggéré que la liaison à KMO était particulièrement forte, tandis qu’une analyse distincte des molécules d’eau dans les sites de liaison indiquait que les interactions avec GSK‑3β étaient également favorables sur le plan thermodynamique.
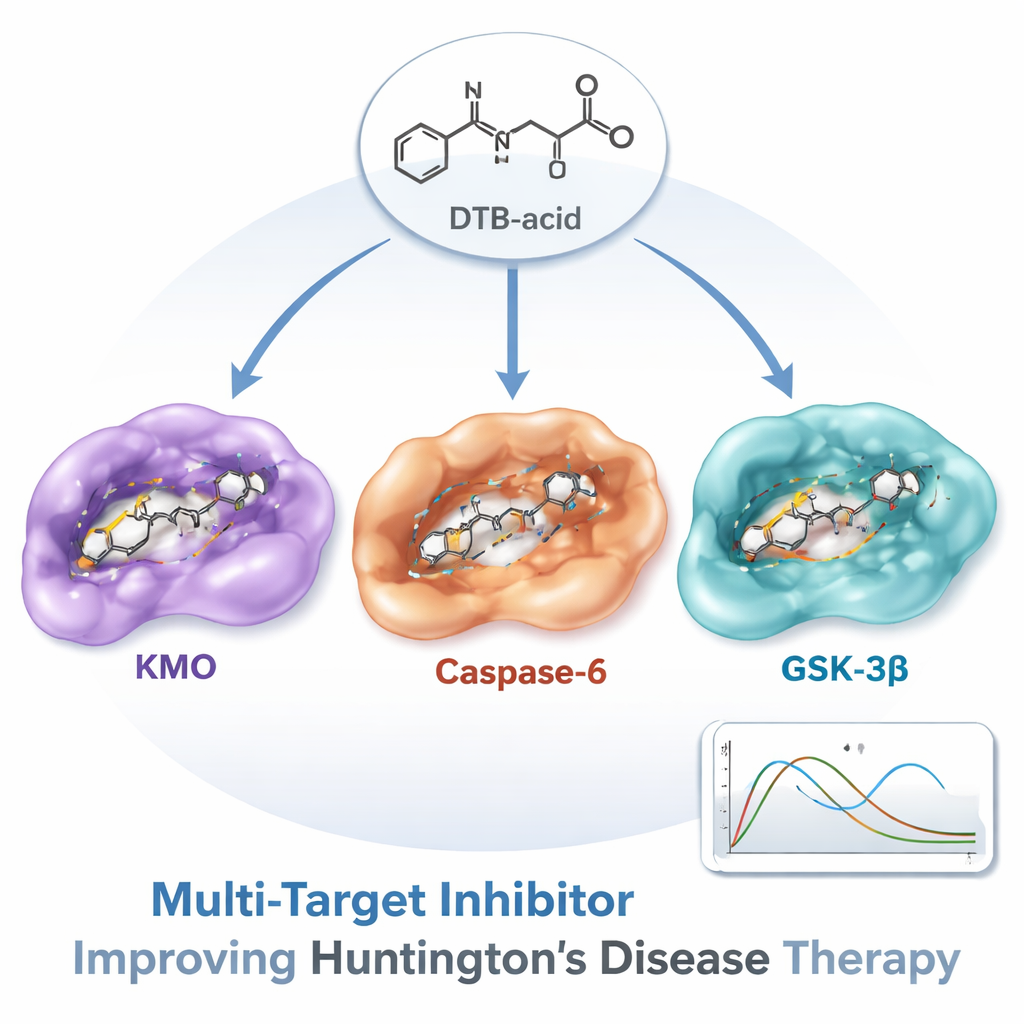
Du « hit » informatique au futur médicament
Évidemment, une molécule prometteuse à l’écran n’est qu’une première étape. Les auteurs insistent sur le fait que l’acide DTB doit encore être testé en cellules et chez l’animal pour confirmer qu’il atteint le cerveau, qu’il atteint ses cibles prévues et qu’il protège réellement les neurones sans effets indésirables nocifs. Même ainsi, ce travail démontre une voie puissante et efficace pour découvrir des médicaments multi‑cibles pour des maladies cérébrales complexes. Pour le grand public, le message clé est que, plutôt que de traiter la maladie de Huntington par une série de médicaments séparés et ciblés de façon étroite, il pourrait être possible de concevoir un seul composé soigneusement ajusté comme l’acide DTB qui s’attaque simultanément à plusieurs causes de dommage — offrant un nouvel espoir pour ralentir ou modifier le cours de cette maladie implacable.
Citation: Zheng, B., Banday, M., Gangwar, S. et al. In silico discovery of natural compound-derived multi-target inhibitor for Huntington’s disease therapy. Sci Rep 16, 7716 (2026). https://doi.org/10.1038/s41598-026-38430-w
Mots-clés: Maladie de Huntington, médicament multi‑cible, découverte de médicaments par calcul, composés naturels, neurodégénérescence