Clear Sky Science · fr
Dépistage intégré de plusieurs jeux de données pour prédire le pronostic et identifier des cibles génétiques d’immunothérapie chez les patients atteints de carcinome hépatocellulaire
Pourquoi c’est important pour les personnes atteintes d’un cancer du foie
Le carcinome hépatocellulaire, la forme la plus fréquente de cancer primitif du foie, cause la mort de plusieurs centaines de milliers de personnes chaque année. De nombreux patients au même stade de la maladie réagissent très différemment aux traitements, en particulier aux immunothérapies modernes qui cherchent à libérer le système immunitaire de l’organisme. Cette étude pose une question simple mais cruciale : peut‑on lire l’activité génique d’une tumeur comme une empreinte digitale pour prédire qui aura un mauvais devenir, qui répondra aux médicaments à base d’immunothérapie, et quels gènes pourraient constituer les meilleures cibles thérapeutiques ?
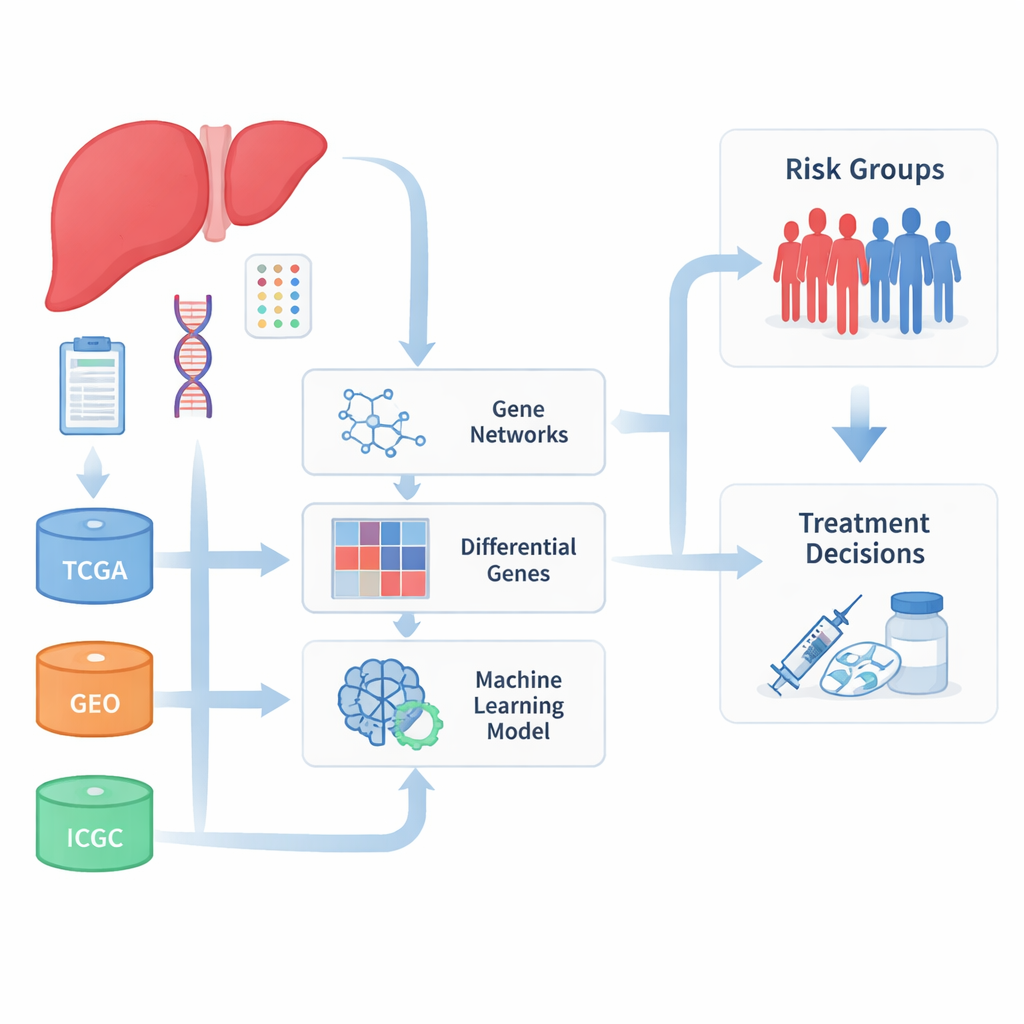
Rassembler de nombreux jeux de données
Les chercheurs ont commencé par regrouper de larges collections d’échantillons de cancer du foie issues de plusieurs bases de données internationales qui stockent l’activité génique tumorale et les résultats cliniques. En combinant les données de The Cancer Genome Atlas, de l’International Cancer Genome Consortium et de multiples études du Gene Expression Omnibus, ils ont constitué un ensemble de patients beaucoup plus vaste et diversifié que celui dont pourrait disposer un seul hôpital ou projet. Comme ces jeux de données ont été produits dans des laboratoires et par des méthodes différentes, l’équipe a d’abord consacré des efforts substantiels à corriger les différences techniques afin que de vrais signaux biologiques, plutôt que du bruit de laboratoire, orientent leurs résultats.
Identifier des motifs géniques liés au pronostic
Avec les données nettoyées en main, l’équipe a recherché des groupes de gènes qui avaient tendance à s’activer ou se désactiver ensemble et qui étaient aussi corrélés au devenir des patients. En utilisant une approche de type réseau, ils ont regroupé des milliers de gènes en modules puis se sont concentrés sur ceux les plus fortement liés au comportement tumoral et à la survie des patients. Ils ont aussi comparé les tumeurs aux tissus non tumoraux pour repérer les gènes nettement plus ou moins actifs dans le cancer. Le recoupement de ces deux angles a donné un ensemble de 93 gènes à la fois altérés dans le cancer du foie et étroitement associés à des caractéristiques clés de la maladie, dont beaucoup participent au métabolisme des médicaments et à la gestion des substances toxiques par le foie.
Construire un score de risque à dix gènes
Pour transformer ces listes de gènes en un outil potentiellement utilisable par les cliniciens, les auteurs ont eu recours à l’apprentissage automatique. Ils ont testé plus d’une centaine de combinaisons d’algorithmes de sélection de variables et de prédiction de survie, les évaluant sur leur capacité à séparer précisément les patients en groupes à meilleur et moins bon pronostic sur plusieurs cohortes indépendantes. De cette recherche étendue, ils ont distillé une signature compacte de dix gènes qui formaient ensemble un score de risque. Les patients ayant des scores élevés présentaient systématiquement des survies globale, sans maladie et sans progression plus courtes, tant dans les jeux de données principaux que dans des cohorts de validation externes. Parmi ces gènes, TYMS s’est distingué comme un fort indicateur de mauvais pronostic, tandis qu’APOL3 et FBXO2 étaient associés à des issues plus favorables.
Indices provenant du voisinage immunitaire de la tumeur
L’étude est allée au‑delà de la prédiction pour interroger le pourquoi de l’importance de ces gènes. En utilisant plusieurs outils computationnels, l’équipe a estimé quels types de cellules immunitaires étaient présents dans chaque tumeur et dans quelle mesure le score à dix gènes était lié à ce paysage immunitaire. Les tumeurs à haut risque présentaient des profils immunitaires et des altérations géniques associés à un plus grand nombre de mutations et à des signes d’échappement immunitaire, y compris des liens avec des molécules de point de contrôle bien connues comme PD‑1 et CTLA‑4. Ils ont également examiné les profils de mutations réels et constaté que les tumeurs à haut risque comportaient plus fréquemment des altérations dans des oncogènes classiques comme TP53. Enfin, des analyses sanguines chez des patients et des volontaires sains ont confirmé que TYMS était élevé et que FBXO2 était diminué chez les personnes atteintes d’un cancer du foie, ce qui soutient l’idée que ces gènes sont biologiquement actifs dans la maladie et pas seulement des artefacts statistiques.
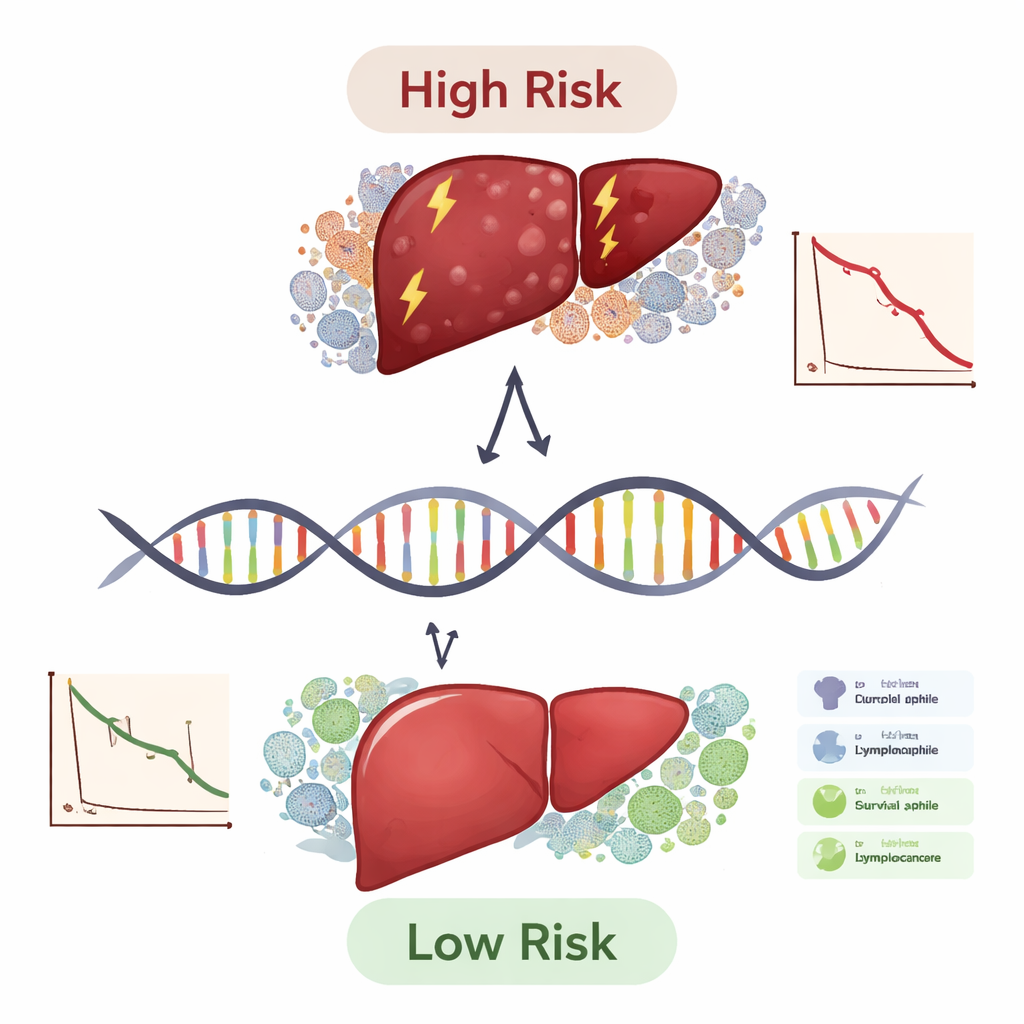
Ce que cela signifie pour les patients et les médecins
En termes pratiques, ce travail propose une feuille de route pour utiliser un petit panel de gènes afin de classer les patients atteints de cancer du foie par niveau de risque et d’indiquer qui pourrait tirer le plus de bénéfice des traitements à base d’immunothérapie. Le score à dix gènes n’est pas encore un test prêt pour la clinique, mais il a surpassé les systèmes de stadification standard seuls et est resté utile à travers différents sous‑groupes de patients. Tout comme les bilans lipidiques orientent la prévention des maladies cardiovasculaires, un panel génétique de ce type pourrait, un jour, aider les oncologues à choisir des thérapies plus agressives pour les patients à haut risque, épargner aux patients à faible risque des effets indésirables inutiles, et orienter les développeurs de médicaments vers de nouvelles cibles comme TYMS, APOL3 et FBXO2. Des études prospectives plus larges et des expériences en laboratoire seront nécessaires, mais cette analyse intégrée marque un pas important vers des soins du cancer du foie plus personnalisés et fondés sur la biologie.
Citation: Zhou, L., Zhang, W., Liu, Z. et al. Integrated multi-dataset screening to predict prognosis and identify immunotherapy gene targets in hepatocellular carcinoma patients. Sci Rep 16, 7014 (2026). https://doi.org/10.1038/s41598-026-38424-8
Mots-clés: carcinome hépatocellulaire, signature génique, immunothérapie, pronostic, microenvironnement tumoral