Clear Sky Science · fr
La signalisation CNOT2 / c-Myc / STAT3 est impliquée de façon critique dans l’apoptose médiée par la glycolyse induite par le benzylisothiocyanate dans le carcinome hépatocellulaire
Un ingrédient anticancer dans votre assiette
Le benzylisothiocyanate, ou BITC, est une substance naturelle présente dans des légumes familiers comme le brocoli, le chou et le kale. Si les médecins savent depuis longtemps que les personnes consommant davantage de ces aliments présentent des taux de cancer plus faibles, les mécanismes par lesquels des composés végétaux spécifiques ralentissent ou tuent les cellules cancéreuses restent encore à élucider. Cette étude examine l’effet du BITC sur des cellules de cancer du foie en laboratoire et met en lumière un lien surprenant entre la façon dont les cellules cancéreuses exploitent le sucre et la manière dont elles sont poussées à l’autodestruction.
Pourquoi le cancer du foie a besoin de meilleures options
Le cancer du foie est l’un des cancers les plus mortels dans le monde, et le carcinome hépatocellulaire en est la forme la plus fréquente. Même avec la chirurgie, la chimiothérapie et les traitements ciblés, de nombreuses tumeurs récidivent ou cessent de répondre aux thérapies. Une raison tient au fait que les cellules cancéreuses réorganisent leur utilisation de l’énergie : au lieu de dépendre principalement de l’oxygène dans leurs centrales (mitochondries), elles brûlent de grandes quantités de sucre très rapidement dans un processus souvent appelé « effet Warburg ». Cette utilisation déformée du sucre aide les cellules cancéreuses à croître plus vite et à résister à la mort. Trouver des moyens sûrs d’interrompre cet apport énergétique, en particulier à l’aide de molécules dérivées d’aliments, constitue une stratégie attrayante.
Tester un composé de légumes sur des cellules de cancer du foie
Les chercheurs ont traité deux lignées de cellules humaines de cancer du foie, SK-Hep1 et Huh7, avec des doses croissantes de BITC. À mesure que la dose augmentait, moins de cellules survivaient, montrant que le BITC est toxique pour ces cellules dans ces conditions. En examinant plus en détail ce qui se passait à l’intérieur des cellules, ils ont observé des caractéristiques classiques de la mort cellulaire programmée, ou apoptose. Des protéines clés qui existent normalement sous une forme « inactive » avant d’être clivées pendant l’apoptose, comme PARP et la caspase‑3, diminuaient dans leurs formes intactes, ou « pro‑ ». Des tests en cytométrie en flux ont aussi montré davantage de cellules dans la fraction sub‑G1 du cycle cellulaire et plus de cellules positives pour l’Annexin V, deux signes indiquant que les cellules cancéreuses subissaient activement l’apoptose plutôt qu’un simple dommage.
Couper l’appétit sucré du cancer
L’équipe a ensuite exploré si le BITC affectait l’effet Warburg. Ils ont mesuré les protéines qui aident les cellules cancéreuses à consommer du sucre et à le transformer en énergie et en lactate — spécifiquement HK2, PKM2 et LDH. Le traitement par BITC a abaissé les niveaux de ces trois protéines dans les deux lignées et a réduit la quantité de lactate libérée par les cellules ainsi que la consommation de glucose dans le milieu de culture. En d’autres termes, le BITC rendait les cellules de cancer du foie moins capables de faire fonctionner leur machinerie de glycolyse à grande vitesse. Lorsque les scientifiques ont ajouté du pyruvate, un produit en aval de la dégradation du sucre qui peut encore alimenter le métabolisme cellulaire, beaucoup des effets du BITC ont été renversés : les cellules ont retrouvé des niveaux plus élevés de PARP, de caspase‑3 et des enzymes de la glycolyse. Ce sauvetage suggère que l’altération du traitement du sucre est une part clé du mécanisme par lequel le BITC déclenche la mort cellulaire.
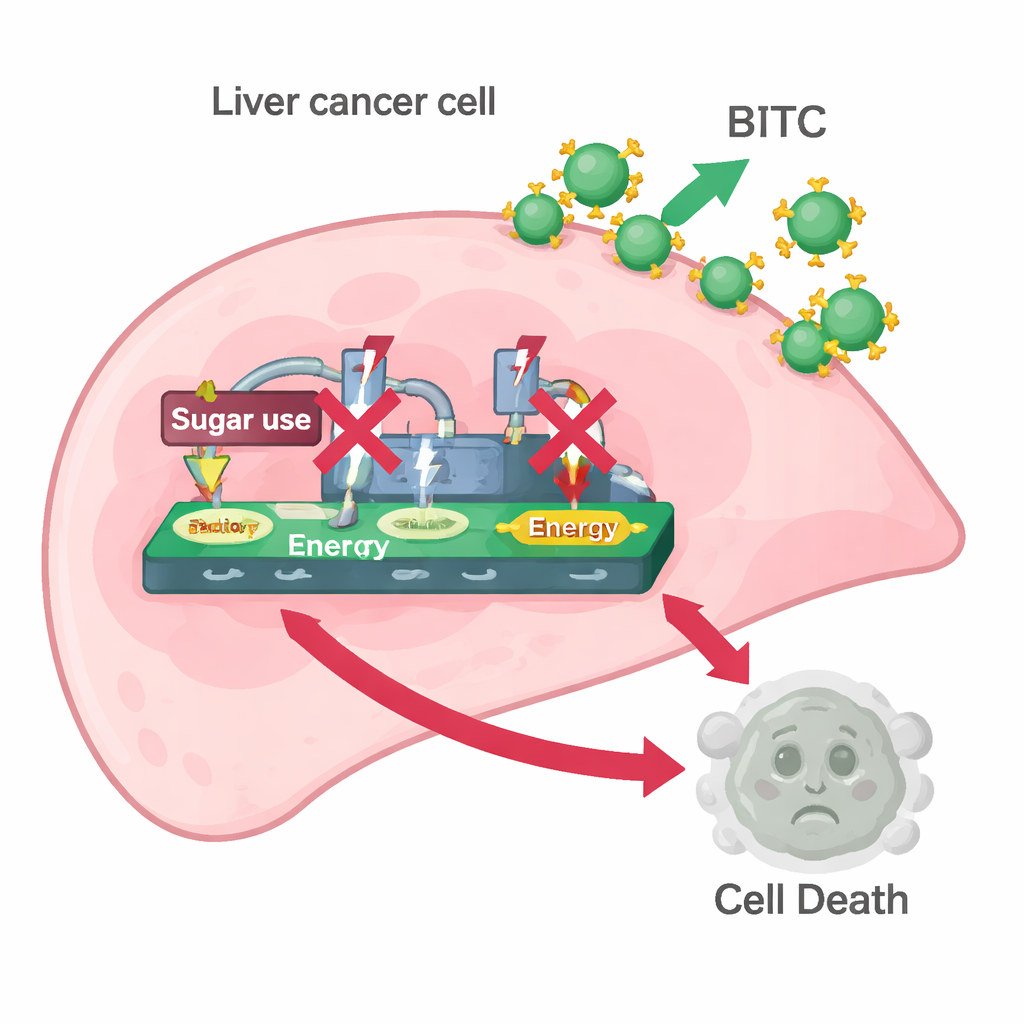
Démêler les commutateurs de contrôle à l’intérieur de la cellule
Pour comprendre des couches de contrôle plus profondes, les chercheurs se sont concentrés sur un trio de signalisation : CNOT2, c‑Myc et STAT3. Ces protéines favorisent la croissance, la survie et la réorganisation métabolique dans de nombreuses tumeurs. Les données de patients atteints de cancer du foie montraient que CNOT2 tend à être plus élevé chez les personnes ayant de moins bons résultats cliniques. En laboratoire, le traitement par BITC réduisait la forme active phosphorylée de STAT3, son activateur en amont JAK1, la protéine promotrice de croissance c‑Myc, et CNOT2 lui‑même. L’utilisation d’outils génétiques pour diminuer les niveaux de CNOT2 ou de STAT3 renforçait l’effet cytotoxique du BITC, abaissant encore PARP et la caspase‑3. Des expériences d’interaction protéine‑protéine ont révélé que le BITC perturbait également les associations physiques entre CNOT2 et STAT3 et entre CNOT2 et c‑Myc. Lorsque CNOT2 ou c‑Myc étaient artificiellement surexprimés, le BITC perdait une grande partie de sa capacité à abaisser les enzymes de la glycolyse et à déclencher l’apoptose, soulignant que cet axe de signalisation agit comme un commutateur maître liant le métabolisme du sucre et la survie.
Ce que cela pourrait signifier pour les thérapies futures
Pris ensemble, les résultats dessinent un tableau cohérent : le BITC attaque les cellules du cancer du foie en coupant leur ligne d’alimentation préférentielle à base de sucre et en activant des interrupteurs de mort cellulaire dépendant de l’axe CNOT2/c‑Myc/STAT3. En bloquant à la fois les signaux de croissance et l’utilisation du sucre, le BITC pousse les cellules cancéreuses au‑delà d’un point de basculement métabolique vers l’apoptose. Ces résultats proviennent d’expériences en culture cellulaire, et non de patients, et seules deux lignées de cancer du foie ont été étudiées, si bien que de nombreux travaux supplémentaires chez l’animal et chez l’humain sont nécessaires. Néanmoins, la recherche renforce l’idée que certains composés issus d’aliments quotidiens pourraient être affinés ou combinés avec d’autres traitements pour affamer plus précisément les tumeurs hépatiques tout en favorisant leur autodestruction.
Citation: Koh, W., Park, SY., Kim, B. et al. CNOT2 /c-Myc/STAT3 signaling is critically involved in glycolysis mediated apoptosis of benzyl isothiocyanate in hepatocellular carcinoma. Sci Rep 16, 7000 (2026). https://doi.org/10.1038/s41598-026-38416-8
Mots-clés: cancer du foie, benzylisothiocyanate, métabolisme du cancer, apoptose, légumes crucifères