Clear Sky Science · fr
Un classifieur d’ensemble en apprentissage automatique pour le diagnostic de la maladie de Parkinson utilisant l’angiographie par tomographie en cohérence optique
Pourquoi les yeux peuvent révéler une maladie cérébrale cachée
La maladie de Parkinson est généralement diagnostiquée seulement après l’apparition de tremblements, de raideur ou d’un ralentissement des mouvements — des signes indiquant que le cerveau évolue déjà depuis des années. Cette étude explore un raccourci inattendu : observer les tout petits vaisseaux sanguins au fond de l’œil à l’aide d’un examen d’imagerie indolore, puis utiliser l’intelligence artificielle pour signaler des personnes susceptibles d’avoir la maladie de Parkinson plus tôt et de façon plus objective que ne le permettent les bilans actuels.
Regarder le cerveau à travers l’œil
Le tissu photosensible au fond de l’œil, la rétine, est essentiellement une partie accessible du cerveau. Elle partage des nerfs et des vaisseaux sanguins similaires, mais peut être examinée de façon non invasive en consultation. Les chercheurs ont utilisé une technique appelée angiographie par tomographie en cohérence optique, ou OCTA, qui produit des cartographies détaillées et sans colorant de la circulation rétinienne. Parce que la maladie de Parkinson a été associée à des altérations des petits vaisseaux ailleurs dans le corps, l’équipe s’est demandé si des changements subtils dans ces réseaux rétiniens pourraient servir de « fenêtre » sur la maladie à un stade précoce.
Transformer des scans oculaires en chiffres
Dans une étude rétrospective, l’équipe a recueilli des scans OCTA de 53 personnes atteintes de Parkinson et de 39 volontaires sains appariés par âge. Ils se sont concentrés sur deux couches de vaisseaux rétiniens : une couche superficielle proche de la surface et une couche plus profonde en dessous. Pour chaque couche, ils ont segmenté automatiquement la zone avasculaire fovéale centrale — la petite dépression sans vaisseaux sanguins nécessaire à la vision nette — ainsi que les capillaires environnants. Ils ont ensuite converti chaque image en 22 mesures numériques. Certaines décrivaient la forme de la zone fovéale, par exemple à quel point son bord était rond, lisse ou irrégulier. D’autres capturaient la densité des vaisseaux sanguins dans l’ensemble et dans un anneau autour de la fovéa. Ensemble, ces mesures quantifiaient la santé microvasculaire avec beaucoup plus de nuances que ne pourrait le juger l’œil humain. 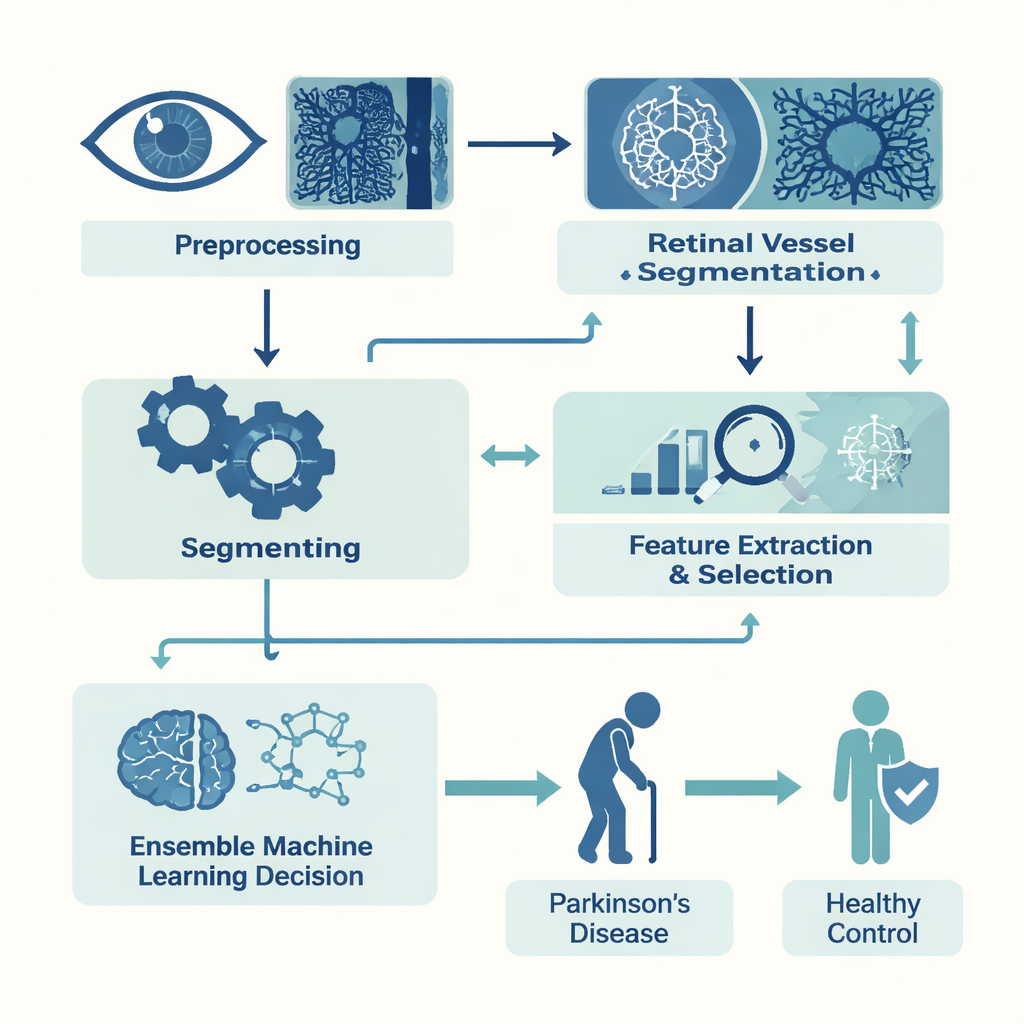
Apprendre à l’IA à repérer les motifs de Parkinson
Avec ces mesures en main, les chercheurs ont construit des modèles informatiques pour distinguer les scans de Parkinson de ceux des sujets sains. Parce que leur jeu de données était modeste, ils ont d’abord utilisé des techniques de sélection de caractéristiques pour réduire les 22 mesures à un sous-ensemble le plus informatif, diminuant ainsi le bruit et le surapprentissage. Ils ont ensuite entraîné plusieurs algorithmes d’apprentissage automatique courants, y compris des méthodes basées sur des arbres de décision et un classifieur k-plus proches voisins. Enfin, ils ont combiné les trois meilleurs performeurs — XGBoost, Random Forest et K-Nearest Neighbors — en un « ensemble » pondéré, de sorte que le vote de chaque modèle compte en proportion de ses performances habituelles.
Ce que les modèles ont trouvé dans la rétine
Comparées aux volontaires sains, les personnes atteintes de Parkinson présentaient des signes clairs d’altération de la microcirculation rétinienne. Les mesures de densité vasculaire étaient plus faibles, et la zone fovéale centrale avait tendance à être moins régulière — moins ronde, moins lisse et moins compacte — dans les couches superficielles comme profondes des vaisseaux. Testé sur des données non vues auparavant, le modèle d’ensemble a correctement classé environ trois yeux sur quatre au total. Fait notable, il a atteint une sensibilité de 90 % : il a correctement identifié neuf cas sur dix de Parkinson. La spécificité était plus modeste, un peu plus de la moitié, ce qui signifie que certains individus sains ont été incorrectement signalés comme malades. L’aire sous la courbe ROC, un résumé courant de la performance diagnostique, était de 0,75, indiquant une discrimination utile mais non définitive. 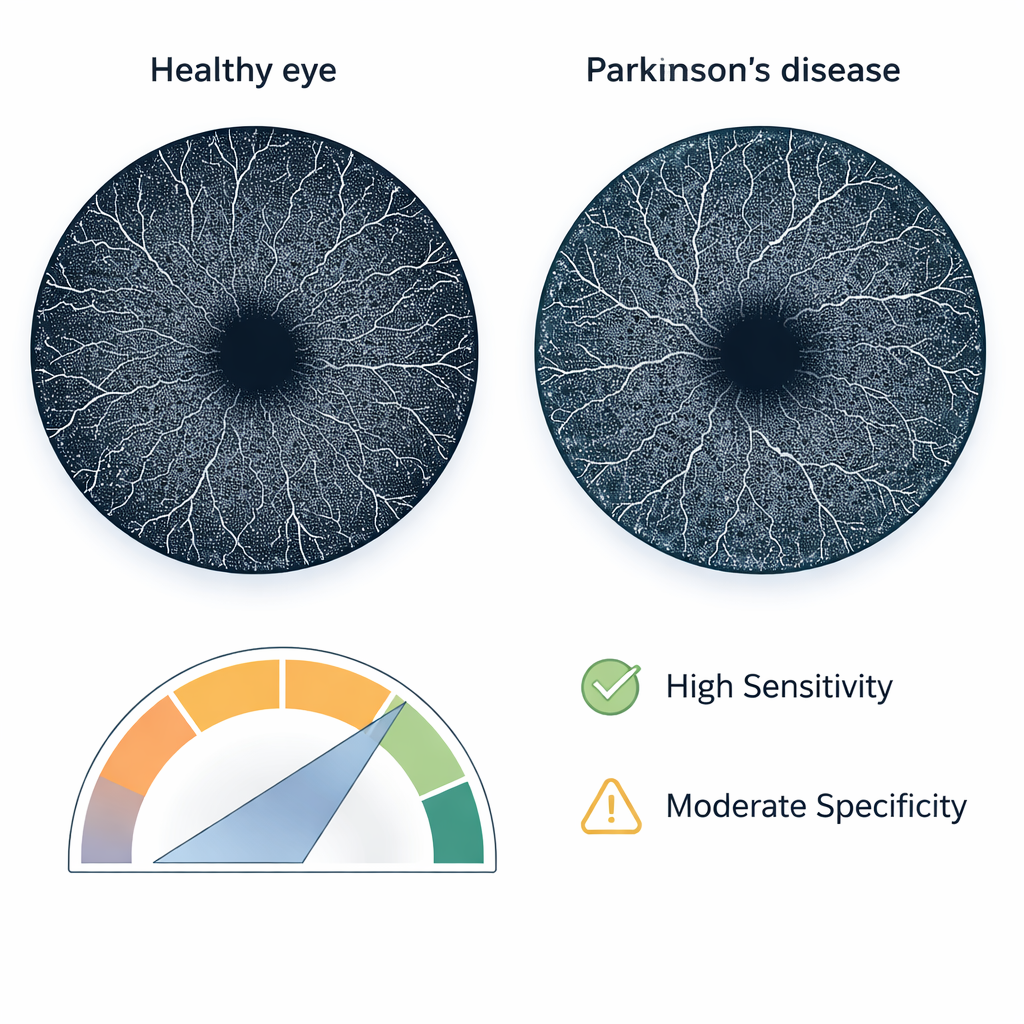
De l’algorithme à la clinique
Pour dépasser le stade théorique, l’équipe a intégré ses méthodes dans un outil logiciel prototype appelé Parkinson’s Disease Artificial Intelligence (PDAI). Via une interface graphique simple, les cliniciens peuvent charger des scans OCTA, revoir les vaisseaux sanguins et la zone fovéale centrale tracés automatiquement, visualiser les principales caractéristiques numériques et obtenir une prédiction instantanée indiquant si un scan ressemble à ceux de patients atteints de Parkinson. Parce que le système repose sur des mesures définies manuellement et clairement plutôt que sur une « boîte noire » opaque, les contributions à chaque décision sont plus faciles à interpréter par les cliniciens et potentiellement à relier à la biologie sous-jacente.
Ce que cela signifie pour les patients
Ce travail n’offre pas encore un test autonome pour la maladie de Parkinson, mais il montre qu’un scan oculaire rapide et non invasif, analysé avec des méthodes d’apprentissage automatique soigneusement conçues, peut détecter des changements liés à la maladie avec une sensibilité élevée. En pratique, un tel outil pourrait un jour servir d’aide au dépistage — aidant ophtalmologistes et neurologues à décider qui devrait être surveillé de plus près ou orienté pour une évaluation complémentaire bien avant l’apparition de symptômes invalidants. Des études plus larges, multicentriques, sont encore nécessaires, mais l’étude suggère que les yeux peuvent effectivement fournir un signal d’alerte précoce pratique pour la maladie de Parkinson.
Citation: Hasanshahi, M., Mehdizadeh, A., Mahmoudi, T. et al. An ensemble machine learning classifier for Parkinson’s disease diagnosis using optical coherence tomography angiography. Sci Rep 16, 7297 (2026). https://doi.org/10.1038/s41598-026-38407-9
Mots-clés: Maladie de Parkinson, imagerie rétinienne, OCTA, apprentissage automatique, diagnostic précoce