Clear Sky Science · fr
Analyse algorithmique de la structure des tumeurs odontogéniques mixtes
Pourquoi de petites tumeurs de la mâchoire comptent
La plupart d’entre nous ne pensent à nos dents que lorsqu’elles font mal ou nécessitent un plombage, mais les tissus qui forment les dents peuvent parfois donner naissance à des tumeurs rares. Ces excroissances, appelées tumeurs odontogéniques, sont peu fréquentes mais importantes car elles peuvent endommager les mâchoires et être difficiles à diagnostiquer au microscope. Cette étude se demande si des algorithmes informatiques modernes peuvent mesurer l’architecture de ces tumeurs avec une telle précision qu’ils aident les anatomopathologistes à distinguer des lésions similaires et à mieux comprendre leur comportement.
Des croissances rares qui imitent les dents en formation
Les tumeurs odontogéniques ne surviennent que dans les régions de la mâchoire où se forment les dents. L’équipe s’est concentrée sur un petit groupe appelé tumeurs odontogéniques mixtes, qui contiennent à la fois la couche cellulaire donnant normalement naissance à l’émail (épithélium) et le tissu de soutien formant la dent (ectomésenchyme). Dans ce groupe, trois lésions — la tumeur odontogénique primordiale (POT), le fibrome améloblastique (AF) et l’odontome en développement (DO) — peuvent se ressembler de façon remarquable entre elles et avec les bourgeons dentaires normaux, les structures précoces à l’origine des dents. La POT est particulièrement nouvelle pour la communauté scientifique, ayant été reconnue formellement par l’Organisation mondiale de la santé seulement en 2017, et reste si rare que chaque cas supplémentaire est pertinent pour affiner sa définition.
Transformer des lames de microscope en cartes mesurables
Pour dépasser les limites de l’examen visuel des lames, les chercheurs ont numérisé des échantillons de biopsie provenant de 15 tumeurs odontogéniques mixtes (cinq de chaque : POT, AF et DO) et de cinq bourgeons dentaires normaux. Après la coloration habituelle, ils ont scanné les lames à fort grossissement et utilisé un logiciel d’analyse d’image pour localiser chaque noyau cellulaire. Ensuite, des outils mathématiques connus sous le nom de transformations watershed ont défini une sorte de « zone d’influence » autour de chaque noyau, créant des milliers de « cellules virtuelles » dont la taille et la forme pouvaient être mesurées automatiquement. En empilant et en alignant les images, l’équipe a aussi étudié la densité de noyaux à différentes profondeurs sous les couches superficielles du tissu.
Ce que les algorithmes ont vu à l’intérieur des tumeurs
Dans la POT, les cartes de densité dérivées par ordinateur ont confirmé un encombrement marqué des cellules juste sous la couche superficielle de l’épithélium, avec des noyaux les plus serrés dans le tiers supérieur du tissu et s’éclaircissant vers le centre. Ce schéma — appelé condensation sous‑épithéliale — était présent dans la plupart des échantillons de POT mais absent chez une minorité dépourvue de cette bande dense. Les noyaux du tissu de soutien étaient légèrement plus grands que ceux de l’épithélium, mais les deux compartiments présentaient des formes similarly arrondies. En comparant les cellules virtuelles entre toutes les entités, l’équipe a constaté que les cellules virtuelles épithéliales étaient toujours les plus petites, reflet de leur densité d’empilement plus élevée, tandis que les régions plus profondes contenaient des cellules virtuelles beaucoup plus grandes. L’odontome en développement montrait la plus grande dispersion des surfaces de cellules virtuelles épithéliales, avec des valeurs généralement plus élevées que dans les autres lésions, tandis que le fibrome améloblastique avait tendance à présenter les plus petites.
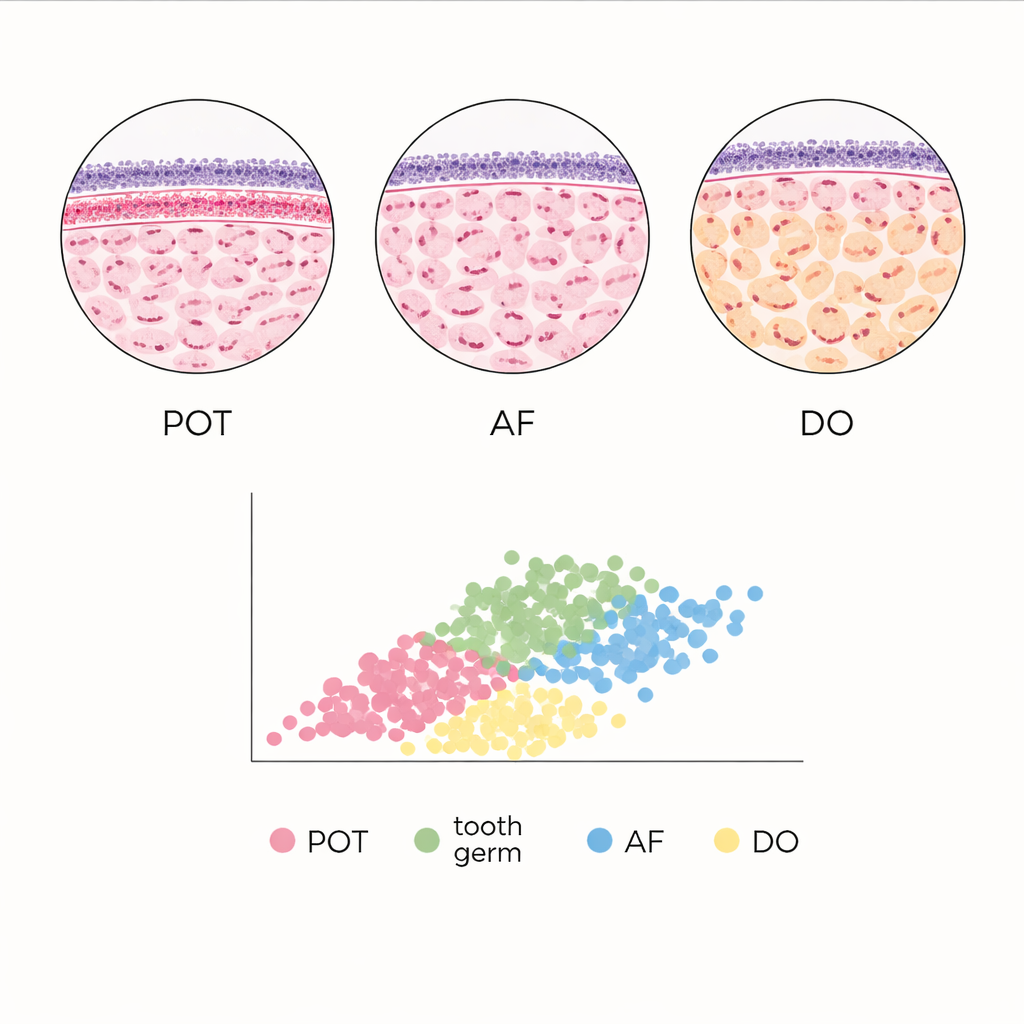
Le développement normal de la dent comme référence
Pour situer ces tumeurs, les auteurs les ont comparées à des bourgeons dentaires normaux capturés aux stades précoces de « chapeau » et de « cloche » du développement. Dans certaines régions, l’architecture de la POT sans bande sous‑épithéliale condensée ressemblait fortement à celle des bourgeons dentaires : les surfaces moyennes des cellules virtuelles épithéliales n’étaient pas statistiquement différentes. En revanche, l’odontome en développement et le fibrome améloblastique montraient des signatures quantitatives distinctes, incluant moins de couches de cellules virtuelles et des distributions de surfaces cellulaires épithéliales différentes, malgré une imitation parfois fidèle du développement dentaire au microscope. Ces différences mesurables suggèrent que, même lorsque les tissus se ressemblent à l’œil nu, leur organisation spatiale sous‑jacente peut révéler des indices diagnostiques subtils.
Ce que cela signifie pour les patients et les pathologistes
L’étude montre que l’analyse « cellules virtuelles » pilotée par algorithme peut saisir des motifs architecturaux qui soutiennent l’idée de la tumeur odontogénique primordiale en tant que type distinct de lésion de la mâchoire, l’une qui dans certaines zones se comporte comme un bourgeon dentaire précoce et activement interactif. Dans le même temps, elle quantifie la façon dont d’autres tumeurs odontogéniques mixtes diffèrent par la taille et le feuilletage de leurs compartiments épithéliaux. Pour les patients, cela ne change pas encore la prise en charge, mais cela ouvre la voie à un futur où des mesures assistées par ordinateur complèteraient la pathologie traditionnelle, en particulier dans des biopsies petites ou ambiguës. Les auteurs soulignent que leur jeu de données reste limité et que des études multicentriques plus vastes sont nécessaires avant que de telles méthodes puissent guider le diagnostic de façon routinière, mais le travail illustre comment les outils numériques peuvent transformer les impressions qualitatives d’un pathologiste en chiffres reproductibles.
Citation: Pereira-Prado, V., Sicco, E., Silveira, F.M. et al. Algorithmic analysis of the structure of mixed odontogenic tumors. Sci Rep 16, 7538 (2026). https://doi.org/10.1038/s41598-026-38399-6
Mots-clés: tumeurs odontogéniques, tumeur odontogénique primordiale, pathologie numérique, analyse cellulaire virtuelle, développement dentaire