Clear Sky Science · fr
Modèle pronostique basé sur l’apprentissage automatique des gènes liés à la « stemness » et à l’angiogenèse pour prédire le pronostic et l’infiltration immunitaire chez les patients atteints de CHC
Pourquoi cette recherche est importante pour les patients atteints de cancer du foie
Le carcinome hépatocellulaire, la forme la plus fréquente de cancer du foie, récidive ou se dissémine souvent même après traitement. Cette étude explore les raisons de ces échecs et comment les cliniciens pourraient mieux prédire quels patients présentent le risque le plus élevé. En combinant d’importantes bases de données génétiques et des méthodes modernes d’apprentissage automatique, les chercheurs ont développé un outil qui relie deux caractéristiques majeures du cancer — la « stemness » (des cellules qui se comportent comme des graines persistantes) et la néovascularisation — aux chances de survie des patients et à leur réponse probable aux thérapies immunitaires.
Les « cellules‑graine » du cancer et la néovascularisation
De nombreuses tumeurs contiennent un petit sous‑groupe de cellules qui agissent comme des graines. Ces cellules souches cancéreuses peuvent se renouveler, résister aux traitements et relancer la tumeur après chirurgie ou chimiothérapie. Parallèlement, les tumeurs doivent former de nouveaux vaisseaux sanguins pour apporter oxygène et nutriments et ainsi croître et se disséminer. Des travaux récents montrent que ces deux processus sont interdépendants : les cellules de type stem envoient des signaux qui favorisent la croissance vasculaire, tandis qu’un microenvironnement riche en vaisseaux aide ces cellules‑graine à survivre. Comprendre et cibler conjointement ce partenariat est particulièrement important dans le cancer du foie, qui est à la fois très vascularisé et sujet aux récidives.
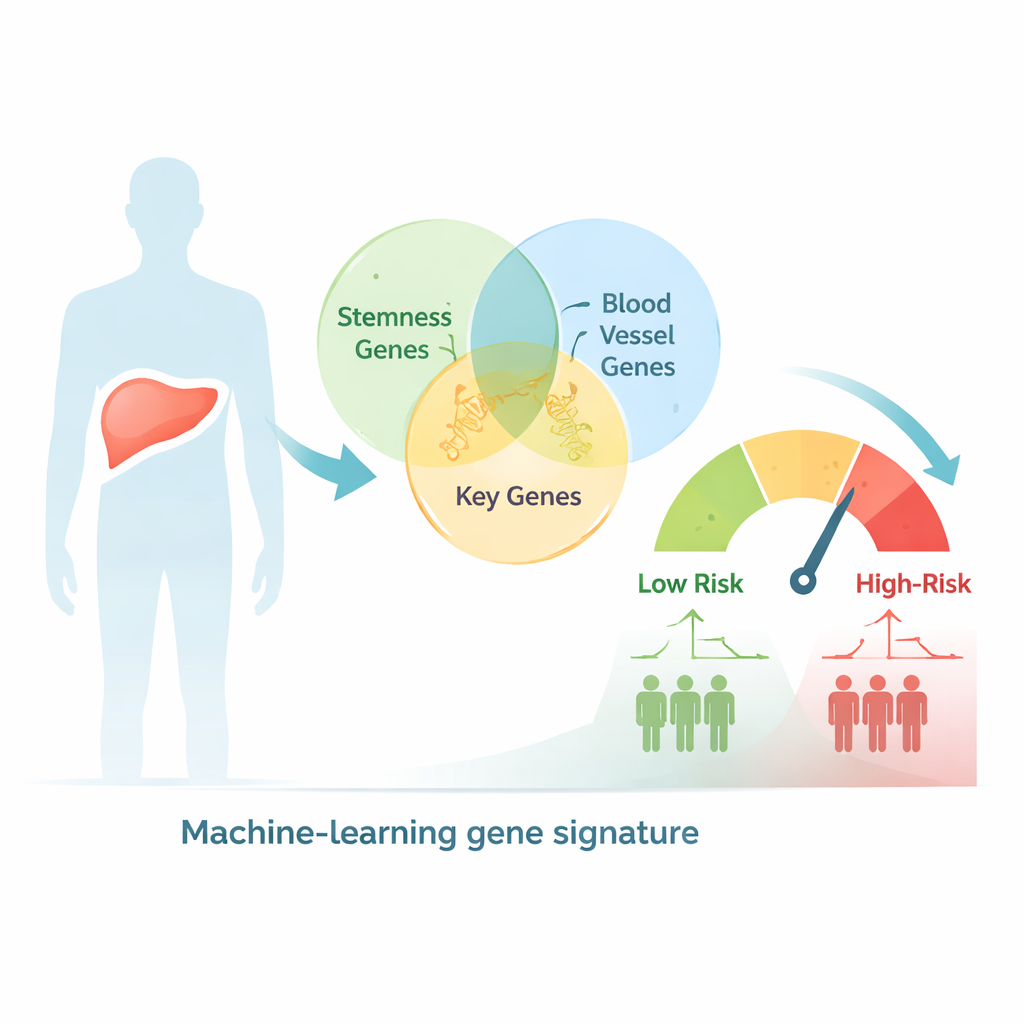
Exploiter le big data pour classer les patients selon le risque
Les chercheurs ont commencé par interroger une vaste base de données génétiques humaines pour identifier des gènes liés à la fois au comportement de type stem et à la formation de vaisseaux, obtenant plus de 2 600 candidats communs. Ils ont ensuite étudié des échantillons de carcinome hépatocellulaire provenant de centaines de patients dont l’activité génique tumorale et l’évolution clinique étaient consignées dans des bases de données publiques sur le cancer. À l’aide de tests statistiques et de méthodes de clustering, ils ont regroupé les patients en deux sous‑types génétiques montrant des différences nettes de stade, de taille tumorale et de survie, suggérant que les signaux combinés de stemness et d’angiogenèse captent une biologie significative de cette maladie.
Construction d’un score de risque à neuf gènes
À partir de ce vaste pool de gènes, l’équipe a utilisé une approche d’apprentissage automatique pour réduire la liste à neuf gènes clés dont l’activité combinée prédit le mieux la durée de survie des patients. Ces neuf gènes ont servi au calcul d’un score de risque pour chaque patient. Les patients dont la tumeur présentait un score élevé avaient une survie globale significativement plus courte, tant dans l’ensemble de données initial que dans un groupe indépendant de patients utilisé pour la validation. La précision du modèle était comparable, voire supérieure, à celle de nombreux outils existants, et lorsque le score a été combiné avec des informations cliniques simples comme le stade tumoral dans un nomogramme, la prédiction de la survie à 1, 3 et 5 ans s’est encore améliorée.
Liens avec le système immunitaire et la réponse thérapeutique
L’équipe a aussi examiné ce que révélait le score à neuf gènes sur le microenvironnement immunitaire tumoral. Les tumeurs à faible risque avaient tendance à être plus « inflammées », avec des niveaux plus élevés de diverses populations cellulaires immunitaires et des signaux d’activation des voies de défense plus marqués. Les tumeurs à haut risque, en revanche, montraient des profils cohérents avec l’évasion immunitaire et des taux de mutation plus élevés dans des gènes clés tels que TP53. En utilisant des outils informatiques établis qui estiment la probabilité de réponse aux immunothérapies modernes, l’étude suggère que les patients à faible risque pourraient mieux répondre aux inhibiteurs de points de contrôle immunitaire que les patients à haut risque. Bien que ces prédictions nécessitent encore une validation en contexte clinique réel, elles offrent une voie pratique pour identifier les patients susceptibles de bénéficier le plus de ces traitements.
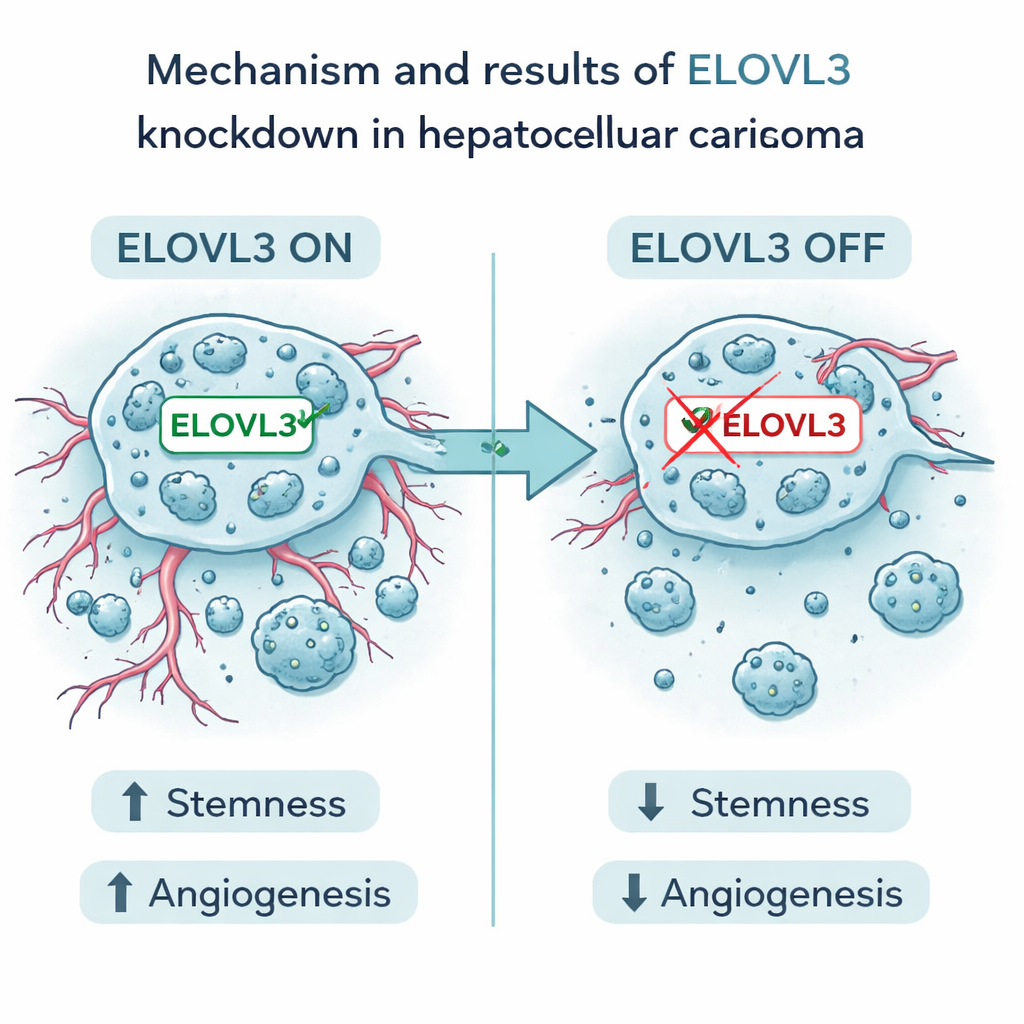
Zoom sur une cible prometteuse
Parmi les neuf gènes, l’un nommé ELOVL3 s’est distingué. Des niveaux élevés de ce gène étaient associés à une survie moindre. En expériences de laboratoire, les auteurs ont réduit l’expression d’ELOVL3 dans des cellules humaines de cancer du foie. Cela a diminué la capacité des cellules à former des agrégats de type stem et a abaissé les niveaux de marqueurs de stemness bien connus. La production et la libération de deux facteurs majeurs favorisant les vaisseaux, VEGFA et FGF2, ont également été réduites. Les cellules cancéreuses présentaient une prolifération, une migration et une invasion réduites, et dans des modèles murins, les tumeurs avec une expression réduite d’ELOVL3 étaient plus petites et présentaient moins de caractéristiques d’agressivité. Ces résultats soutiennent l’idée qu’ELOVL3 contribue à alimenter à la fois le comportement de type graine des cellules cancéreuses hépatiques et leur capacité à générer un réseau vasculaire de soutien.
Ce que cela pourrait signifier pour la prise en charge future
En termes simples, ce travail délivre deux messages principaux. Premièrement, un score simple à neuf gènes, dérivé d’échantillons tumoraux, peut classer les patients atteints de cancer du foie en groupes de risque élevés et faibles et donner des indications sur leur réponse aux traitements immunitaires. Deuxièmement, l’un des gènes de ce score, ELOVL3, semble occuper une position charnière entre la capacité du cancer à se régénérer et sa capacité à développer de nouveaux vaisseaux, ce qui en fait une cible médicamenteuse intéressante pour l’avenir. Bien que le modèle et la cible doivent être confirmés dans des essais cliniques prospectifs, ils ouvrent la voie à une prise en charge plus personnalisée du cancer du foie et à des stratégies combinées visant à bloquer à la fois les « cellules‑graine » du cancer et leur approvisionnement sanguin.
Citation: Cheng, F., Shi, Y., Gao, X. et al. Machine learning-based prognostic model of stemness and angiogenesis-related genes for predicting prognosis and immune infiltration in patients with HCC. Sci Rep 16, 7271 (2026). https://doi.org/10.1038/s41598-026-38379-w
Mots-clés: carcinome hépatocellulaire, cellules souches cancéreuses, angiogenèse, signature génique pronostique, ELOVL3