Clear Sky Science · fr
Variabilité des gènes de référence selon l’âge et le sexe chez la souris 5XFAD souligne les défis de normalisation dans les modèles de la maladie d’Alzheimer
Pourquoi cette étude chez la souris compte pour la recherche sur Alzheimer
Lorsque les scientifiques recherchent des signes précoces ou l’effet d’un traitement dans la maladie d’Alzheimer, ils mesurent souvent l’activité d’expression de divers gènes dans le cerveau. Mais pour savoir si un gène a réellement changé, il faut d’abord une « règle » stable pour la comparaison : des gènes de référence supposés constants. Cet article montre que, dans un modèle murin d’évolution rapide de la maladie d’Alzheimer, ces gènes prétendument stables ne le sont pas autant que de nombreux chercheurs le supposent — en particulier selon l’âge, la région cérébrale et entre mâles et femelles.
Comment les scientifiques lisent l’activité génétique du cerveau
La recherche cérébrale moderne repose souvent sur une technique appelée RT-qPCR, qui quantifie la quantité du message d’un gène présent dans un échantillon de tissu. Comme les échantillons ne contiennent jamais exactement la même quantité totale de matière, les chercheurs normalisent leurs mesures à un ou plusieurs gènes de référence, souvent appelés gènes « ménage », censés rester constants entre les conditions. En pratique, toutefois, des maladies comme Alzheimer modifient profondément les types cellulaires, le métabolisme et l’inflammation dans le cerveau, ce qui peut faire bouger discrètement les niveaux de ces gènes de référence. Si la référence elle-même dérive, toute mesure qui en dépend peut induire en erreur, exagérer ou masquer de véritables changements biologiques.
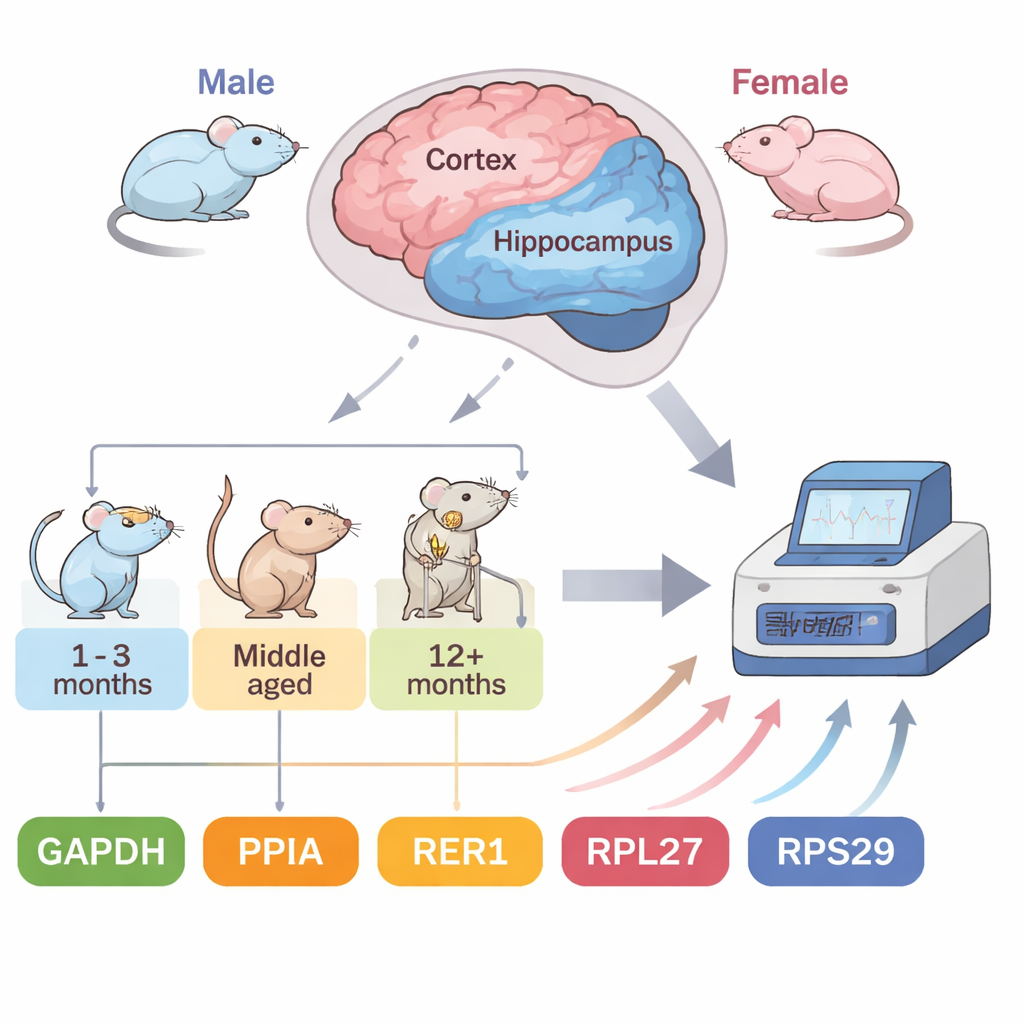
Un modèle murin accéléré de la maladie d’Alzheimer
Les auteurs se sont concentrés sur les souris 5XFAD, un modèle largement utilisé qui porte cinq mutations humaines liées à la forme familiale de la maladie d’Alzheimer. Ces animaux développent des plaques amyloïdes — des agrégats protéiques caractéristiques de la maladie — de façon remarquablement précoce : vers deux mois, avec une accumulation importante à quatre–cinq mois. Cette accélération permet aux chercheurs de suivre les changements liés à la maladie sur quelques mois plutôt que sur des années. Les chercheurs ont examiné deux régions cérébrales vulnérables, le cortex et l’hippocampe, chez des mâles et des femelles à quatre stades : précoce (2 mois), en développement (4 mois) et plus avancés (7 et 10 mois). Ils ont testé cinq gènes de référence courants et utilisé quatre outils statistiques indépendants pour classer la stabilité de chacun dans ces conditions changeantes.
Les gènes de référence ne conviennent pas universellement
Les résultats montrent qu’aucun gène unique n’est parfaitement stable partout. La stabilité dépendait plutôt de la région cérébrale d’origine de l’échantillon, du sexe de la souris et du stade d’avancement de la maladie. Certains gènes, comme Gapdh — un classique utilisé dans de nombreuses études — ont donné des performances relativement bonnes dans plusieurs contextes, notamment dans le cortex aux âges précoces, mais ont montré davantage de variabilité aux stades ultérieurs ou dans certains échantillons hippocampiques. D’autres candidats, tels que Rps29, Ppia, Rpl27 et Rer1, se sont révélés de meilleurs partenaires en combinaisons spécifiques, et ces « meilleures paires » changeaient avec l’âge et le sexe. Globalement, le cortex montrait plus de variabilité que l’hippocampe, et les stades avancés de la maladie, particulièrement chez les mâles, perturbaient la stabilité supposée de plusieurs gènes de référence.
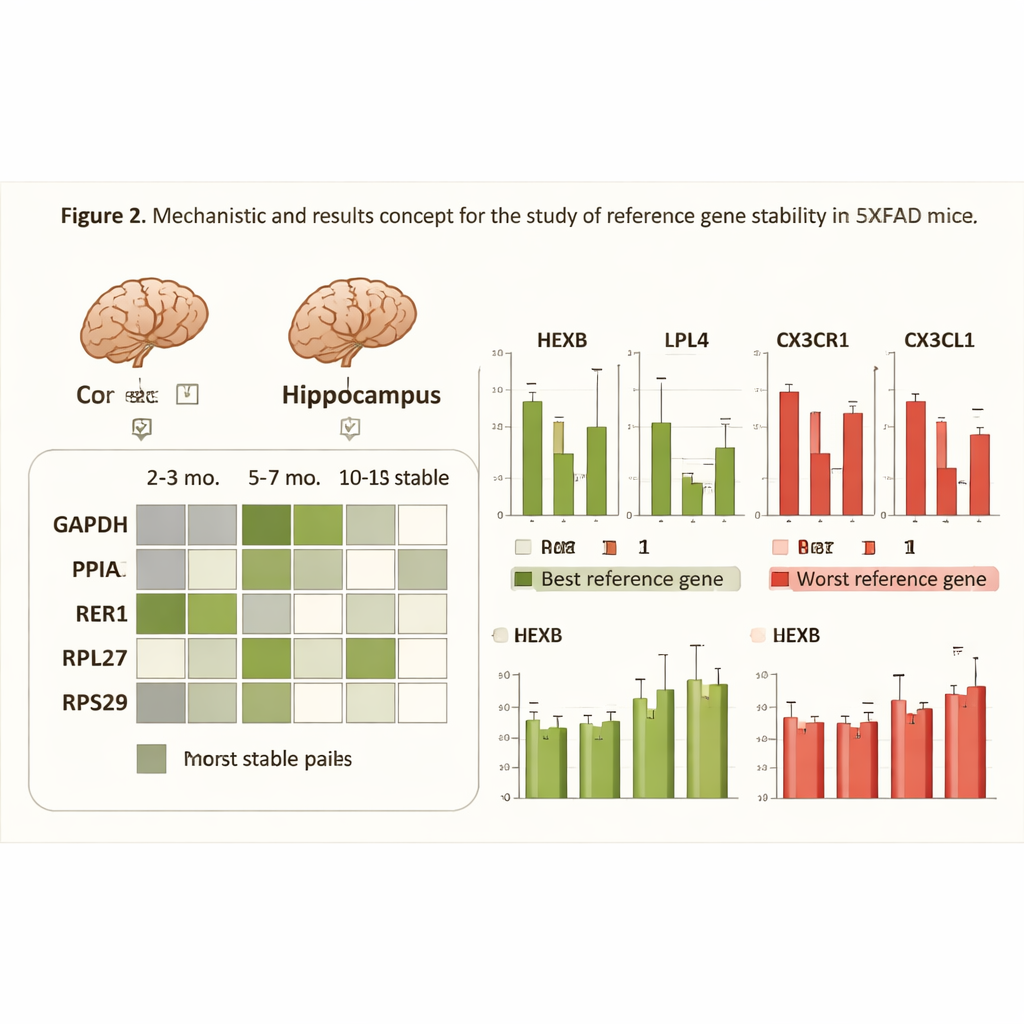
Que se passe-t-il quand la règle se déforme
Pour illustrer pourquoi le choix judicieux des gènes de référence est important, les chercheurs ont analysé quatre gènes cérébraux liés à l’inflammation, au métabolisme et à la signalisation immunitaire — des processus fortement impliqués dans la maladie d’Alzheimer. Ils ont comparé les variations apparentes de ces gènes cibles lorsqu’elles étaient normalisées soit par la paire de référence la plus stable, soit par le gène unique le moins stable, soit par l’ensemble des cinq gènes. Lorsque des gènes de référence de mauvaise qualité étaient utilisés, les données devenaient plus bruyantes et certains changements biologiquement pertinents semblaient atténués voire statistiquement non significatifs. En revanche, l’utilisation de la paire la mieux adaptée à chaque condition réduisait la dispersion des mesures et renforçait la détection de différences réelles entre souris saines et malades, en particulier aux stades pathologiques avancés.
Des signaux plus clairs pour une maladie complexe
Pour les non-spécialistes, la conclusion est simple : même les étalons de base utilisés dans les études d’expression génique peuvent se déformer sous la pression d’une maladie cérébrale en rapide évolution comme Alzheimer. Ce travail fournit un guide pratique pour choisir de meilleurs gènes de référence dans un modèle murin important et souligne que les chercheurs doivent valider leurs « règles » pour chaque région cérébrale, âge et sexe étudiés. Ce faisant, les scientifiques obtiennent des mesures plus nettes et plus fiables des gènes qui changent réellement lors de la dégénérescence de type Alzheimer — une étape essentielle pour comprendre les mécanismes de la maladie et évaluer des traitements potentiels.
Citation: Daini, E., Antonioni, K., Piemontese, M. et al. Reference gene variability across age and sex in 5XFAD mice highlights normalization challenges in Alzheimer’s models. Sci Rep 16, 7302 (2026). https://doi.org/10.1038/s41598-026-38346-5
Mots-clés: maladie d’Alzheimer, expression génique, souris 5XFAD, gènes de référence, RT-qPCR