Clear Sky Science · fr
DGCR8 régule plusieurs processus de réparation par excision de nucléotides couplée à la transcription
Comment la lumière du soleil parle à nos gènes
Chaque fois que nous nous exposons au soleil, des rayons ultraviolets (UV) invisibles frappent notre peau et endommagent l’ADN de nos cellules. La plupart du temps, nos cellules réparent silencieusement ces lésions avant qu’elles ne causent des problèmes. Cette étude met en lumière un acteur surprenant de ce système de protection : une protéine appelée DGCR8, connue jusqu’ici pour son rôle dans la production de microARN. Les auteurs montrent que DGCR8 peut changer de fonction après exposition aux UV, coordonnant plusieurs étapes d’une voie clé de réparation de l’ADN qui aide à prévenir le cancer et d’autres maladies.
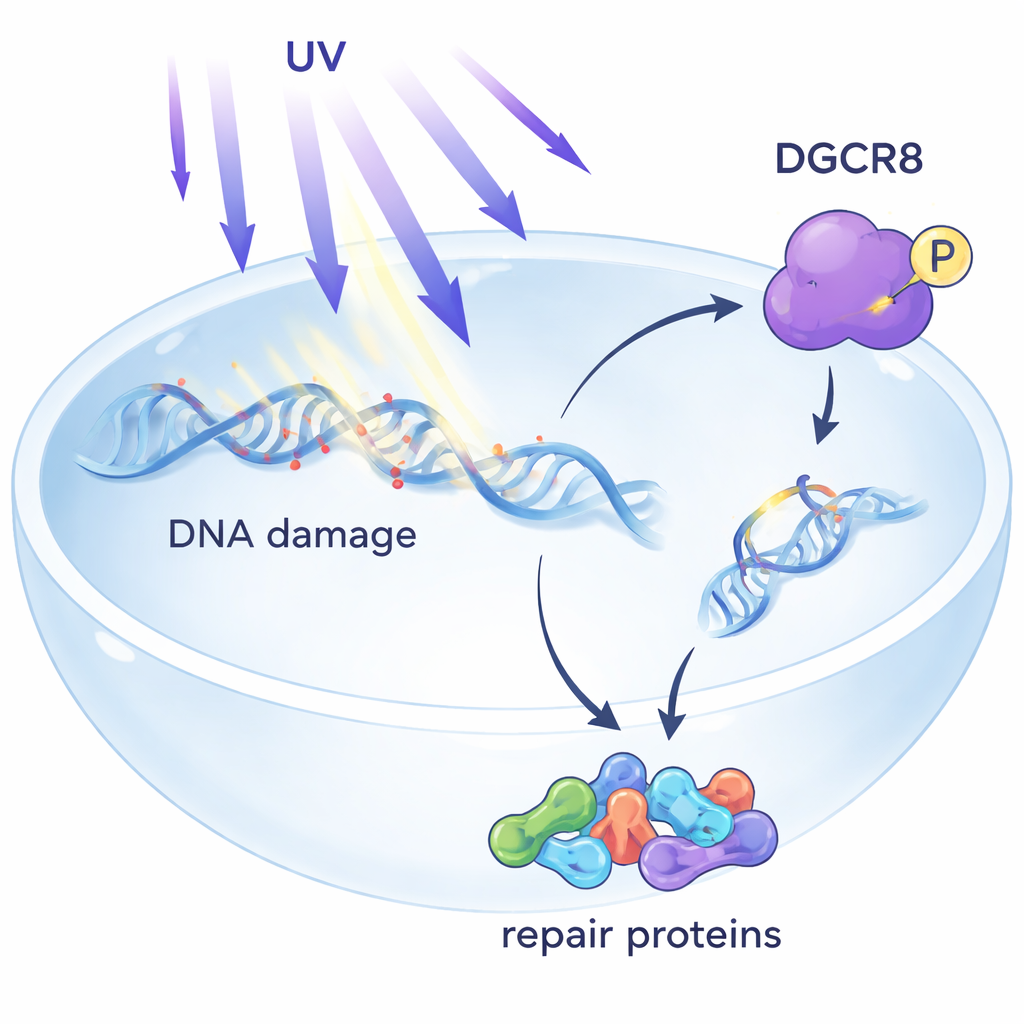
Un gardien discret au cœur de la réparation de l’ADN
La lumière UV crée de petites lésions dans l’ADN qui peuvent bloquer les machines moléculaires qui lisent les gènes. L’une des principales défenses du corps est la réparation par excision de nucléotides couplée à la transcription (TC-NER), qui cible les dommages qui arrêtent l’enzyme de lecture des gènes. Jusqu’à présent, DGCR8 était surtout connu pour traiter les microARN, de courts ARN qui modulent finement l’activité des gènes. Des travaux antérieurs laissaient entendre que DGCR8 protégeait aussi les cellules des UV, mais le mécanisme était obscur. Cet article montre qu’après exposition aux UV, DGCR8 s’associe physiquement à des facteurs centraux de la TC-NER, agissant comme un organisateur qui rassemble les composants de la réparation là où la transcription est bloquée.
Un interrupteur moléculaire marche/arrêt pour DGCR8
La clé du nouveau rôle de DGCR8 est une seule modification chimique sur l’un de ses composants, l’acide aminé sérine en position 153. Lorsque ce site est phosphorylé — c’est-à-dire quand un groupe phosphate y est ajouté — DGCR8 acquiert la capacité de se lier aux acteurs centraux de la TC-NER, notamment l’ARN polymérase II (l’enzyme de lecture des gènes) et des facteurs de réparation nommés CSB, CSA et UVSSA. Des cellules modifiées pour exprimer une version de DGCR8 qui ne peut pas être phosphorylée en ce site (le mutant S153A) ont montré des interactions affaiblies ou perdues entre ces protéines de réparation, et l’assemblage habituel du complexe de réparation déclenché par les UV n’a pas eu lieu. Une version « phosphomimétique » qui se comporte comme si elle était constamment phosphorylée a eu l’effet inverse, renforçant les interactions clés même sans UV. Ces résultats indiquent que la phosphorylation de la Ser153 agit comme un interrupteur marche/arrêt qui bascule DGCR8 de son rôle habituel de traitement des ARN vers un coordinateur de la réparation de l’ADN.
Démêler des nœuds dangereux ADN–ARN
Au-delà de rassembler les protéines de réparation, DGCR8 aide aussi à gérer des structures appelées boucles R — de courts segments où l’ARN nouvellement synthétisé se rattache à l’ADN d’origine, formant un hybride ADN–ARN. En petite quantité, les boucles R peuvent être utiles, mais lorsqu’elles s’accumulent après exposition aux UV, elles peuvent bloquer la réplication et déstabiliser les chromosomes. À l’aide d’anticorps spécialisés et de sondes fluorescentes, les auteurs ont constaté que les cellules dépourvues de DGCR8, ou exprimant la forme non-phosphorylable S153A, accumulent beaucoup plus de boucles R après UV. La DGCR8 phosphorylée a été observée au niveau de ces structures hybrides, en particulier là où elles chevauchaient les lésions induites par les UV, ce qui suggère qu’elle aide à prévenir ou à éliminer les boucles R nuisibles précisément aux gènes actifs sous stress.
Maintenir la copie de l’ADN sous contrôle
Lorsque des lésions d’ADN ou des boucles R perturbent la copie du génome, les cellules ralentissent normalement la réplication via un circuit de sécurité connu sous le nom de point de contrôle ATR–CHK1. Des expériences de suivi des fibres ont montré que les cellules avec DGCR8 normal ralentissaient leurs pistes de réplication après exposition aux UV, traduisant l’activation du point de contrôle. En contraste frappant, les cellules dépourvues de DGCR8 ou portant la mutation S153A ont continué à répliquer à une vitesse quasi normale, bien qu’elles aient accumulé des lésions d’ADN et des boucles R. Des tests supplémentaires ont révélé que si ATR lui-même était activé, son partenaire clé CHK1 était peu activé dans ces cellules mutantes. Cela indique que la DGCR8 phosphorylée aide à relayer le signal de stress issu de l’ADN endommagé et des boucles R vers CHK1, permettant à la cellule de faire une pause et de stabiliser la réplication.
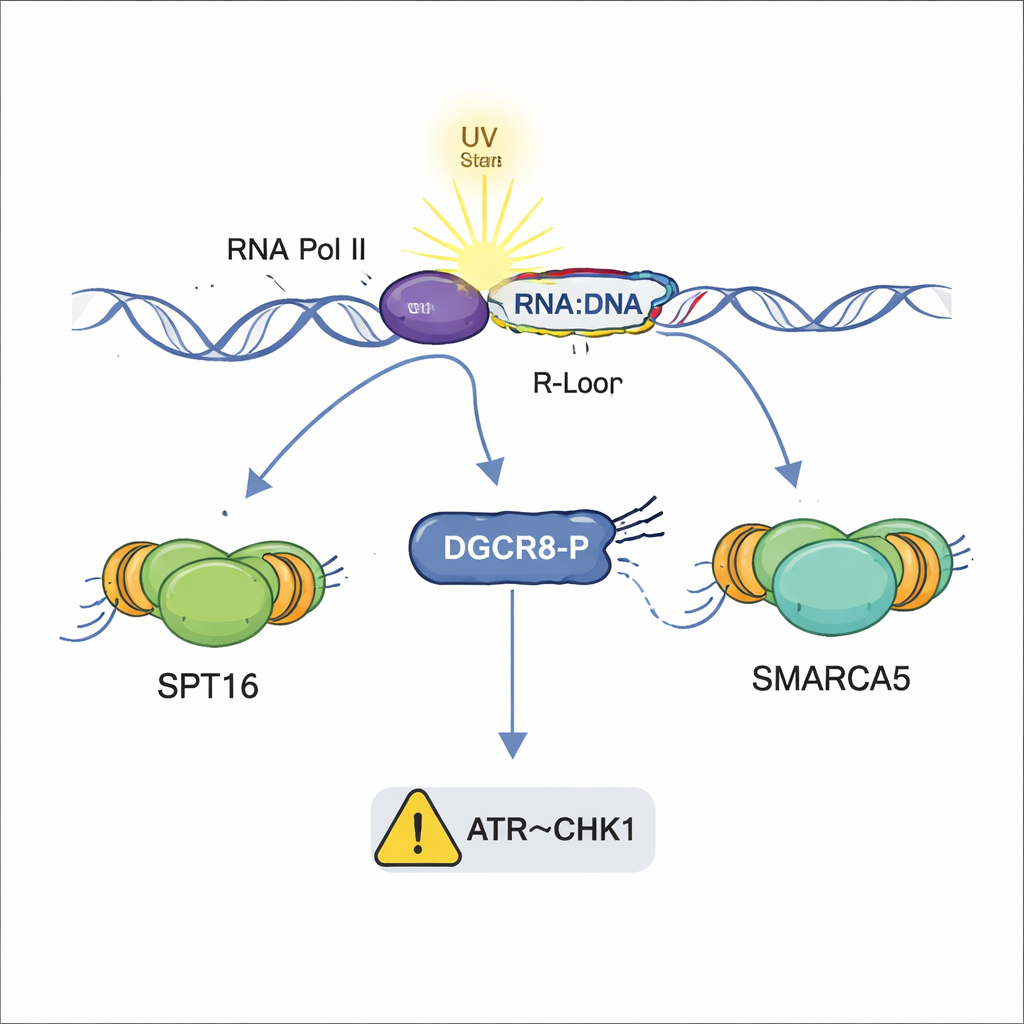
Pourquoi cela compte pour la santé et la maladie
Pris ensemble, ces résultats révèlent DGCR8 comme un gardien polyvalent qui coordonne plusieurs niveaux de la réponse aux dégâts induits par les UV : l’assemblage de l’équipe TC-NER, le recrutement de remodelateurs de la chromatine qui ouvrent l’ADN, la limitation des hybrides ADN–ARN nuisibles, et la contribution au ralentissement de la réplication via la voie ATR–CHK1. De manière cruciale, ces actions sont séparées du rôle traditionnel de DGCR8 dans la biogenèse des microARN et dépendent de la phosphorylation d’un site unique. Étant donné que des défauts dans la réparation de l’ADN et le contrôle des boucles R sont associés au cancer et à des maladies neurologiques, et que des mutations de DGCR8 ont été identifiées dans certains tumeurs, comprendre cet interrupteur moléculaire pourrait ouvrir de nouvelles perspectives pour le diagnostic ou le traitement de pathologies liées aux dégâts UV et à l’instabilité du génome.
Citation: Watanabe, T., Yoshinami, D., Yamasaki, H. et al. DGCR8 regulates multiple processes of transcription coupled nucleotide excision repair. Sci Rep 16, 7112 (2026). https://doi.org/10.1038/s41598-026-38338-5
Mots-clés: dégâts d’ADN UV, DGCR8, réparation de l’ADN, boucles R, stabilité du génome