Clear Sky Science · fr
PARP-1 relie la signalisation β-caténine/TCF4 à la transition épithélio‑mésenchymateuse dans l’endométriose
Pourquoi cette recherche est importante pour la santé des femmes
L’endométriose est une pathologie douloureuse dans laquelle du tissu semblable à la muqueuse utérine se développe au mauvais endroit, par exemple sur les ovaires. Ces foyers ectopiques peuvent envahir les structures voisines, provoquer des adhérences et contribuer à l’infertilité ; les traitements actuels restent imparfaits et les symptômes récidivent souvent. Cette étude explore un « interrupteur » moléculaire appelé PARP‑1 et se demande s’il favorise l’invasion des lésions d’endométriose — et si des médicaments existants qui bloquent PARP‑1 pourraient en atténuer l’activité.
Un regard approfondi sur le comportement des lésions invasives
Bien que l’endométriose soit classée comme une maladie bénigne, le tissu ectopique se comporte souvent de façon étonnamment agressive : il migre, s’implante et persiste de manière comparable à un cancer à progression lente. Un processus clé derrière ce comportement est la transition épithélio‑mésenchymateuse (TEM ou EMT en anglais), au cours de laquelle des cellules organisées en feuillets relâchent leurs connexions et acquièrent un phénotype plus mobile et fibreux. Les auteurs ont analysé des tissus de femmes avec et sans endométriose et ont constaté que les lésions ovariennes endométriosiques présentaient un profil de type EMT : la protéine « colle » E‑cadhérine était réduite, tandis que des marqueurs de cellules plus mobiles, comme la N‑cadhérine et la vimentine, étaient augmentés. Parallèlement, les niveaux de PARP‑1 et des composants de la voie de contrôle de croissance Wnt/β‑caténine étaient les plus élevés dans ces lésions, suggérant que ces changements évoluent de concert.
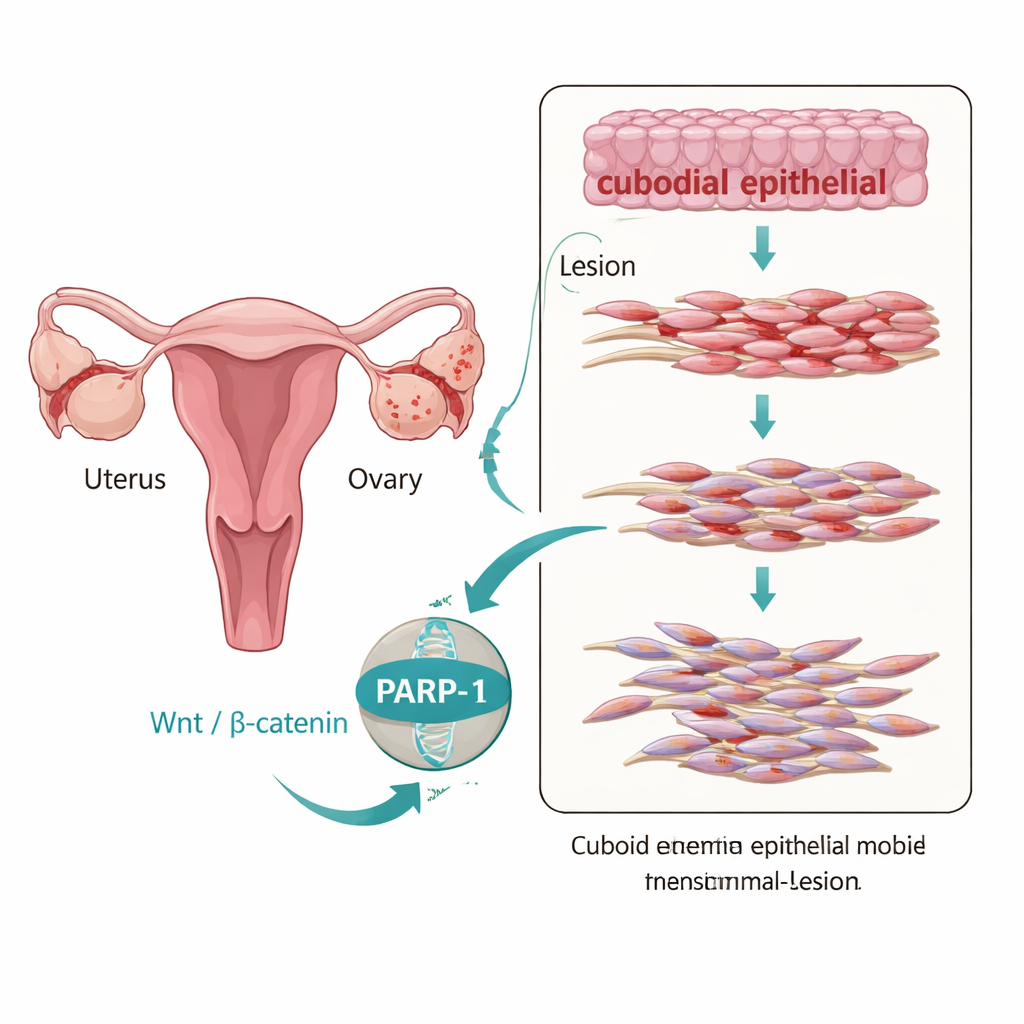
Le pont moléculaire entre les signaux et le changement cellulaire
Pour déterminer si PARP‑1 est simplement présent ou active dans la conduite de ces changements, les chercheurs ont utilisé une lignée cellulaire épithéliale endométriosique immortalisée appelée 12Z. Lorsqu’ils ont augmenté artificiellement les niveaux de PARP‑1 dans ces cellules, les marqueurs de TEM ont évolué vers un profil plus invasif et les cellules sont devenues plus mobiles et viables dans des essais in vitro reproduisant la cicatrisation et l’invasion tissulaire. En réduisant PARP‑1 avec des ARN ciblés, le schéma s’est inversé : l’E‑cadhérine augmentait, les marqueurs mésenchymateux diminuaient, et les cellules se déplaçaient et proliféraient moins. Fait important, PARP‑1 s’associait physiquement à la β‑caténine et à TCF4, deux acteurs clés qui traduisent les signaux Wnt en activité génique, positionnant PARP‑1 comme un pont reliant les indices externes au programme génique de la TEM dans le noyau.
Atténuer l’interrupteur avec un médicament anticancéreux
Étant donné que des médicaments inhibant l’activité de PARP sont déjà utilisés en oncologie, l’équipe a ensuite étudié si l’un d’eux, l’olaparib, pouvait atténuer les caractéristiques de type EMT et réduire la croissance des lésions dans un modèle murin d’endométriose. Des souris implantées avec de petits fragments de tissu utérin ont développé des lésions ectopiques abdominales, reproduisant des aspects de la maladie humaine. Traitées pendant deux semaines par olaparib, ces animaux présentaient un volume total des lésions nettement réduit et des utérus plus légers avec moins de lésions adhérentes que les contrôles non traités. Les tissus des souris traitées montraient également un profil plus « épithélial » — E‑cadhérine plus élevée et N‑cadhérine, vimentine, β‑caténine et TCF4 plus faibles — indiquant que l’inhibition de PARP avait éloigné les cellules de l’état invasif de type EMT.
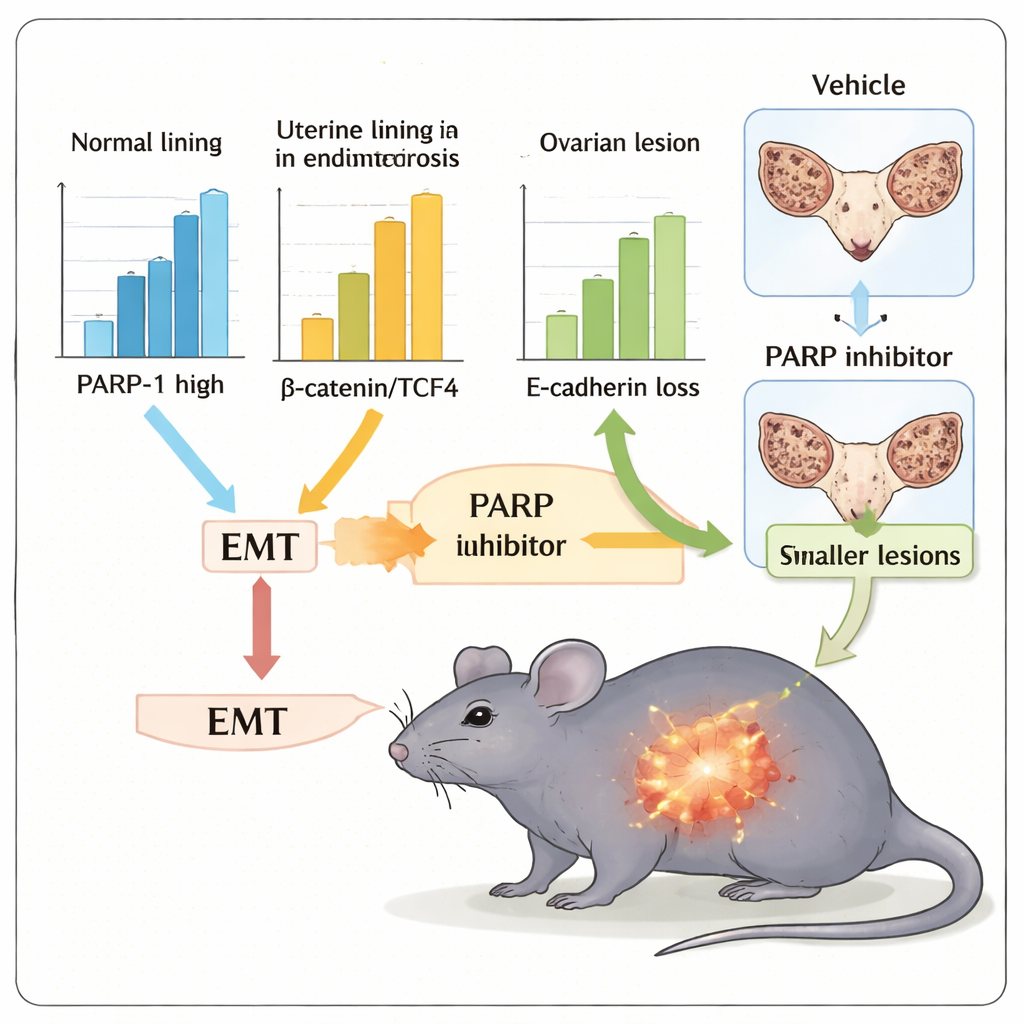
Ce que cela pourrait signifier pour les soins futurs
Pris ensemble, les résultats issus d’échantillons de patientes, d’expériences en culture cellulaire et du modèle murin soutiennent une idée unificatrice : PARP‑1 agit comme un nœud pharmacologiquement ciblable qui couple la signalisation Wnt/β‑caténine au comportement de type TEM dans l’endométriose. Plutôt que d’être l’unique maître‑interrupteur, PARP‑1 semble être un connecteur clé dans un réseau plus large d’inflammation, de stress oxydatif et de signaux hormonaux qui déterminent la croissance et l’invasion des lésions. Étant donné l’existence d’inhibiteurs de PARP, ce travail ouvre la possibilité de les réaffecter ou d’en adapter l’usage — peut‑être en combinaison avec d’autres traitements ciblant ces voies ou le système immunitaire — pour réduire la charge lésionnelle, les adhérences et possiblement l’impact sur la fertilité. Des études plus larges et de plus longue durée seront nécessaires, mais cette recherche trace une voie concrète vers des thérapies plus ciblées et fondées sur les mécanismes pour une affection qui touche des millions de femmes dans le monde.
Citation: Zhang, L., Li, X., Kong, L. et al. PARP-1 couples β-catenin/TCF4 signaling to epithelial–mesenchymal transition in endometriosis. Sci Rep 16, 6940 (2026). https://doi.org/10.1038/s41598-026-38335-8
Mots-clés: endométriose, PARP-1, transition épithélio‑mésenchymateuse, Wnt/β‑caténine, thérapie par inhibiteur de PARP