Clear Sky Science · fr
Une nouvelle méthode par chambre d’écoulement couplée à l’IA quantifiant la fragilité osmotique des érythrocytes
Pourquoi la fragilité des globules rouges importe
Chaque seconde, des millions de vos globules rouges se faufilent dans des vaisseaux d’un diamètre comparable à un cheveu tout en transportant l’oxygène. La facilité avec laquelle ces cellules éclatent sous contrainte — appelée leur « fragilité » — peut révéler des anémies, des problèmes de conservation du sang et des complications d’infections sévères comme la septicémie. Cette étude présente un appareil microscopique moderne assisté par IA qui mesure la vitesse à laquelle les globules rouges se désagrègent dans des solutions salines, visant à rendre ce test important plus rapide, plus précis et plus facile à réaliser tant dans les laboratoires de recherche que, un jour, dans les hôpitaux.
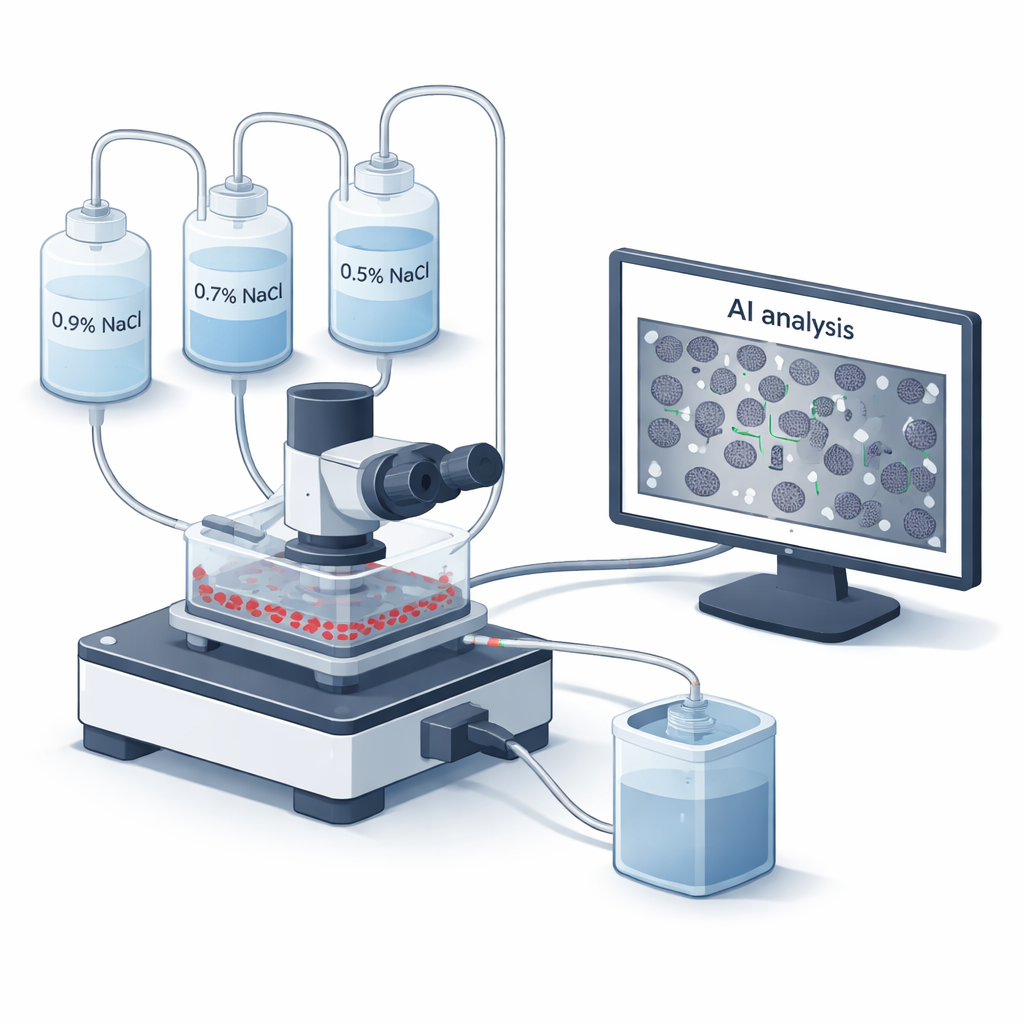
Une nouvelle façon d’observer les cellules sanguines sous stress
Les cliniciens utilisent des tests de fragilité osmotique depuis les années 1940 pour évaluer la résistance des membranes des globules rouges. Classiquement, le sang est mélangé à une série de solutions salines, et un appareil mesure quelle quantité d’hémoglobine se déverse lorsque les cellules éclatent. Bien que fiable, cette méthode traditionnelle est lente, manuelle et aveugle à l’allure réelle des cellules individuelles au moment de leur défaillance. L’équipe à l’origine de cet article a conçu un nouveau système microfluidique de « chambre d’écoulement », nommé BioExP, qui étale les globules rouges en monocouche fine sur une lame de verre traitée. Différentes solutions salines sont acheminées sur cette couche pendant qu’un microscope et une caméra enregistrent en temps réel ce qui se passe, et un logiciel intégré utilise l’intelligence artificielle pour compter combien de cellules restent intactes à chaque concentration saline.
Mettre l’IA et le contrôle d’écoulement à l’épreuve
Pour évaluer la fiabilité de BioExP, les chercheurs l’ont comparé directement à l’essai spectrophotométrique classique en utilisant du sang provenant de quatre donneurs sains. Ils se sont focalisés sur un nombre clé appelé MCF₅₀ : la concentration saline à laquelle la moitié des globules rouges ont éclaté. D’abord, ils ont dû régler leur nouveau système en déterminant le meilleur « temps de satiation » — durée d’exposition des cellules à une solution hypotonique donnée pour que les cellules les plus vulnérables aient lysé sans dépasser. En suivant la disparition des cellules à 0,4 % de sel pendant 15 minutes, ils ont observé qu’environ 80 % de l’hémolyse totale survenait durant les trois premières minutes. Cette fenêtre de trois minutes est devenue leur temps d’exposition standard, conciliant rapidité et mesures fiables.
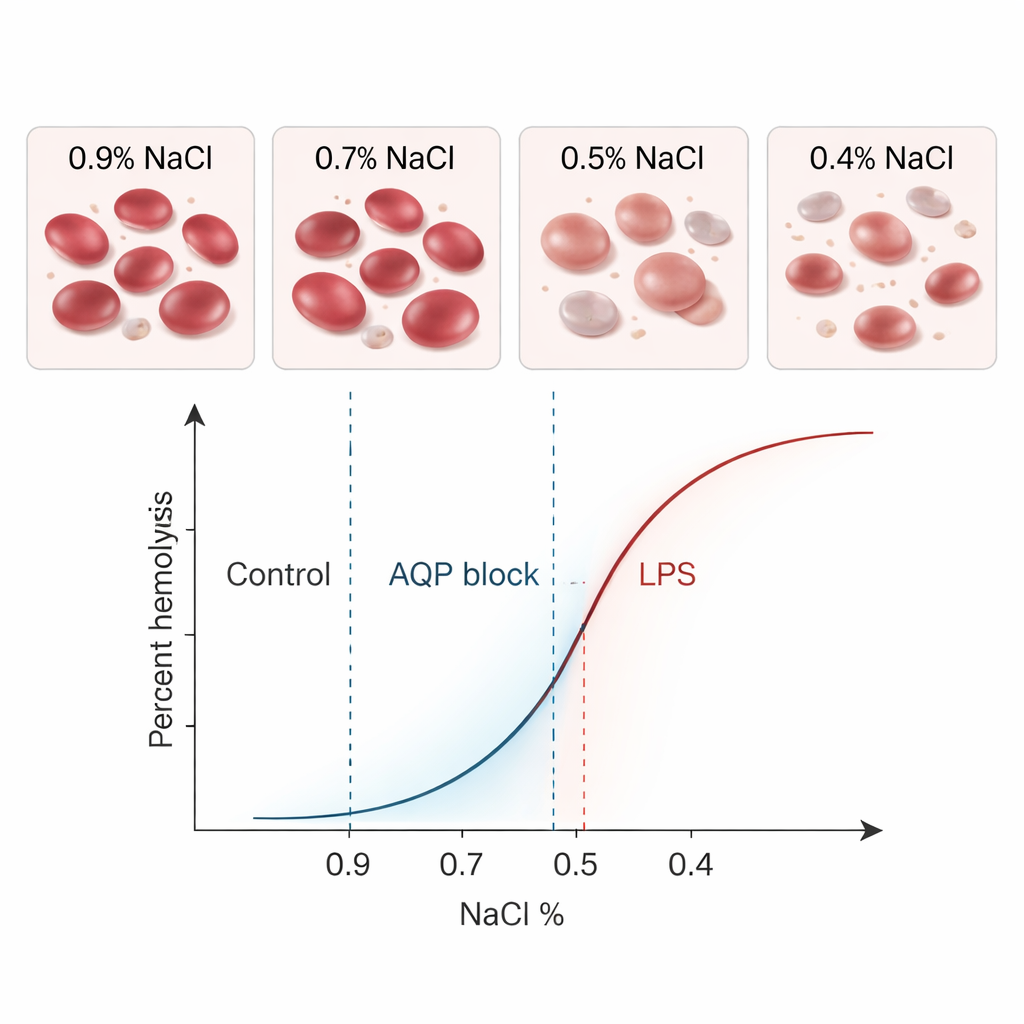
Concordance avec le test classique et exploration de la biologie réelle
Quand ils ont analysé les mêmes échantillons sains avec les deux méthodes, BioExP et le test classique ont fourni des valeurs moyennes de MCF₅₀ presque identiques — 0,41 % de sel — avec une variabilité similaire. Les analyses statistiques n’ont montré aucune différence significative entre les méthodes, et la plupart des paires de résultats se situaient dans des limites d’accord étroites. Autrement dit, le nouvel appareil « parlait » effectivement le même langage que le test établi. La véritable force de BioExP réside cependant dans sa capacité à tester comment diverses conditions modifient la fragilité cellulaire. Les chercheurs ont choisi deux modulateurs biologiquement significatifs : le chlorure de mercure, qui bloque des protéines canal d’eau appelées aquaporines dans la membrane cellulaire, et le lipopolysaccharide bactérien (LPS), une toxine associée à la septicémie.
Comment les toxines et les canaux à eau modifient la résistance cellulaire
Le blocage des aquaporines a rendu les globules rouges plus difficiles à rompre : le MCF₅₀ s’est déplacé vers des concentrations salines plus faibles, ce qui signifie que les cellules toléraient une plus grande dilution avant de se rompre. Tant BioExP que la méthode classique ont détecté clairement ce décalage vers la gauche. Le LPS a eu l’effet inverse. Lorsqu’on a incubé les globules rouges avec une forte dose de LPS en l’absence de plasma, ils sont devenus plus fragiles, se rompant à des concentrations salines plus élevées. Au microscope, de nombreuses cellules ont changé de forme, devenant plus sphériques ou épineuses — signes visuels d’une perturbation de leurs membranes. Là encore, les deux méthodes ont enregistré un fort décalage vers la droite des courbes de fragilité, statistiquement significatif. Sur l’ensemble de ces essais, le nouveau système en chambre d’écoulement a systématiquement suivi les mêmes tendances biologiques que l’essai ancien, avec des valeurs absolues légèrement plus faibles, systématiques et de faible ampleur.
Ce que cela signifie pour les patients et les laboratoires
La plateforme BioExP réduit le temps d’analyse de plusieurs heures à moins d’une heure, nécessite des volumes de sang minimes (potentiellement une simple piqûre au doigt), et automatise le comptage et l’ajustement des courbes avec de l’IA plutôt que de s’appuyer sur de nombreuses étapes manuelles. Parce qu’elle image les mêmes cellules au fil du temps, elle peut relier l’apparence cellulaire à la facilité avec laquelle elles éclatent, et tester de nombreux niveaux de salinité ou conditions médicamenteuses en une seule passe. L’étude montre que cette approche moderne peut égaler la précision du test classique de fragilité osmotique tout en apportant rapidité, souplesse et richesse visuelle. Si elle est validée ultérieurement sur des cohortes plus larges et diversifiées de donneurs, une telle technologie pourrait devenir un outil précieux pour diagnostiquer les anémies hémolytiques, contrôler le sang stocké dans les banques et explorer comment les infections ou de nouveaux médicaments affaiblissent ou protègent nos globules rouges.
Citation: Fırat, I.S., Alaçayır, Ö., Creutz, T. et al. A novel AI-coupled flow chamber method quantifying erythrocyte osmotic fragility. Sci Rep 16, 7175 (2026). https://doi.org/10.1038/s41598-026-38322-z
Mots-clés: globules rouges, fragilité osmotique, microfluidique, septicémie, intelligence artificielle