Clear Sky Science · fr
Inactivation sélective de Lis1 perturbe la migration et le positionnement des interneurones corticals somatostatines
Pourquoi de minuscules cellules cérébrales et un seul gène comptent
Dans notre cerveau, des milliards de neurones doivent se retrouver exactement au bon endroit pour que pensées, émotions et souvenirs fonctionnent correctement. Cette étude s’intéresse à un petit mais puissant groupe de cellules cérébrales appelées interneurones somatostatines et à un gène nommé Lis1, déjà connu pour provoquer un grave trouble de type « cerveau lisse » lorsqu’il est muté. En demandant ce qui se passe quand Lis1 est désactivé uniquement dans cette population cellulaire restreinte, les chercheurs révèlent comment des erreurs subtiles dans le mouvement cellulaire pendant le développement peuvent remodeler des régions cérébrales clés impliquées dans l’humeur, la mémoire et les maladies mentales.
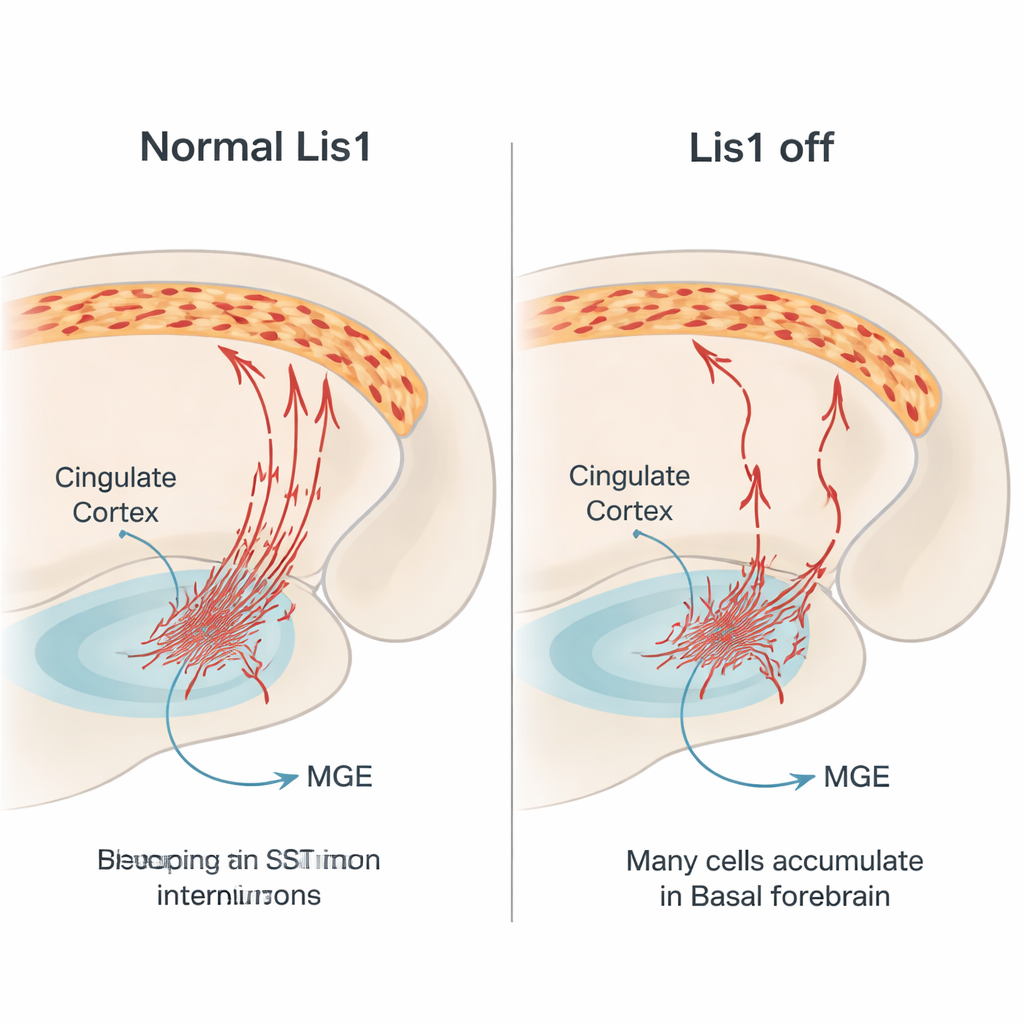
Acteurs clefs du système de freinage du cerveau
Les interneurones somatostatines font partie du système de freinage du cerveau. Ils libèrent le signal inhibiteur GABA et un peptide appelé somatostatine, ciblant principalement les branches des neurones pyramidaux excitateurs. Cela aide à maintenir l’activité cérébrale en équilibre, essentiel pour la perception normale, la prise de décision et le contrôle émotionnel. Beaucoup de ces interneurones naissent dans une région profonde du cerveau embryonnaire appelée la zone ganglionnaire médiale. De là, ils migrent latéralement sur de longues distances vers le cortex cérébral, y compris le cortex cingulaire, un carrefour pour l’émotion, la douleur et la mémoire. Parce que ce trajet est complexe et finement chronométré, les gènes qui guident le mouvement cellulaire sont cruciaux. Lis1 est l’un de ces gènes, connu pour réguler l’armature interne de la cellule et la machinerie motrice qui déplacent le noyau et façonnent la cellule pendant la migration.
Une expérience ciblée d’« extinction » génétique
Pour savoir ce que Lis1 fait spécifiquement dans les interneurones somatostatines, les auteurs ont conçu des souris chez lesquelles Lis1 est supprimé uniquement dans les cellules qui activent le gène de la somatostatine. Ils ont aussi utilisé une protéine rouge fluorescente pour marquer ces cellules de façon permanente et les suivre pendant leur développement. Ce dispositif a permis à l’équipe de distinguer les effets à l’intérieur des cellules somatostatines elles‑mêmes des changements dans le reste du cerveau. Ils ont ensuite examiné deux régions cingulaires — le cortex cingulaire antérieur et le cortex rétrosplénial — environ un mois après la naissance, à un moment où les circuits corticaux sont relativement matures mais encore plastiques. Des méthodes de comptage rigoureuses ont été employées pour estimer à la fois le nombre absolu et la densité des interneurones somatostatines dans chaque couche corticale.
Moins d’interneurones et un motif corticale déplacé
Chez les jeunes souris adultes dépourvues de Lis1 dans les interneurones somatostatines, le cortex cingulaire antérieur comme le cortex rétrosplénial contenaient beaucoup moins de ces cellules que chez les animaux témoins. La réduction était importante et constante dans toutes les couches examinées, indiquant une véritable perte plutôt qu’une simple redistribution. Lorsqu’ils ont regardé de plus près l’organisation des cellules restantes, les chercheurs ont constaté une modification du motif habituel par couche. Chez les souris saines, les interneurones somatostatines tendent à se concentrer davantage dans les couches profondes du cortex. Chez les mutants, ce gradient était inversé, avec relativement plus de cellules dans les couches supérieures et moins dans la couche la plus profonde. Il est important de noter que la taille globale des régions cingulaires n’a pas diminué, si bien que la densité réduite reflète réellement des interneurones manquants et non un volume tissulaire comprimé.
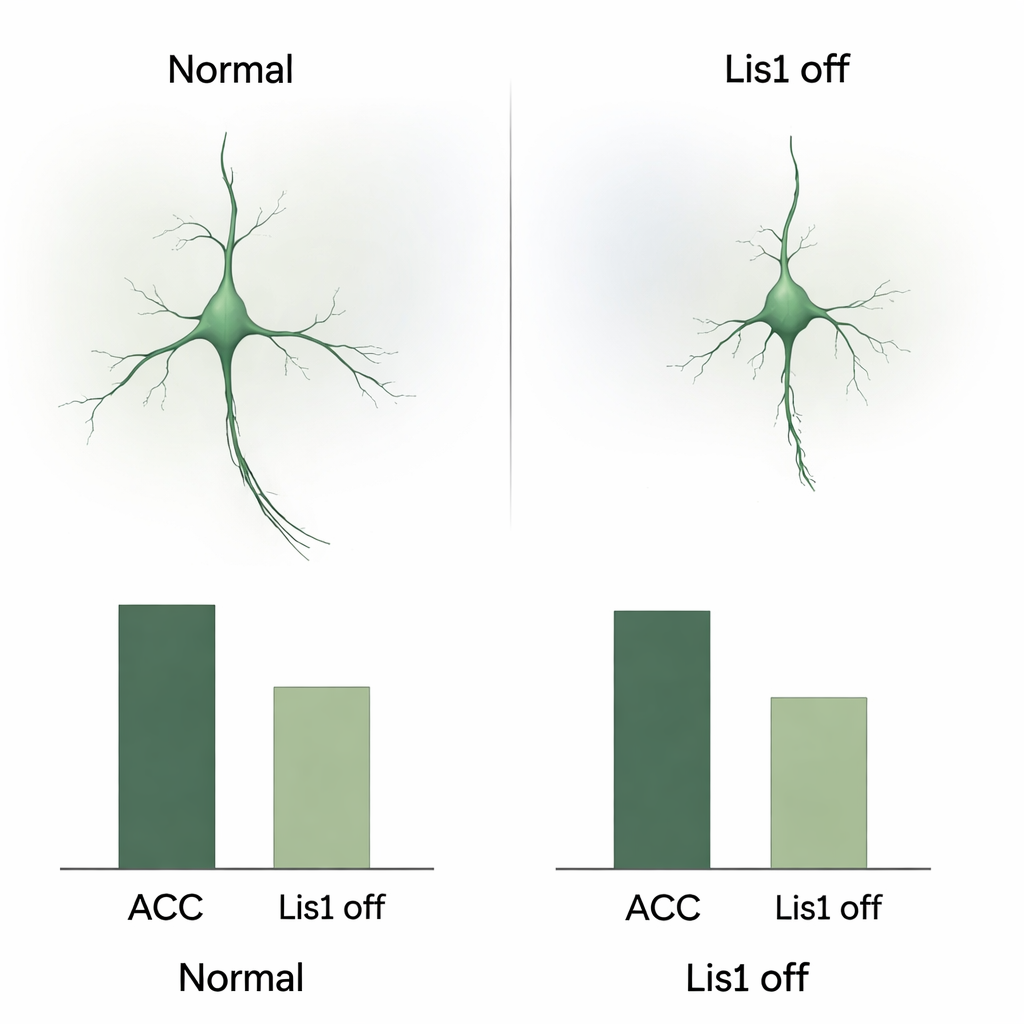
Un trajet développemental qui déraille
Pour comprendre comment cette perte survient, l’équipe a suivi les cellules somatostatines marquées en rouge chez les embryons. Ils ont confirmé que la suppression de Lis1 commence après que ces cellules ont cessé de se diviser, écartant un effet direct sur leur naissance. Au contraire, le problème apparaît pendant leur longue migration. Aux stades de gestation intermédiaires, beaucoup moins de cellules marquées étaient observées en train de traverser les voies normales vers le cortex, et beaucoup semblaient s’enliser dans le cerveau basal, une région ventrale qu’elles doivent franchir. Les cellules migrantes qui avançaient présentaient des formes altérées : prolongements leaders plus courts, moins de ramifications et des corps cellulaires plus petits et plus ronds, autant d’indices d’un dysfonctionnement de leur machinerie de transport interne. À des stades plus tardifs, la région ventrale des mutants contenait davantage de cellules exprimant des marqueurs de mort cellulaire programmée, suggérant que beaucoup d’interneurones bloqués meurent avant d’atteindre le cortex.
Ce que cela signifie pour la santé cérébrale
En résumé, lorsque Lis1 est désactivé uniquement dans les interneurones somatostatines, beaucoup de ces cellules débutent leur parcours normalement mais n’atteignent pas leurs destinations finales dans le cortex cingulaire. Certaines s’accumulent et meurent en chemin, et celles qui arrivent sont moins nombreuses et mal réparties entre les couches corticales. Parce que les systèmes à somatostatine ont été à plusieurs reprises associés à la dépression, à la schizophrénie, à l’épilepsie et aux maladies neurodégénératives, ce travail souligne une voie directe et spécifique à un type cellulaire par laquelle un dysfonctionnement de Lis1 pourrait contribuer à des rythmes cérébraux perturbés et à des symptômes psychiatriques. L’étude montre que même une population neuronale de taille modeste, guidée par un seul gène, peut être cruciale pour construire les circuits équilibrés qui sous-tendent une pensée et un comportement sains.
Citation: Pombero, A., García-López, R., Geijo-Barrientos, E. et al. Selective Lis1 inactivation disrupts migration and positioning of cortical somatostatin interneurons. Sci Rep 16, 7330 (2026). https://doi.org/10.1038/s41598-026-38316-x
Mots-clés: interneurones somatostatines, gène Lis1, migration neuronale, <keyword>troubles du développement neuro