Clear Sky Science · fr
Développement et caractérisation de lignées cellulaires épithéliales intestinales de souris immortalisées
Pourquoi de nouveaux modèles intestinaux sont importants
La muqueuse de l’intestin est une frontière animée où se rencontrent aliments, microbes utiles et germes dangereux. Pour étudier comment cette barrière se forme, se répare et lutte contre les infections, les scientifiques ont besoin de cellules fiables qu’ils peuvent cultiver en laboratoire. Les cultures tridimensionnelles « mini‑intestin » considérées comme référence sont puissantes mais coûteuses, délicates et techniquement exigeantes, ce qui limite leur accès et leur usage. Cette étude présente un ensemble plus pragmatique de lignées cellulaires intestinales de souris conçues pour être faciles à cultiver, génétiquement flexibles et suffisamment proches du tissu réel pour répondre à de nombreuses questions biologiques et pathologiques importantes.
De l’intestin de souris à des cellules compatibles avec le laboratoire
Les chercheurs ont commencé avec de petits segments de l’intestin grêle et du côlon de souris, isolant de petits amas cellulaires incluant des cellules souches intestinales. Ces amas, appelés sphéroïdes, nécessitent normalement un cocktail riche en facteurs de croissance et un support gélifié pour survivre. L’équipe a utilisé un système de délivrance viral pour introduire un gène appelé antigène large T du SV40, qui permet aux cellules de se diviser indéfiniment, créant des lignées « immortalisées ». Ils ont ensuite sevré progressivement les cellules de leurs milieux complexes et du support gélifié, les adaptant à croître en monocouches simples sur des boîtes en plastique standard dans des milieux nutritifs courants. Des clones ont été sélectionnés selon leur apparence — soit plus en nappes épithéliales soit plus de type fibroblastique — et vérifiés exempts de contaminations courantes comme les mycoplasmes. 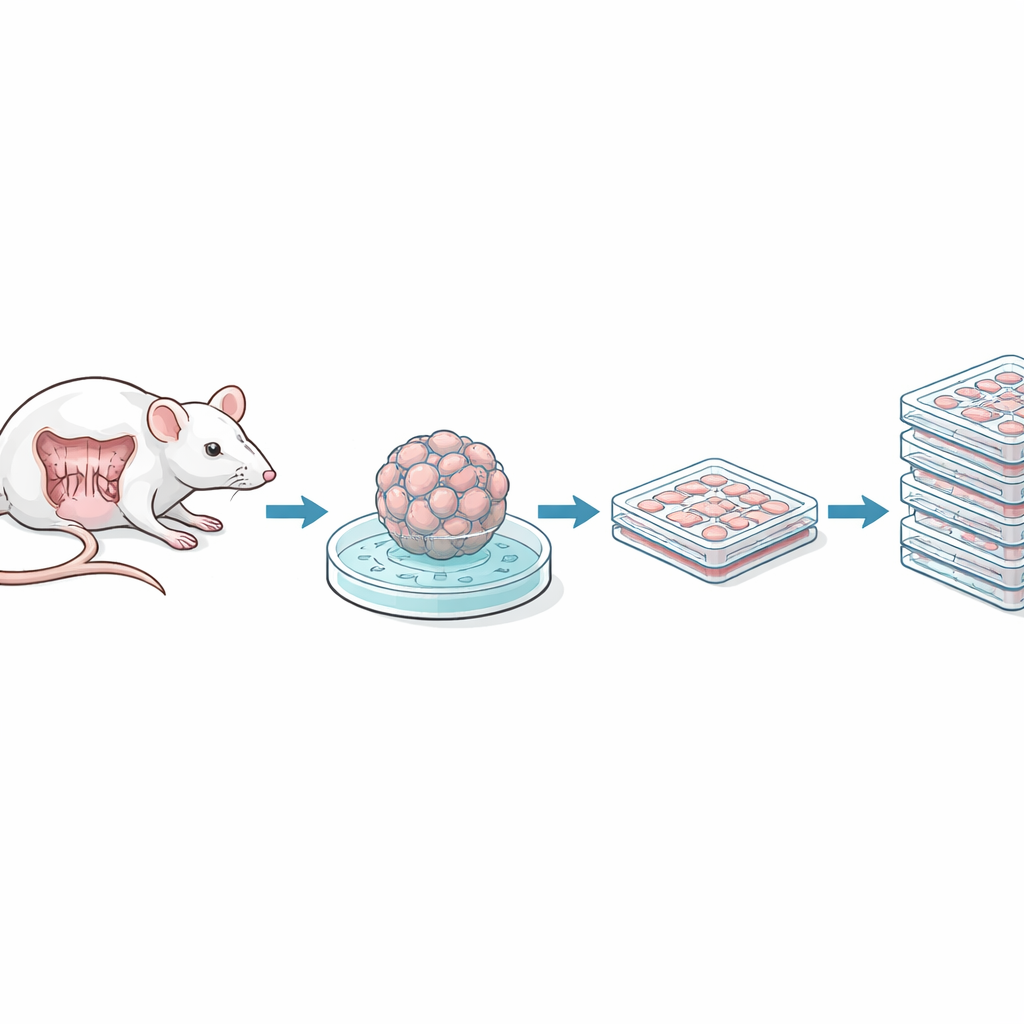
Vérification de l’identité et de la santé génétique
L’immortalisation peut introduire des altérations génétiques indésirables, aussi l’équipe a‑t‑elle soigneusement vérifié ses lignées. Par des méthodes de typage ADN, ils ont montré que les nouvelles lignées correspondaient encore étroitement au tissu d’origine de la souris C57BL/6, et qu’aucun ADN humain ne s’était infiltré. Les étalements chromosomiques ont révélé quelques chromosomes en plus ou réarrangés, comme c’est courant dans les lignées cellulaires de longue durée, mais globalement les nouvelles lignées étaient moins altérées que des lignées de cancer du côlon de souris largement utilisées. Lorsqu’elles ont été cultivées dans un dispositif air–liquide plus exigeant qui favorise normalement la différenciation intestinale complète, les cellules immortalisées ont formé une simple couche basique avec une surface rappelant la bordure en brosse, bien qu’elles ne se soient pas entièrement différenciées en tous les types cellulaires spécialisés présents dans le tissu intestinal natif. Cela suggère qu’elles ressemblent davantage à des cellules progénitrices en division active qu’à des cellules entièrement différenciées.
Personnalité moléculaire : entre épithélium et mode réparation
Pour comprendre ces cellules au niveau de l’expression génique, l’équipe a comparé leurs profils ARN à ceux des sphéroïdes originels et à des types cellulaires intestinaux normaux. Les cellules immortalisées avaient réduit l’expression des marqueurs épithéliaux classiques et augmenté celle de gènes associés à un processus appelé transition épithélio‑mésenchymateuse, au cours duquel les cellules desserrent leurs jonctions et deviennent plus mobiles — un état souvent observé lors de la réparation des plaies et dans le cancer. Pourtant, elles exprimaient toujours de nombreuses protéines jonctionnelles et conservaient des signatures distinctes selon qu’elles provenaient de l’intestin grêle ou du côlon. Dans l’ensemble, les lignées ressemblaient à des cellules progénitrices « à amplification transitoire » — des intermédiaires en division rapide situés entre cellules souches et cellules intestinales matures — suggérant qu’elles modélisent un épithélium orienté vers la régénération et la réparation.
Faciles à reprogrammer et à défier avec des germes
Un avantage majeur de ces nouvelles lignées est leur grande permissivité aux manipulations génétiques et environnementales. Les chercheurs ont pu introduire de l’ADN dans les cellules à l’aide de réactifs de transfection standards ainsi que de vecteurs lentiviraux, produisant des signaux fluorescents robustes. Ils ont ensuite testé dans quelle mesure les cellules modélisent les rencontres hôte–microbe. Lors d’une infection par le virus de la stomatite vésiculaire, les cellules ont permis la réplication virale mais pouvaient être protégées de façon dose‑dépendante en les prétraitant par interféron, un signal antiviral clé. Les mêmes cellules ont rapidement activé des gènes stimulés par l’interféron, confirmant une réponse antivirale intacte. Dans des expériences séparées, les cellules ont permis l’invasion et la survie de bactéries Salmonella et ont réagi aux composés bactériens en activant la voie NF‑κB et en sécrétant une gamme de cytokines et chimiokines inflammatoires, comportements attendus d’une barrière intestinale en alerte. 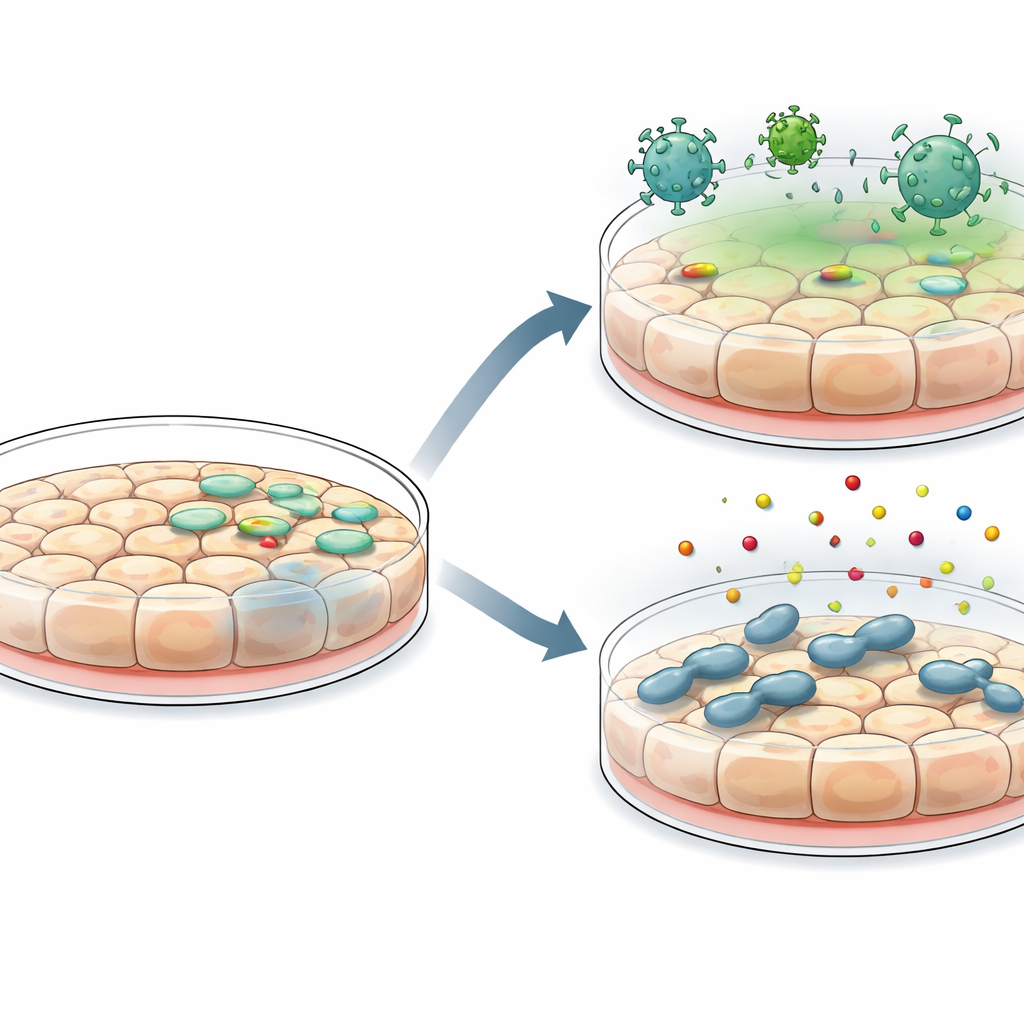
Réduction des coûts et ouverture de possibilités
Parce que ces lignées immortalisées croissent sur du plastique standard dans un milieu simple, elles sont beaucoup moins chères et plus faciles à manipuler que les mini‑intestins tridimensionnels. Les auteurs estiment qu’un criblage de 10 000 composés coûterait des dizaines à des centaines de fois moins cher avec leur système qu’avec des cultures de sphéroïdes ou d’organoïdes primaires, et demanderait moins de temps et de compétences spécialisées. Bien que les cellules ne reproduisent pas parfaitement la diversité et la structure complètes de l’intestin natif et présentent certains traits de transformation partielle, elles remplissent une niche importante : une plateforme basée sur la souris, génétiquement manipulable et physiologiquement informée, adaptée à la découverte à haut débit. En pratique, ces lignées peuvent servir de banc d’essai évolutif et évolutif, dont les résultats prometteurs seront ensuite confirmés dans des cultures mini‑intestins plus complexes ou chez l’animal.
Ce que cela signifie pour la recherche intestinale
En termes simples, l’étude fournit un nouvel ensemble de lignées cellulaires intestinales de souris faciles à cultiver, faciles à modifier et réactives aux virus, bactéries et signaux immunitaires d’une manière qui reflète le tissu intestinal réel. Elles se situent entre des lignées cancéreuses simples mais mal définies et des systèmes d’organoïdes exigeants mais très réalistes. En abaissant les barrières techniques et financières, ces cellules épithéliales intestinales immortalisées sont prêtes à accélérer les études sur le développement intestinal, l’infection, l’inflammation et les réponses aux médicaments, aidant les chercheurs à passer plus rapidement des questions fondamentales à des découvertes qui pourront être testées dans des modèles de plus haute fidélité et, finalement, chez des organismes vivants.
Citation: Zhou, J.Y., Espenschied, S.T., Lu, Q. et al. Development and characterization of immortalized mouse intestinal epithelial cell lines. Sci Rep 16, 8297 (2026). https://doi.org/10.1038/s41598-026-38295-z
Mots-clés: cellules épithéliales intestinales, lignées cellulaires immortalisées, modèles intestinaux de souris, interactions hôte–pathogène, immunité innée