Clear Sky Science · fr
Les réseaux de neurones sur graphes hétérogènes révèlent les mécanismes moléculaires de la carence en folate dans l’insuffisance placentaire par intégration multiomique
Pourquoi cela compte pour les mères et les nourrissons
Le folate est surtout connu comme la vitamine des compléments prénataux qui aide à prévenir les malformations congénitales, mais son rôle dans une grossesse saine est beaucoup plus étendu. Cette étude examine comment un manque de folate peut endommager discrètement le placenta — l’organe qui nourrit et protège le fœtus en développement. En combinant biologie de pointe et intelligence artificielle avancée, les chercheurs montrent comment de subtiles altérations des gènes, des protéines et des petites molécules s’associent pour priver le placenta de ce dont il a besoin, et explorent comment ces connaissances pourraient un jour aider les médecins à repérer plus tôt les grossesses à haut risque.
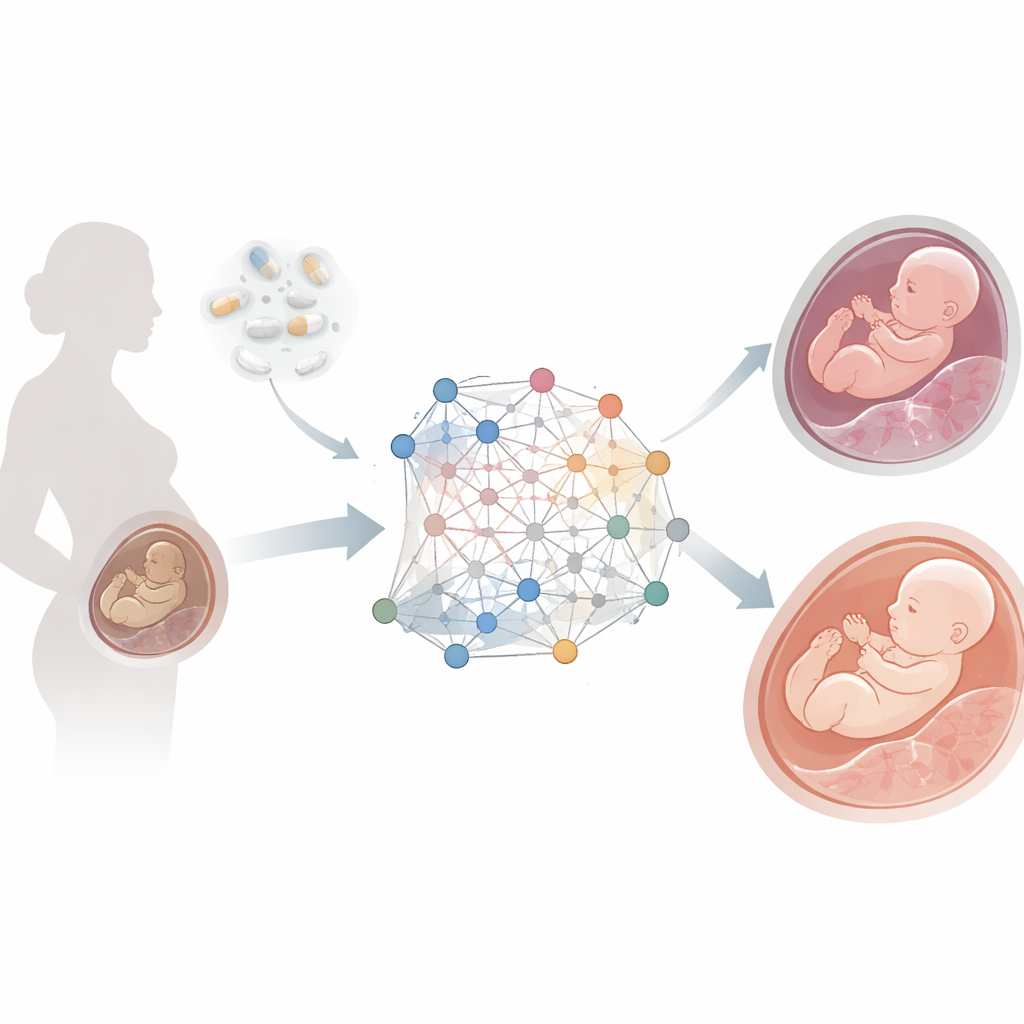
Quand le placenta ne suit plus
L’insuffisance placentaire survient lorsque le placenta n’apporte pas suffisamment d’oxygène et de nutriments au fœtus, entraînant des complications telles qu’un retard de croissance, la prééclampsie et un accouchement prématuré. Elle touche environ cinq à dix pour cent des grossesses dans le monde. Le folate est au cœur de nombreux processus cellulaires — construction de l’ADN, contrôle de l’expression génique et soutien de la santé des vaisseaux sanguins. Lorsque les taux de folate sont trop faibles, ces systèmes peuvent dysfonctionner, mais la chaîne précise d’événements au sein du tissu placentaire a été difficile à reconstituer. Les études traditionnelles examinent généralement un type de données biologiques à la fois, comme les gènes ou les métabolites, manquant ainsi la vue d’ensemble des interactions entre ces niveaux.
Lire le placenta à travers plusieurs lentilles
Pour aborder cette complexité, l’équipe a collecté des échantillons de placenta au moment de l’accouchement chez 156 grossesses présentant une insuffisance placentaire liée au folate et 142 contrôles sains. Pour chaque échantillon, ils ont mesuré quatre types d’informations moléculaires : variations de l’ADN, activité génique, niveaux protéiques et petits métabolites. Plutôt que de traiter ces mesures comme des listes longues et séparées, ils les ont reliées en une grande carte biologique contenant 6 704 molécules et plus de 16 000 interactions connues. Les gènes, protéines et métabolites ont été représentés comme différents types de nœuds connectés par des arêtes reflétant la façon dont ils se lient, se régulent ou se transforment les uns les autres dans des cellules réelles.
Apprendre à un réseau intelligent à repérer les problèmes
Les chercheurs ont ensuite entraîné un modèle d’intelligence artificielle spécialisé, appelé réseau de neurones sur graphes hétérogène, sur cette cartographie moléculaire. Contrairement aux algorithmes classiques qui considèrent chaque mesure isolément, ce modèle « écoute » la façon dont les signaux se propagent à travers l’ensemble du réseau. Il attribue des poids d’attention pour mettre en évidence les molécules et les connexions les plus informatives pour différencier les placentas malades des placentas sains. Sur un jeu de test tenu à part, le modèle a correctement classé 94,7 % des placentas et obtenu une aire sous la courbe ROC quasi parfaite de 0,978, surpassant nettement les méthodes classiques d’apprentissage automatique et toute analyse utilisant un seul type de données. Cela montre que le signal de la maladie ne réside pas seulement dans des marqueurs individuels, mais dans des motifs partagés à travers plusieurs niveaux biologiques.
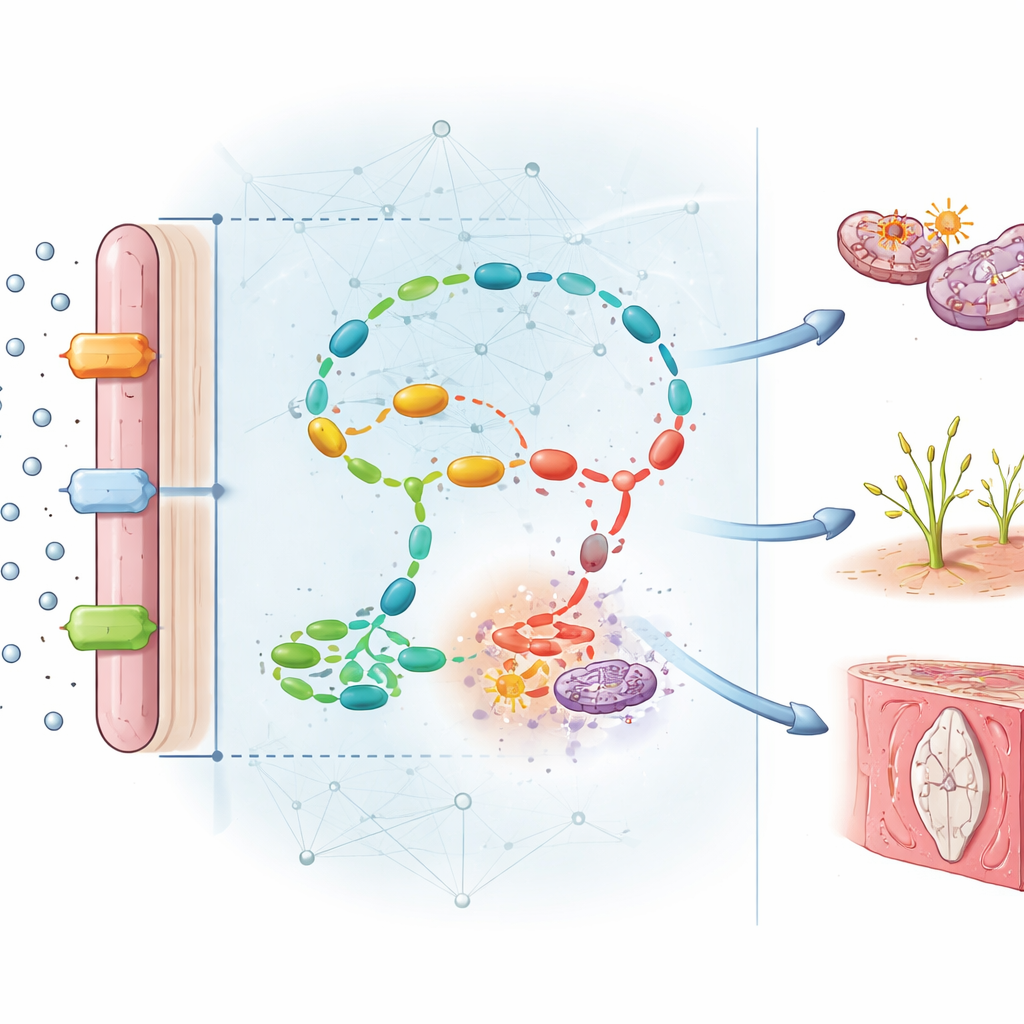
Découvrir les chaînes cachées de dommages
Au-delà de la prédiction, la conception du modèle a permis aux auteurs d’identifier les molécules qui pesaien t le plus dans ses décisions. Plusieurs se sont démarquées. Des composants clés du métabolisme du folate — comme l’enzyme MTHFR et le transporteur de folate FOLR1 — étaient fortement réduits dans les placentas malades, tandis que l’homocystéine, un sous‑produit toxique, s’accumulait plus de six fois. À partir du réseau, sept modules fonctionnels majeurs ont émergé, reliant l’altération du métabolisme du folate à une réduction de la méthylation de l’ADN, une augmentation du stress oxydatif, une croissance vasculaire défaillante, l’inflammation et une mort cellulaire excessive. En d’autres termes, la carence en folate n’endommage pas le placenta d’une seule façon ; elle déclenche un réseau d’échecs interconnectés qui limitent ensemble le flux sanguin et l’apport en nutriments au fœtus.
Ce que cela pourrait signifier pour la prise en charge future
Pour l’instant, ce travail constitue surtout un microscope puissant plutôt qu’un test de chevet. Parce que tous les échantillons ont été prélevés à l’accouchement, le modèle ne peut pas encore être utilisé pour prédire le risque pendant la grossesse, c’est‑à‑dire au moment où une intervention serait la plus utile. Néanmoins, les signatures moléculaires qu’il révèle — en particulier les changements combinés du transport du folate, l’accumulation d’homocystéine et l’altération des voies de croissance vasculaire — offrent une feuille de route pour rechercher des marqueurs sanguins qui pourraient refléter ce qui se passe dans le placenta. Avec des études futures suivant les mères au fil du temps et comparant leur sang à leur tissu placentaire, cette approche pourrait aider à construire des outils de dépistage précoces non invasifs et des stratégies nutritionnelles ou médicales plus ciblées pour protéger les grossesses vulnérables.
Citation: Xie, X., Li, Z., Xiao, Q. et al. Heterogeneous graph neural networks reveal molecular mechanisms of folate deficiency in placental insufficiency through multiomics integration. Sci Rep 16, 8417 (2026). https://doi.org/10.1038/s41598-026-38288-y
Mots-clés: insuffisance placentaire, carence en folate, réseaux de neurones sur graphes, multiomique, complications de la grossesse