Clear Sky Science · fr
La dexmédétomidine atténue la stéatose hépatique associée à la dysfonction métabolique induite par un régime riche en graisses chez le rat en régulant la voie de l'autophagie
Pourquoi cela compte pour la santé quotidienne
Alors que les tours de taille augmentent dans le monde, un problème silencieux se développe à l’intérieur de nombreux organismes : des foies chargés de lipides qui peuvent évoluer vers des maladies graves. Cette étude examine si un sédatif hospitalier, la dexmédétomidine, peut également agir comme un protecteur hépatique surprenant chez des rats nourris avec un régime riche en graisses. En stimulant le système naturel de « nettoyage » du foie, le médicament a semblé limiter l’accumulation de graisses, les dommages oxydatifs et la mort cellulaire — ce qui indique une piste possible pour lutter contre une maladie moderne très répandue.
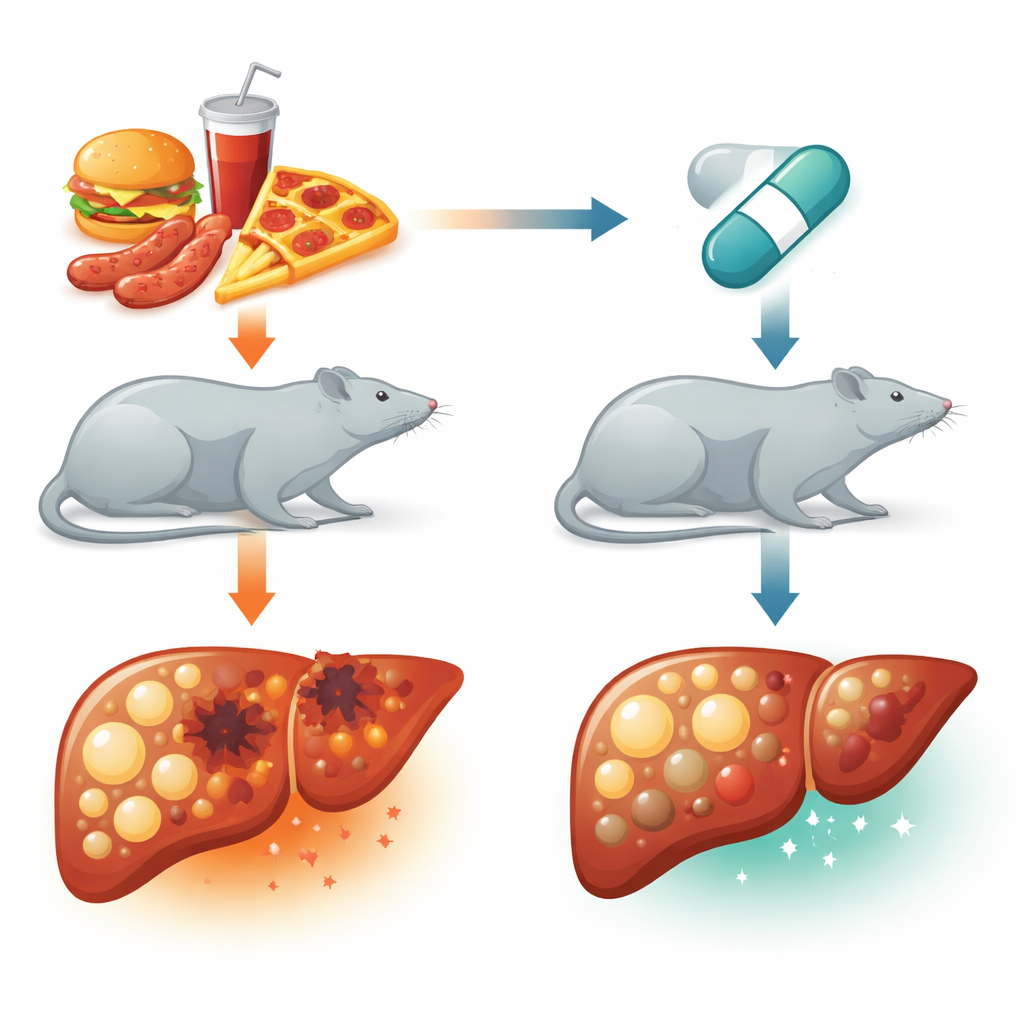
Trop de graisses, un foie stressé
Le foie est une plaque tournante centrale pour le métabolisme des lipides : il les conditionne, les brûle pour produire de l’énergie et les distribue dans l’organisme. Lorsque ce système est submergé — souvent par une consommation prolongée d’aliments riches en calories et en graisses — des gouttelettes lipidiques commencent à s’accumuler dans les hépatocytes. Cette affection, désormais appelée maladie hépatique stéatosique associée à la dysfonction métabolique (MASLD), touche environ un quart de la population mondiale et est étroitement liée à l’obésité, au diabète, à l’hypertension et aux troubles lipidiques sanguins. Avec le temps, une simple accumulation de graisses peut évoluer vers l’inflammation, la fibrose et même la cirrhose. Une idée centrale dans le domaine est la théorie des « deux coups » : d’abord l’excès de graisse s’accumule ; ensuite, le stress et les dommages des machineries cellulaires déclenchent inflammation et lésions supplémentaires.
L’équipe de nettoyage de la cellule : recycler les graisses de l’intérieur
Pour contrer ces agressions, les hépatocytes comptent sur l’autophagie — un processus de recyclage intégré dans lequel les composants usés et les gouttelettes de graisse en surplus sont enveloppés dans de petites membranes et livrés aux compartiments « digestifs » cellulaires. Une forme spécialisée, appelée lipophagie, cible spécifiquement les gouttelettes lipidiques. Lorsqu’elle fonctionne correctement, la lipophagie dégrade les graisses stockées en molécules plus petites qui peuvent être oxydées pour produire de l’énergie, tout en éliminant des structures endommagées qui génèrent des espèces réactives de l’oxygène. Quand ce mécanisme interne ralentit, les graisses et les sous-produits toxiques s’accumulent, favorisant la progression de la MASLD. Dans cette étude, les chercheurs se sont concentrés sur plusieurs sentinelles moléculaires bien connues qui reflètent l’activité de ce système, notamment des protéines impliquées dans le déclenchement de l’autophagie et le marquage du matériel à dégrader.
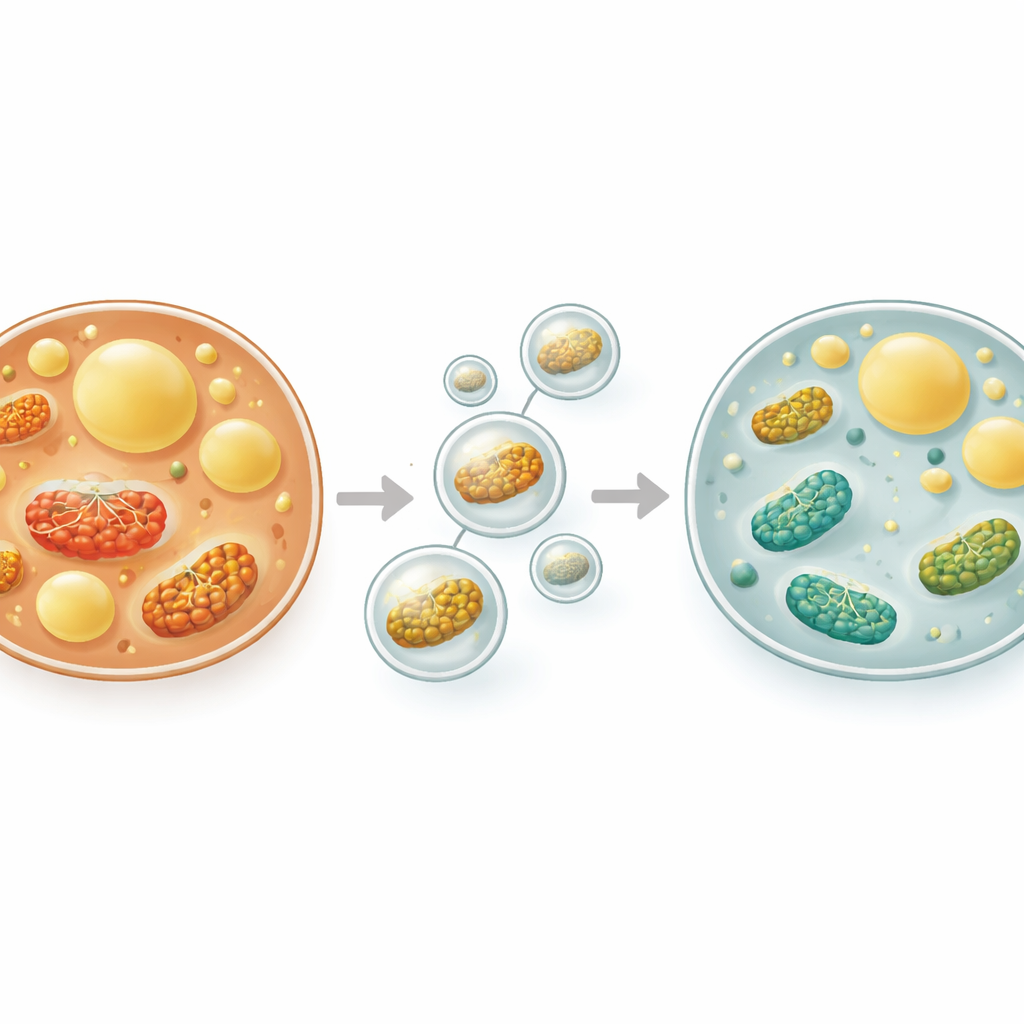
Tester un sédatif comme bouclier hépatique chez le rat
L’équipe a utilisé des rats mâles et les a nourris pendant huit semaines avec un régime dont 60 % des calories provenaient de suif de bœuf, déclenchant de manière fiable une stéatose hépatique et des perturbations métaboliques. Deux groupes de ces rats alimentés richement en graisses ont également reçu des injections quotidiennes de dexmédétomidine à faibles ou fortes doses, tandis que les rats témoins consommaient une alimentation standard. À la fin de l’expérience, les scientifiques ont mesuré des marqueurs sanguins de lésion hépatique, le cholestérol et les triglycérides, des signes chimiques de stress oxydatif, et les niveaux de protéines clés liées à l’autophagie dans le tissu hépatique. Ils ont aussi examiné des coupes fines du foie au microscope et utilisé des méthodes de coloration pour visualiser des protéines liées à la survie cellulaire ou à la mort cellulaire programmée.
Des foies plus propres, des cellules plus calmes
Les rats soumis uniquement au régime riche en graisses ont développé des modifications lipidiques sévères du foie : de grandes gouttelettes de graisse encombraient les cellules, les tests sanguins de lésion hépatique ont fortement augmenté, et le stress oxydatif a grimpé alors que les antioxydants protecteurs diminuaient. Parallèlement, les signatures moléculaires de l’autophagie ont été fortement supprimées, et des protéines qui s’accumulent lorsque ce système est bloqué sont devenues abondantes. Les marqueurs d’apoptose, tels que la caspase-3, ont augmenté, tandis que des protéines protectrices comme Bcl-2 ont diminué. En contraste saisissant, les rats traités par dexmédétomidine ont montré des améliorations dépendant de la dose. Leurs foies contenaient beaucoup moins de graisse visible, et les taux sanguins d’enzymes hépatiques, de cholestérol total et de triglycérides ont chuté vers la normale. À l’intérieur des hépatocytes, les défenses antioxydantes se sont améliorées et la peroxydation lipidique délétère a diminué. Surtout, les protéines qui déclenchent et exécutent l’autophagie ont rebondi, tandis que la protéine « d’embouteillage » p62 a diminué, indiquant que la machinerie de nettoyage avait non seulement été activée mais fonctionnait. Simultanément, les niveaux de caspase-3 ont baissé et Bcl-2 a augmenté, suggérant que moins de cellules subissaient la mort programmée.
Ce que ces résultats pourraient signifier
Dans l’ensemble, les résultats suggèrent que la dexmédétomidine aide le foie gras et stressé en réactivant ses systèmes internes de recyclage — en particulier la voie qui dégrade les gouttelettes lipidiques — et en réduisant les lésions oxydatives et la perte cellulaire. Dans ce modèle animal, le médicament a orienté le foie loin d’une trajectoire d’aggravation de l’accumulation lipidique et des dommages, vers un état qui se rapproche davantage de la santé. Bien que ces observations ne signifient pas que le sédatif soit prêt à être utilisé comme traitement chez l’humain atteint de MASLD, elles mettent en évidence une stratégie prometteuse : soutenir les outils internes de nettoyage et de réparation du foie pour contrer les effets des régimes riches en graisses et de la dysfonction métabolique.
Citation: Ezzat, S.M., Sharawy, M.H. & Suddek, G.M. Dexmedetomidine attenuates high-fat diet-induced metabolic dysfunction-associated steatotic liver disease in rats by regulating the autophagic pathway. Sci Rep 16, 8943 (2026). https://doi.org/10.1038/s41598-026-38250-y
Mots-clés: maladie du foie gras, régime riche en graisses, autophagie, dexmédétomidine, stress oxydatif