Clear Sky Science · fr
Améliorer la sécurité diagnostique avec une classification CTPA à faible iode et faible radiation via l’apprentissage profond
Examens plus sûrs pour un caillot pulmonaire dangereux
L’embolie pulmonaire est une obstruction soudaine des vaisseaux sanguins des poumons qui peut être rapidement fatale si elle est manquée. Les médecins s’appuient sur un scanner spécial, appelé angiographie pulmonaire par tomodensitométrie (CTPA), pour repérer ces caillots. Mais les examens les plus fiables aujourd’hui utilisent souvent des doses relativement élevées de rayons X et un produit de contraste à base d’iode, ce qui peut solliciter les reins et augmenter le risque de cancer au cours de la vie. Cette étude examine si l’intelligence artificielle (IA) moderne peut préserver l’exactitude vitale de la CTPA tout en utilisant beaucoup moins de radiation et de produit de contraste, rendant potentiellement ces examens plus sûrs pour les patients vulnérables.
Pourquoi les scanners actuels impliquent un compromis
La CTPA standard produit des images nettes des vaisseaux pulmonaires en combinant des faisceaux de rayons X puissants avec une dose généreuse de contraste iodé, qui fait ressortir les vaisseaux sur l’image. Cette clarté aide les radiologues à voir de petits caillots mais a un coût : les examens répétés peuvent contribuer à l’exposition cumulative aux radiations, et le produit de contraste peut nuire aux patients ayant des reins fragiles ou des problèmes cardiaques. Lorsque les équipes de radiologie tentent de réduire la radiation ou l’iode, les images deviennent granuleuses et sombres, rendant les caillots subtils difficiles à distinguer de l’anatomie normale. Les algorithmes classiques, et même de nombreux outils d’apprentissage profond, ont été conçus pour des examens à pleine dose et ont tendance à peiner lorsque la qualité d’image diminue.
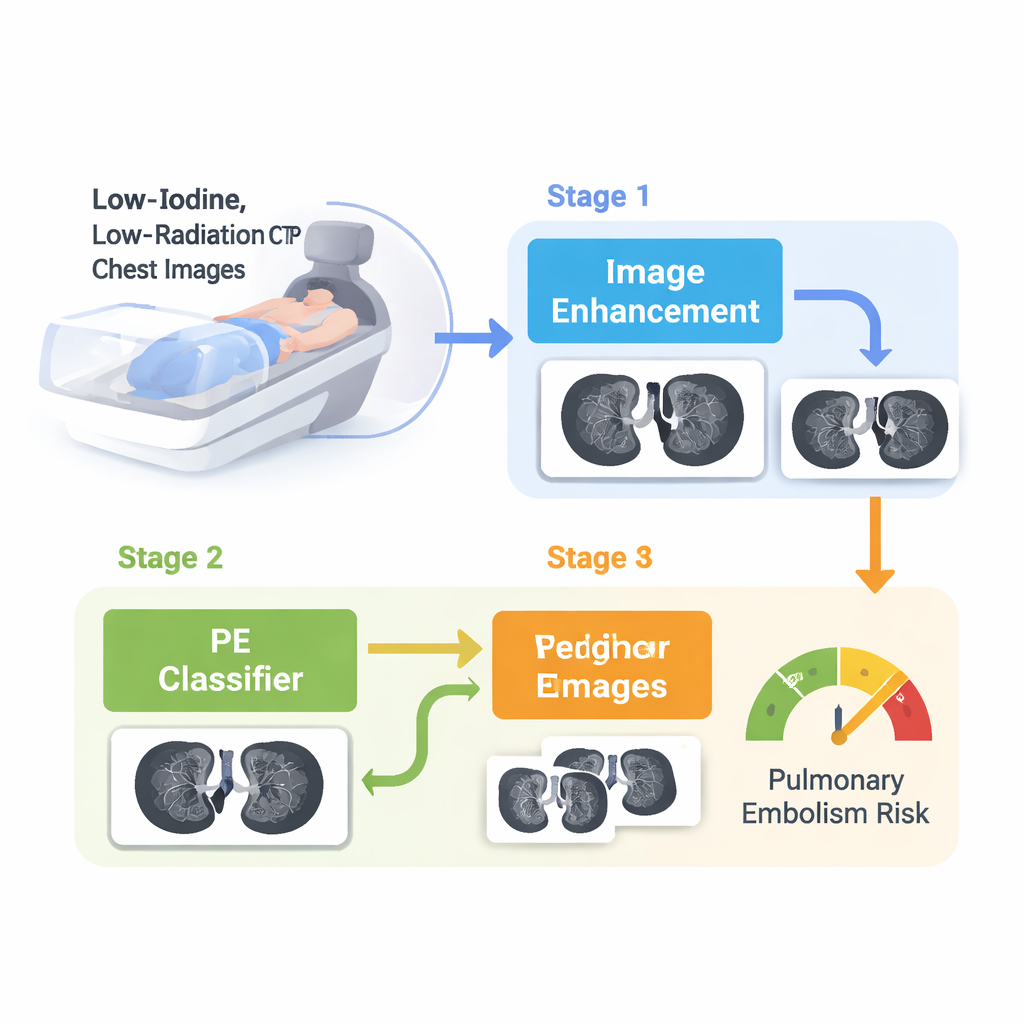
Un assistant IA en deux étapes pour l’imagerie à faible dose
Les auteurs ont conçu un cadre d’IA en deux étapes spécifiquement adapté à la CTPA à faible iode et faible radiation. Dans la première étape, un réseau « d’amélioration d’image » aiguise les scanners flous et bruyants. Il fonctionne en analysant à la fois les motifs de pixels usuels et leur contenu fréquentiel sous‑jacent — séparant essentiellement les bords fins, les contours des vaisseaux et les textures subtiles du bruit de fond — puis en renforçant les détails importants tout en supprimant l’encombrement. Dans la seconde étape, un classificateur « à double branche » examine côte à côte l’image à faible dose d’origine et sa version améliorée. Une branche se concentre sur la structure globale du thorax, tandis que l’autre zoome sur les détails fins des vaisseaux. Le système fusionne ensuite ces deux perspectives via un mécanisme d’attention qui apprend quand faire davantage confiance à l’une ou l’autre branche.
Un nouveau jeu de données réel et la façon dont il a été testé
Pour rendre cette approche cliniquement pertinente, l’équipe a constitué un nouveau jeu de données de 191 patients adultes examinés à l’hôpital de Pékin en utilisant une radiation délibérément réduite et seulement 30 millilitres de contraste iodé — nettement moins que les 50–100 millilitres souvent utilisés dans les protocoles standards. Des radiologues expérimentés ont étiqueté chaque cas et, pour un sous‑ensemble, ont minutieusement tracé les coupes contenant des caillots. Les chercheurs ont également créé des images simulées à faible dose à partir d’un grand jeu de données public pour pré‑entraîner leurs modèles avant un ajustement fin sur les véritables scans à faible exposition. Ils ont ensuite mesuré les performances à l’aide de métriques diagnostiques standard telles que la sensibilité (quel pourcentage de vrais caillots est détecté), la spécificité (combien de fausses alertes sont évitées) et l’aire sous la courbe ROC, un résumé de la précision globale.
Images plus nettes et détection de caillots plus fiable
Le réseau d’amélioration a, à lui seul, produit des images de vaisseaux plus claires que plusieurs méthodes bien connues de super‑résolution, en préservant les structures fines tout en limitant les détails artificiels « hallucinés ». Pourtant, l’utilisation uniquement des scans améliorés pour le diagnostic n’a pas surpassé l’utilisation des images brutes à faible dose, car l’aiguisage peut parfois exagérer des motifs bénins qui imitent une maladie. Le véritable progrès provient de la conception à double branche : en combinant la stabilité des images originales avec le supplément de détail des images améliorées, le système a atteint une aire sous la courbe ROC élevée de 0,928, avec une sensibilité et une spécificité équilibrées. Il est également resté robuste lorsque du bruit supplémentaire a été ajouté, suggérant qu’il peut faire face aux conditions imparfaites de l’imagerie à faible dose en milieu réel.
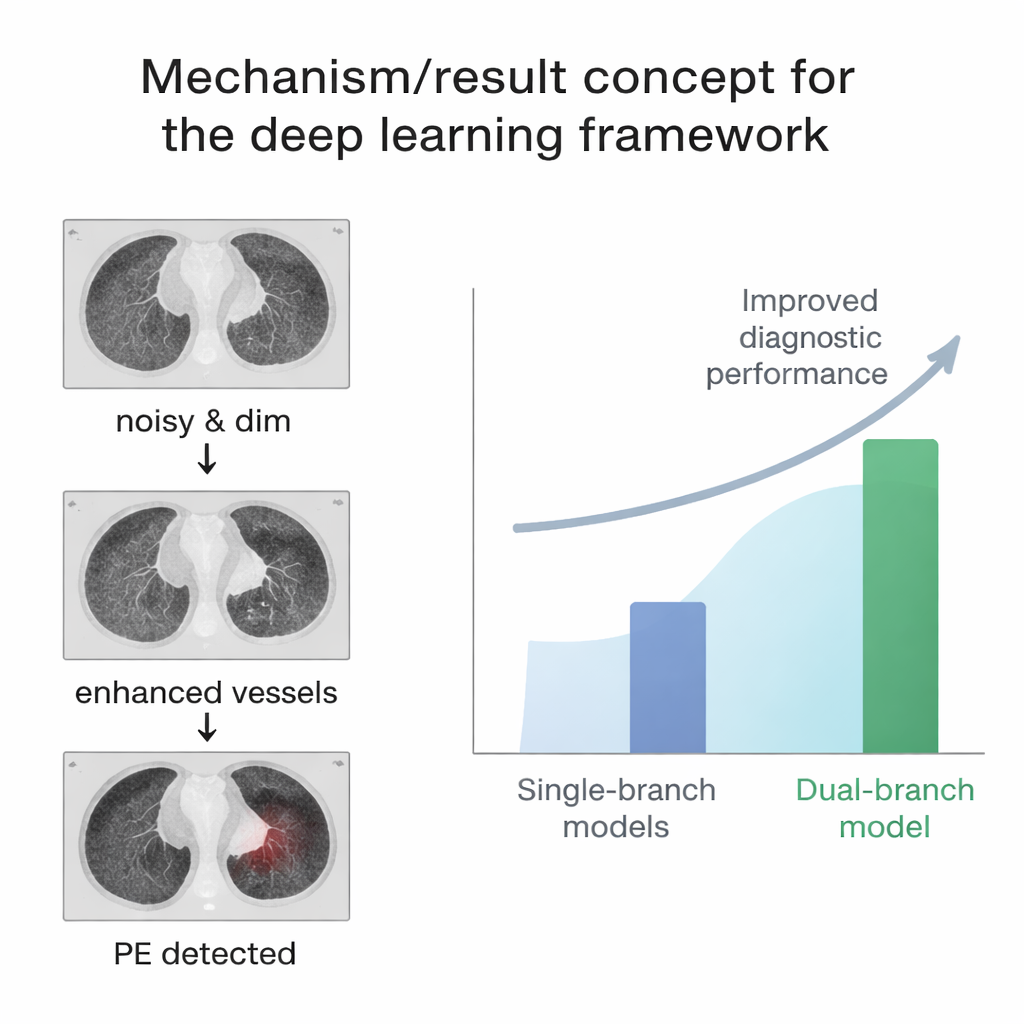
Ce que cela pourrait signifier pour les patients
Pour les patients, le message principal est que l’IA pourrait aider à rendre plus sûrs les examens essentiels pour l’embolie pulmonaire sans sacrifier la fiabilité. L’étude montre qu’un système d’IA conçu avec soin et conscient de la tâche peut compenser une partie de la perte de qualité associée à une moindre radiation et à moins de contraste iodé. Cela pourrait être particulièrement précieux pour les personnes qui nécessitent des examens répétés, ou dont les reins ou l’état de santé général rendent les doses standard de contraste risquées. Bien que des tests plus larges à travers plusieurs hôpitaux et types de scanners restent nécessaires, ce travail ouvre la voie vers un avenir où la détection de caillots vitale peut être réalisée avec des protocoles CT plus doux et plus respectueux des patients.
Citation: Hong, M., Gu, T., An, H. et al. Enhancing diagnostic safety with low iodine, low radiation CTPA classification using deep learning. Sci Rep 16, 7205 (2026). https://doi.org/10.1038/s41598-026-38223-1
Mots-clés: embolie pulmonaire, CT à faible dose, angiographie pulmonaire par CT, IA en imagerie médicale, réduction d’agent de contraste