Clear Sky Science · fr
L’inhibition de PERK atténue la mort cellulaire multi-programmes via l’activation Nrf2/HO-1 dans la rétinopathie diabétique avec protéomique intégrée et validation fonctionnelle dans des HRECs
Pourquoi protéger la vue chez les personnes diabétiques est crucial
Pour des millions de personnes vivant avec le diabète, l’une des complications les plus redoutées est la perte progressive de la vision appelée rétinopathie diabétique. Cette atteinte du tissu photosensible au fond de l’œil débute souvent de manière silencieuse, bien avant l’apparition des symptômes. L’étude à l’origine de cet article examine ce qui tue réellement les petits vaisseaux sanguins qui maintiennent la rétine en bonne santé — et teste une nouvelle stratégie pour les protéger. En comprenant et en calmant les « réponses au stress » cellulaires déclenchées par l’hyperglycémie, les chercheurs espèrent ralentir voire prévenir la cécité chez les personnes diabétiques.
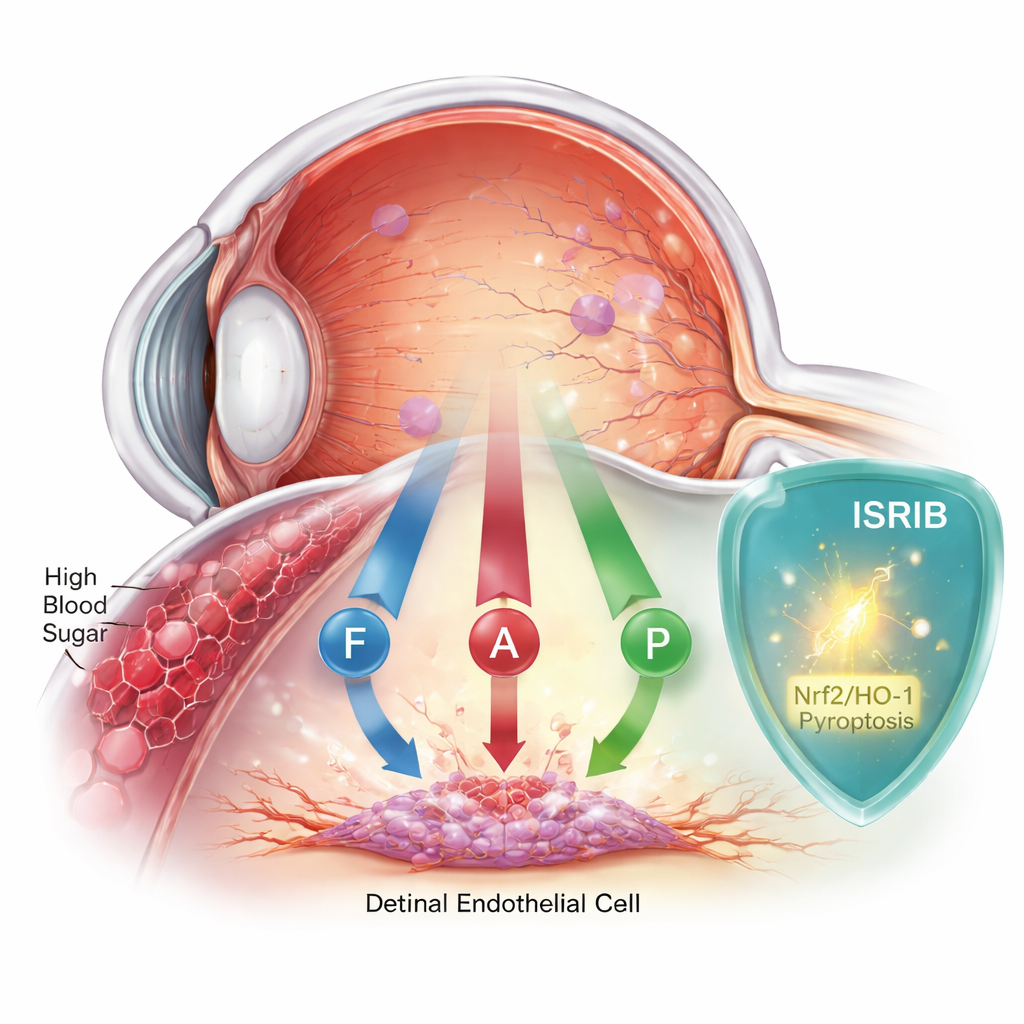
Quand le sucre blesse silencieusement l’œil
La rétinopathie diabétique commence lorsque l’hyperglycémie endommage l’endothélium délicat des vaisseaux rétiniens. Ces cellules forment une barrière qui maintient la rétine nourrie et protégée. Pendant des années, les scientifiques ont pensé qu’une seule forme de mort cellulaire, l’apoptose, était principalement en cause. Mais les preuves s’accumulent pour montrer que l’histoire est plus complexe. L’équipe s’est concentrée sur des cellules endothéliales rétiniennes humaines cultivées en laboratoire, exposées à des concentrations de sucre similaires à celles observées dans le diabète mal contrôlé, puis a observé leurs réponses sur deux jours.
Trois façons dont les cellules peuvent mourir simultanément
Grâce à une puissante technique de mesure des protéines appelée protéomique, les chercheurs ont constaté que des taux élevés de sucre perturbaient des centaines de protéines, en particulier celles impliquées dans les réponses au stress, le métabolisme et la gestion du fer. Des tests complémentaires ont montré que les cellules ne mouraient pas d’une seule manière, mais de trois : la mort programmée classique (apoptose), une forme enflammatoire (pyroptose) et une forme plus récente liée au fer nommée ferroptose. Les marqueurs de dommages oxydatifs, de surcharge en fer et d’antioxydants épuisés ont augmenté, tandis que les enzymes protectrices ont diminué. Ensemble, ces changements dessinaient le portrait de cellules submergées par le stress, l’inflammation et l’accumulation toxique de molécules réactives.
Un interrupteur de stress au cœur du problème
L’équipe s’est ensuite intéressée à un senseur de stress clé à l’intérieur des cellules appelé PERK, situé sur la membrane du réticulum endoplasmique, une structure qui aide au repliement et au traitement des protéines. En condition d’hyperglycémie, PERK est devenu hyperactif, agissant comme une alarme d’urgence bloquée qui ne cesse de retentir. Cela semblait alimenter les trois programmes de mort. Parallèlement, un système de défense naturel qui aide normalement les cellules à gérer les dommages oxydatifs — la voie antioxydante Nrf2/HO-1 — était affaibli. En termes simples, les signaux de danger étaient amplifiés tandis que les extincteurs internes étaient désactivés.
Réduire le stress, augmenter la protection
Pour savoir s’ils pouvaient rompre ce cercle vicieux, les chercheurs ont traité les cellules exposées au sucre élevé avec ISRIB, une petite molécule qui atténue efficacement la signalisation de stress via PERK. Les résultats furent frappants. ISRIB a amélioré la survie cellulaire, réduit les marqueurs des dommages liés au fer et au stress oxydatif, et diminué les signes chimiques d’apoptose et de pyroptose. Parallèlement, il a renforcé la voie de défense Nrf2/HO-1, aidant les cellules à restaurer leur capacité antioxydante. Un autre médicament bloquant spécifiquement la ferroptose a également été utile, mais ISRIB s’est distingué en calmant les trois voies de mort à la fois plutôt qu’une seule.
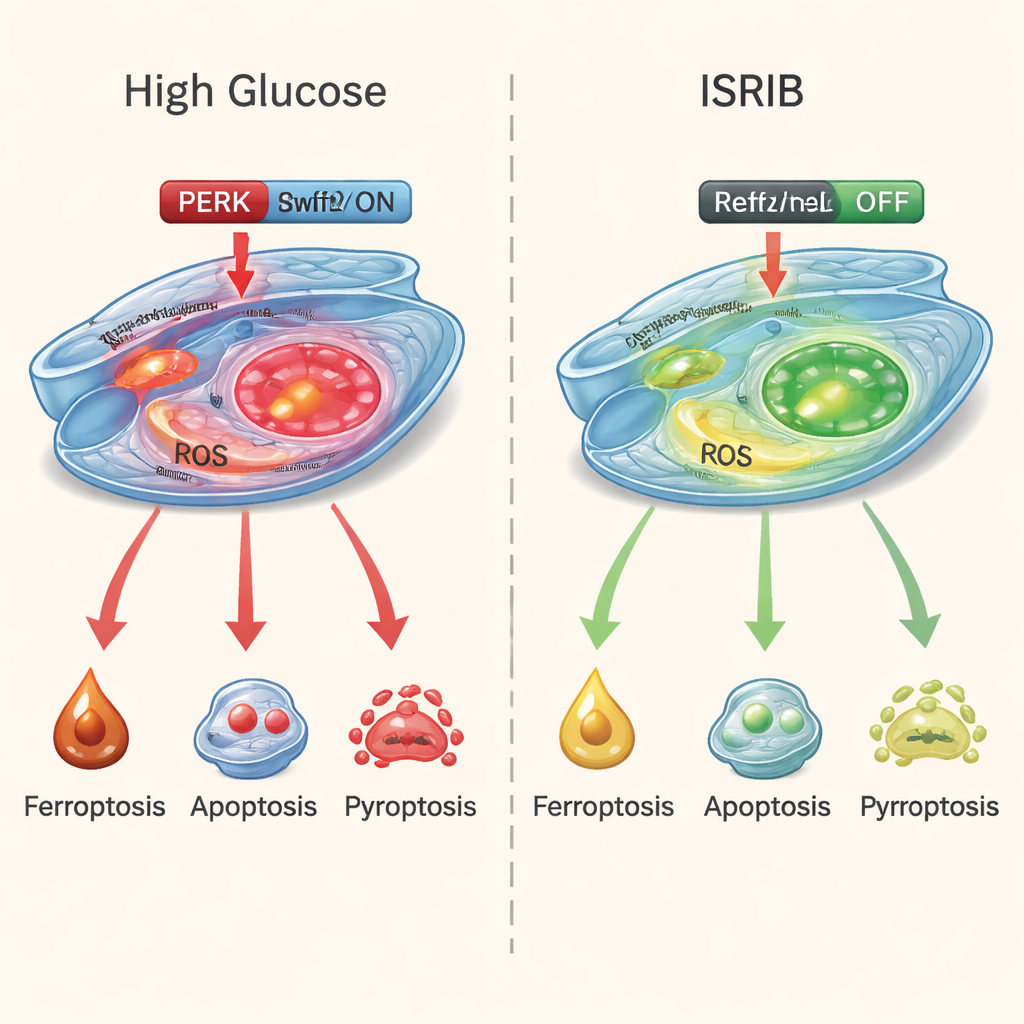
Ce que cela pourrait signifier pour les personnes diabétiques
Ce travail suggère que les lésions précoces dans la rétinopathie diabétique ne sont pas causées par un seul « coupable », mais par la convergence de plusieurs programmes de mort auto‑amplifiants entraînés par un stress cellulaire chronique. En abaissant l’interrupteur de stress PERK et en réactivant les systèmes de protection propres à la cellule, des médicaments comme ISRIB pourraient offrir une approche plus unifiée pour préserver les vaisseaux rétiniens. Bien que ces expériences aient été menées sur des cellules et non encore chez des patients, elles orientent vers des traitements futurs ciblant les réponses au stress à l’intérieur de l’œil — ajoutant potentiellement une nouvelle couche de protection aux contrôles glycémiques et aux injections intraoculaires actuelles pour aider à préserver la vision chez les personnes diabétiques.
Citation: Xie, L., Zhang, X., Tian, M. et al. PERK inhibition attenuates multi-program cell death through Nrf2/HO-1 activation in diabetic retinopathy with integrated proteomics and functional validation in HRECs. Sci Rep 16, 7225 (2026). https://doi.org/10.1038/s41598-026-38213-3
Mots-clés: rétinopathie diabétique, mort cellulaire rétinienne, stress oxydatif, voie PERK, Nrf2 HO-1