Clear Sky Science · fr
Inhibition de la voie SHH et co-culture avec des astrocytes induisent des réponses distinctes dans le glioblastome et les cellules souches cancéreuses
Pourquoi les tumeurs cérébrales sont si difficiles à traiter
Le glioblastome est l’un des cancers du cerveau les plus meurtriers, et même avec la chirurgie, la radiothérapie et la chimiothérapie, seule une infime fraction des patients survit au-delà de cinq ans. Une des raisons est que ces tumeurs ne sont pas composées d’un seul type de cellule. Elles contiennent un petit groupe de « cellules souches cancéreuses » particulièrement tenaces qui peuvent survivre aux traitements et permettre à la tumeur de repousser. Cette étude pose une question clé : comment ces différents types cellulaires tumoraux réagissent‑ils lorsqu’un signal stimulant la croissance est bloqué, et comment la présence de cellules cérébrales normales de soutien, les astrocytes, modifie‑t‑elle cette réponse ?
Un regard plus approfondi sur les cellules les plus résistantes de la tumeur
Les chercheurs ont travaillé avec deux types cellulaires principaux d’un modèle courant de glioblastome : les cellules de la masse tumorale et une petite sous‑population marquée par une protéine appelée CD133, qui se comporte comme des cellules souches cancéreuses. Ces cellules de type souches se divisaient moins, paraissaient plus petites et plus rondes, et formaient des amas plus compacts que les cellules de la masse tumorale. L’équipe a également cultivé les cellules tumorales en présence d’astrocytes, ces cellules étoilées qui contribuent au maintien du tissu cérébral sain. Cette culture mixte mime mieux le véritable environnement tumoral, où les cellules cancéreuses « dialoguent » en permanence avec leurs voisines. 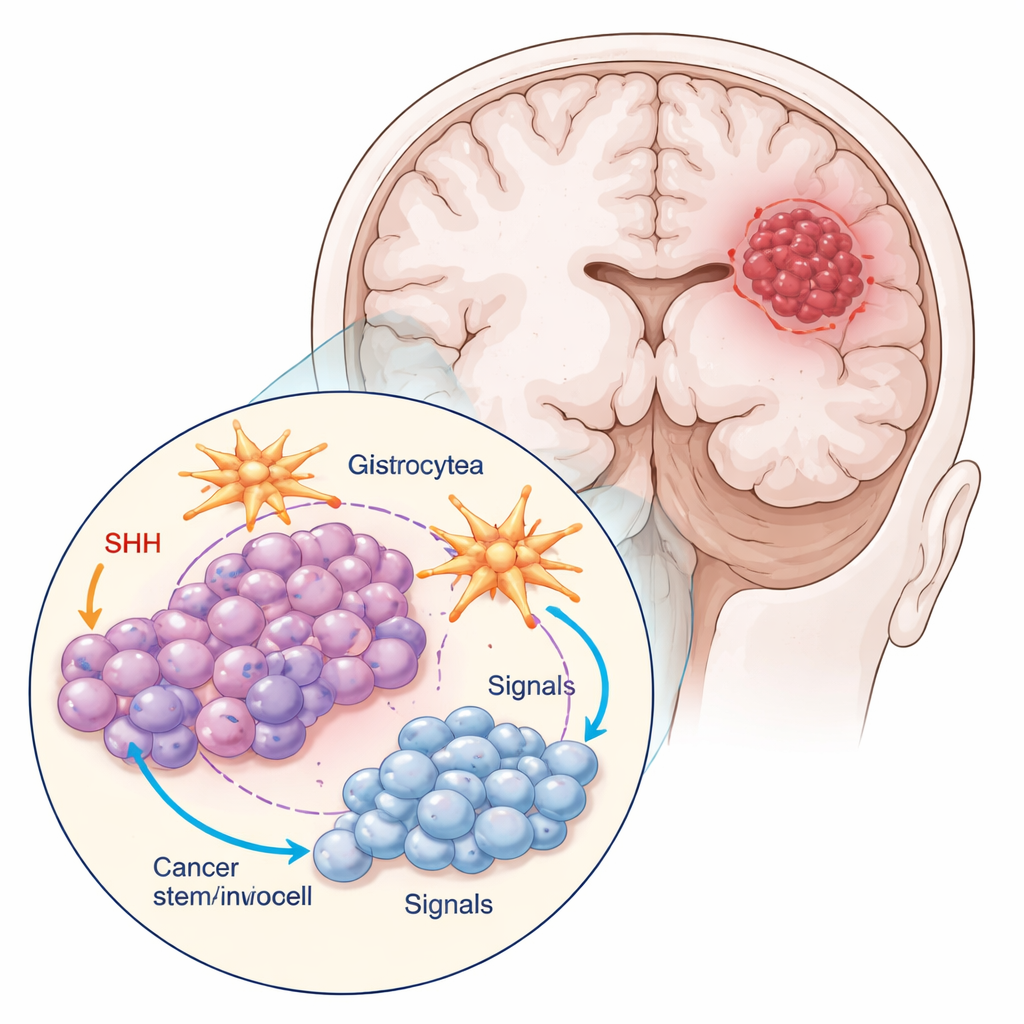
Bloquer un signal de développement réutilisé par les tumeurs
De nombreux glioblastomes, en particulier leurs cellules de type souches, détournent une voie de communication moléculaire appelée Sonic Hedgehog (SHH), normalement active pendant le développement cérébral. L’équipe a utilisé la cyclopamine, un composé qui bloque un composant clé de la voie SHH, pour observer comment les cellules de la masse tumorale et les cellules souches cancéreuses réagissaient. Ils ont mesuré l’activité des gènes et protéines liés à SHH, la vitesse de progression du cycle cellulaire et la fréquence d’apoptose (mort cellulaire programmée). La cyclopamine a modifié la signalisation SHH d’une manière fortement dépendante du type cellulaire et de la présence d’astrocytes. Les cellules souches cancéreuses produisaient le plus de signal SHH lorsqu’elles étaient cultivées seules, mais cette sécrétion a diminué quand elles étaient en co‑culture avec des astrocytes et exposées au médicament, suggérant que les cellules cérébrales environnantes peuvent atténuer l’« auto‑soutien » chimique de la tumeur.
Comment le voisinage influe sur croissance et mort
Au‑delà de SHH lui‑même, l’équipe a suivi d’autres réseaux géniques qui déterminent si les cellules continuent à se diviser, s’arrêtent ou commencent à se spécialiser. Dans des cultures simples ne contenant que la tumeur, le blocage de SHH poussait les cellules de la masse tumorale vers un arrêt tardif de la division (phase G2/M), tandis que les cellules de type souches avaient tendance à s’accumuler plus tôt, en phase de repos ou d’entrée (G0/G1). Lorsque des astrocytes étaient ajoutés, ces schémas ont changé : les cellules souches, qui étaient plus quiescentes, basculaient vers un arrêt en G2/M, impliquant un ensemble différent de « freins » appliqués dans l’environnement mixte. Les chercheurs ont également observé que des signaux liés au destin cellulaire et à la morphogenèse—comme les voies WNT, BMP et TGF‑β—étaient modulés différemment dans les cellules de la masse et les cellules de type souches en présence d’astrocytes, ce qui signifie que le microenvironnement peut incliner les cellules soit vers un comportement stem‑like maintenu, soit vers un état plus différencié et moins agressif.
Déclencher la mort des cellules les plus résistantes
L’étude a également examiné la propension des cellules à subir l’apoptose. Les données génétiques et un test de détection des dommages à l’ADN (test TUNEL) ont montré que la cyclopamine favorisait une voie « extracellulaire » de mort cellulaire, orchestrée par une protéine appelée CASP8, en particulier dans la population de cellules souches cancéreuses. Fait intéressant, dans les cellules tumorales cultivées seules, la mortalité globale a parfois diminué après le blocage de SHH, suggérant que ces cellules pouvaient activer des stratégies de survie de rechange. En revanche, lorsque les cellules de type souches étaient en co‑culture avec des astrocytes, la cyclopamine augmentait les marqueurs d’apoptose, indiquant que les cellules cérébrales environnantes peuvent rendre ces cellules autrement résistantes plus vulnérables une fois la signalisation SHH bloquée. 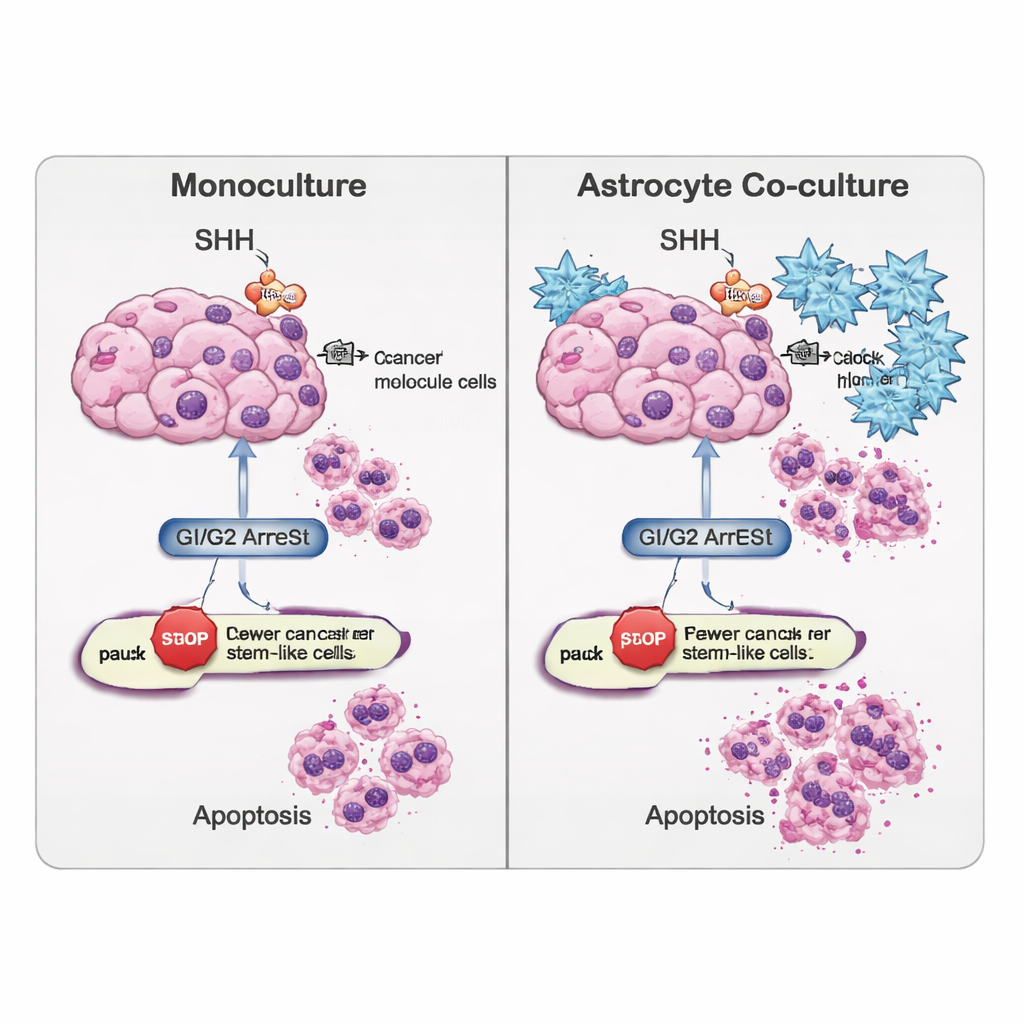
Ce que cela signifie pour les traitements futurs des cancers cérébraux
Pour un non‑spécialiste, le message principal est que cibler un seul signal de croissance dans le glioblastome ne suffit pas si l’on ignore le voisinage tumoral. Ce travail montre que les astrocytes—les cellules normales partageant l’espace avec la tumeur—peuvent modifier profondément la façon dont les cellules de la masse et les cellules souches cancéreuses réagissent au blocage de la voie SHH. Les cellules souches cancéreuses, en particulier, devenaient plus sujettes à l’arrêt du cycle cellulaire et à une forme de mort cellulaire en présence d’astrocytes. Les auteurs concluent que les médicaments ciblant SHH et les voies associées ont plus de chances de fonctionner s’ils sont testés et finalement utilisés dans des conditions reflétant le véritable environnement cérébral, possiblement en association avec d’autres traitements qui s’attaquent aux voies de survie de secours de la tumeur. En bref, comprendre et exploiter la « conversation » entre les cellules tumorales et leurs voisines pourrait ouvrir des stratégies plus précises et durables contre ce cancer par ailleurs implacable.
Citation: Kocaturk, D.C., Ozdil, B., Adali, Y. et al. SHH pathway inhibition and astrocyte co-culture induce distinct responses in glioblastoma and cancer stem cells. Sci Rep 16, 7712 (2026). https://doi.org/10.1038/s41598-026-38199-y
Mots-clés: glioblastome, cellules souches cancéreuses, voie Sonic Hedgehog, microenvironnement tumoral, astrocytes