Clear Sky Science · fr
Identification et validation d’un nouveau signature génique liée à la ferroptose associée à la dégénérescence rétinienne héréditaire chez la souris Rd10
Pourquoi la mort des cellules oculaires nous concerne tous
La rétinite pigmentaire regroupe des maladies oculaires héréditaires qui volent progressivement la vue des personnes, commençant souvent par une cécité nocturne et aboutissant à une perte de vision complète. Il n’existe pas de remède, et les thérapies géniques actuelles ne peuvent aider qu’une petite fraction des patients. Cette étude explore un angle différent : une forme particulière de mort cellulaire appelée ferroptose, entraînée par le fer et le stress oxydatif, afin de découvrir de nouveaux gènes cibles qui pourraient un jour protéger les cellules photoréceptrices de la rétine — quelle que soit la mutation avec laquelle une personne est née.
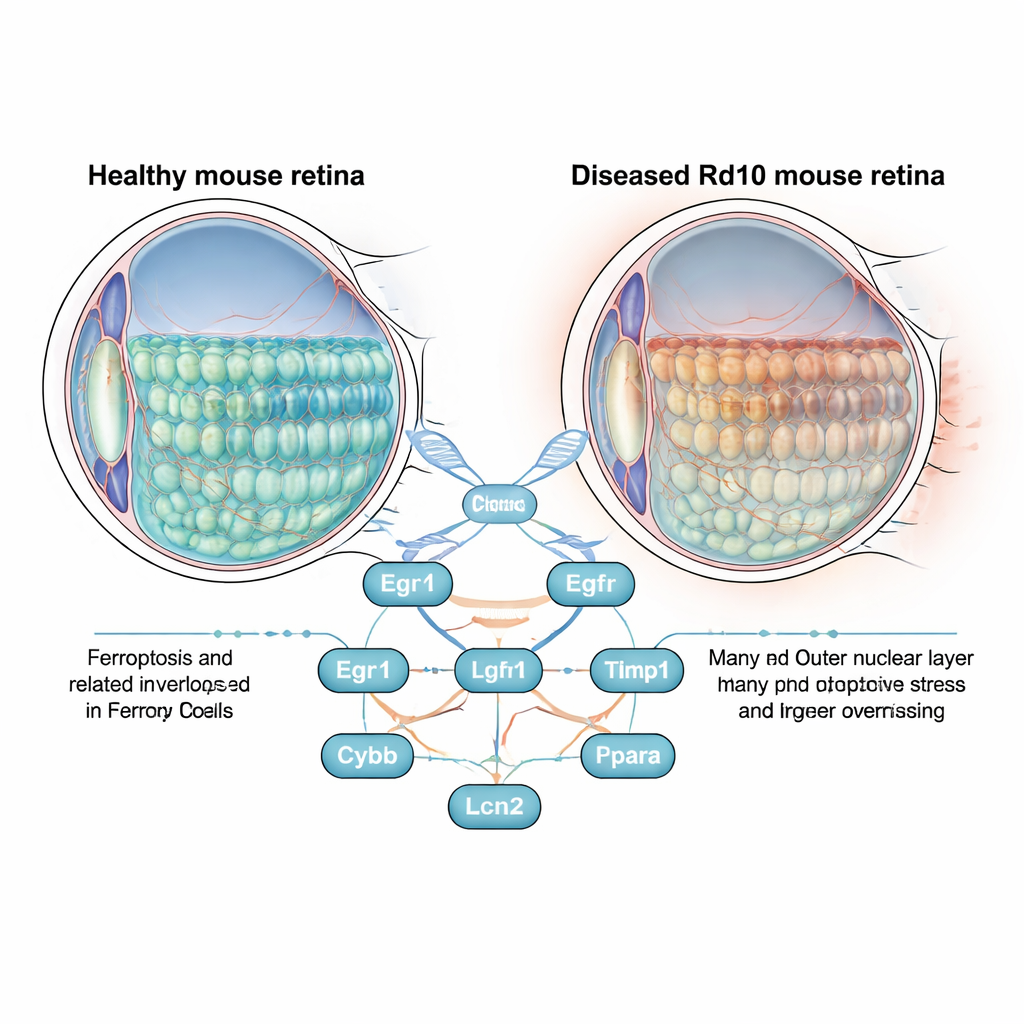
Un examen approfondi d’une maladie oculaire aveuglante
La rétine est une fine couche de tissu au fond de l’œil qui contient les photorécepteurs bâtonnets et cônes, les cellules qui transforment la lumière en signaux électriques. Dans la rétinite pigmentaire, ces cellules meurent lentement, privant d’abord les patients de la vision nocturne et périphérique, puis de la vision centrale. Les scientifiques étudient souvent ce processus chez la souris Rd10, qui porte une mutation reproduisant fidèlement la maladie humaine. Plutôt que de se concentrer uniquement sur le gène défectueux, les auteurs ont posé une question plus large : à mesure que la rétine dégénère, quels gènes liés à la ferroptose s’activent ou s’éteignent, et pourraient-ils être responsables de la perte cellulaire ?
Trouver les gènes clés dans un océan de données
L’équipe a exploité d’importants jeux de données publics d’expression génique provenant de rétines de souris saines et Rd10, prenant en quelque sorte un « instantané » global des gènes plus ou moins actifs. Ils ont identifié plus de 2 000 gènes modifiés, puis les ont recoupés avec une liste sélectionnée de gènes liés à la ferroptose. Cela a réduit la sélection à 37 candidats associés à la mort cellulaire oxydative induite par le fer. Des analyses informatiques ont montré que ces gènes se regrouperaient dans des processus tels que la réponse au stress oxydatif, la régulation de la mort neuronale et les voies du métabolisme lipidique — des marques de la ferroptose et des réponses au stress connues dans les nerfs en dégénérescence.
Huit gènes qui se distinguent
Pour identifier les acteurs les plus influents, les chercheurs ont construit un réseau d’interaction protéique et appliqué plusieurs algorithmes de classement. Huit gènes « hubs » sont apparus : Egr1, Cd44, Egfr, Tlr4, Timp1, Cybb, Lcn2 et Ppara. Sept d’entre eux étaient plus actifs dans les rétines malades, tandis que Ppara était moins actif. Le groupe a confirmé ces profils dans un jeu de données indépendant puis a examiné de plus près la localisation des gènes principaux dans l’œil. À l’aide de marquages fluorescents et de séquençage ARN unicellulaire, ils ont montré que Egr1 est fortement augmenté dans les photorécepteurs bâtonnets et cônes, tandis que Cd44 est fortement élevé dans les cellules de Müller, les cellules gliales de soutien qui traversent la rétine. Cela suggère que les photorécepteurs stressés et leurs cellules de soutien peuvent coopérer — peut‑être de façon néfaste — via des voies liées à la ferroptose.
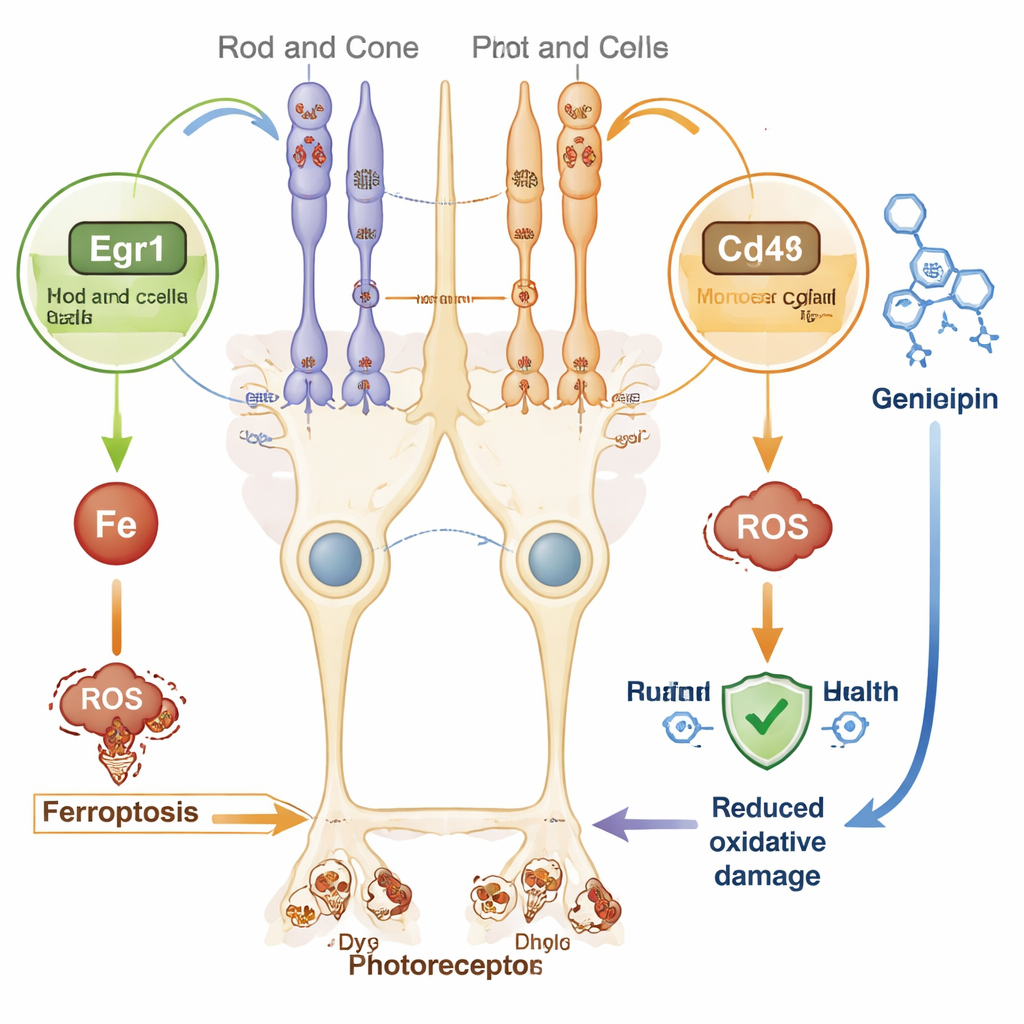
Ce que cela signifie pour les traitements futurs
Comme la thérapie génique adaptée à chaque gène défectueux est complexe et coûteuse, des stratégies à large spectre sont attrayantes. La signature génique nouvellement identifiée suggère plusieurs de ces pistes. Par exemple, Egr1 est un commutateur d’action rapide qui répond au stress oxydatif et peut favoriser la ferroptose dans d’autres organes. Cd44, une molécule de surface des cellules de Müller, a été montrée dans différents tissus comme aggravant la surcharge en fer et la mort cellulaire. Parallèlement, la diminution de Ppara, régulateur du métabolisme lipidique et de l’utilisation énergétique, pourrait rendre les cellules rétiniennes plus vulnérables aux dégâts. En ciblant ces voies de stress partagées, il pourrait être possible de ralentir la dégénérescence rétinienne dans de nombreuses formes génétiques de la rétinite pigmentaire.
Médicaments susceptibles d’aider à protéger la vision
En utilisant une base de données d’interactions médicament–gène, les auteurs ont recherché des composés pouvant influencer Egr1 ou Cd44. Plusieurs molécules existantes sont apparues, y compris le composé naturel genipine, qui a montré des effets protecteurs dans des modèles de la maladie de Parkinson, de dégénérescence nerveuse et de rétinopathie diabétique en atténuant le stress oxydatif et l’inflammation. Bien qu’aucun de ces médicaments candidats n’ait encore été testé dans ce modèle murin spécifique de rétinite pigmentaire, ils constituent des points de départ prometteurs pour des études précliniques et animales futures visant à protéger les photorécepteurs de la ferroptose.
Message essentiel pour les non‑spécialistes
Ce travail montre que la mort cellulaire oxydative liée au fer est étroitement liée aux changements d’activité génique observés dans un modèle classique de cécité héréditaire. En isolant huit gènes clés, et en particulier Egr1, réactif au stress dans les photorécepteurs, et Cd44 dans les cellules de Müller, l’étude ouvre de nouveaux horizons pour des thérapies potentielles qui ne reposent pas sur la correction d’un seul gène muté. Si des expériences futures confirment que calmer la ferroptose via ces cibles peut maintenir les cellules rétiniennes en vie, cela pourrait ouvrir la voie à des traitements bénéfiques pour un large éventail de patients confrontés à une perte progressive de la vision.
Citation: Qiu, X., Fu, XW., Lei, XL. et al. Identification and validation of a novel ferroptosis-related gene signature associated with inherited retinal degeneration in Rd10 mice. Sci Rep 16, 6992 (2026). https://doi.org/10.1038/s41598-026-38193-4
Mots-clés: rétinite pigmentaire, ferroptose, photorécepteurs, dégénérescence rétinienne, Egr1 Cd44