Clear Sky Science · fr
La métabolomique intégrée et le séquençage 16S rRNA révèlent le mécanisme des flavones totales d’Abelmoschus manihot (L.) Medic contre la fibrose hépatique
La puissance de la fleur pour un foie cicatrisé
La cicatrisation du foie, ou fibrose, est un danger silencieux qui peut lentement évoluer vers la cirrhose et l’insuffisance hépatique. La médecine moderne manque encore de médicaments sûrs et globalement efficaces pour arrêter ou inverser ce processus. Cette étude examine si des composés naturels issus des fleurs jaune vif d’Abelmoschus manihot — une plante utilisée en médecine traditionnelle chinoise notamment pour les maladies rénales — peuvent protéger le foie contre des lésions toxiques chroniques, et comment ils pourraient le faire en agissant à la fois sur la chimie corporelle et sur les microbes de notre intestin.
Un problème hépatique mondial en expansion
Des centaines de millions de personnes dans le monde vivent avec une maladie hépatique chronique due aux virus, à l’alcool, à l’accumulation de graisses ou à des toxines. Lorsque le foie est blessé à plusieurs reprises, il réagit en déposant du tissu cicatriciel, un peu comme une plaie qui ne guérit jamais complètement. Avec le temps, cette fibrose peut raidir l’organe, entraver la circulation sanguine et évoluer vers la cirrhose, une cause majeure de mortalité liée au foie. Parce que de nombreux facteurs peuvent simultanément causer ce dommage, les chercheurs s’intéressent particulièrement aux mélanges d’origine végétale capables d’agir sur plusieurs cibles à la fois, plutôt qu’aux médicaments à molécule unique qui n’atteignent qu’une seule voie.
Tester un remède traditionnel chez la souris
L’équipe s’est concentrée sur les « flavones totales » d’Abelmoschus manihot (TFA) — un mélange concentré de sept composés végétaux apparentés, déjà montrés anti‑inflammatoires et antioxydants. Ils ont utilisé un modèle murin bien établi dans lequel une exposition répétée au tétrachlorure de carbone (CCl4), un produit industriel, provoque une lésion hépatique chronique et une fibrose similaires à celles observées chez l’humain. Des souris mâles ont été réparties en groupes : témoins sains, souris « modèle » exposées au CCl4, un groupe traité par un médicament standard, et trois groupes recevant des doses différentes de TFA. Après des semaines d’exposition au CCl4, les chercheurs ont administré le TFA par voie orale puis examiné le sang, les tissus hépatiques et le contenu intestinal des animaux.
Des analyses sanguines plus nettes et un tissu hépatique plus sain
Le TFA a montré des effets protecteurs marqués. Les taux sanguins des enzymes hépatiques ALT et AST — indicateurs cliniques de lésion des cellules hépatiques — ont fortement augmenté chez les souris exposées au CCl4, mais ont diminué d’environ moitié chez les animaux ayant reçu du TFA. L’examen microscopique confirmait ces observations : les foies fibrosés non traités présentaient une architecture déformée, des cellules mortes, d’importants dépôts de collagène et des foyers inflammatoires. Les foies traités par TFA présentaient moins de « pseudo‑lobules » cicatriciels, une coloration au collagène réduite et moins de signes de mort cellulaire. Les marqueurs de stress oxydatif se sont également améliorés : les défenses antioxydantes (SOD et GSH‑Px) ont augmenté, tandis que les produits nocifs (MDA) ont chuté. Des médiateurs inflammatoires clés, dont TNF‑α, IL‑6 et TGF‑β1, ont aussi été abaissés, de même que des marqueurs chimiques de la fibrose tels que l’hydroxyproline, le collagène IV et l’acide hyaluronique.
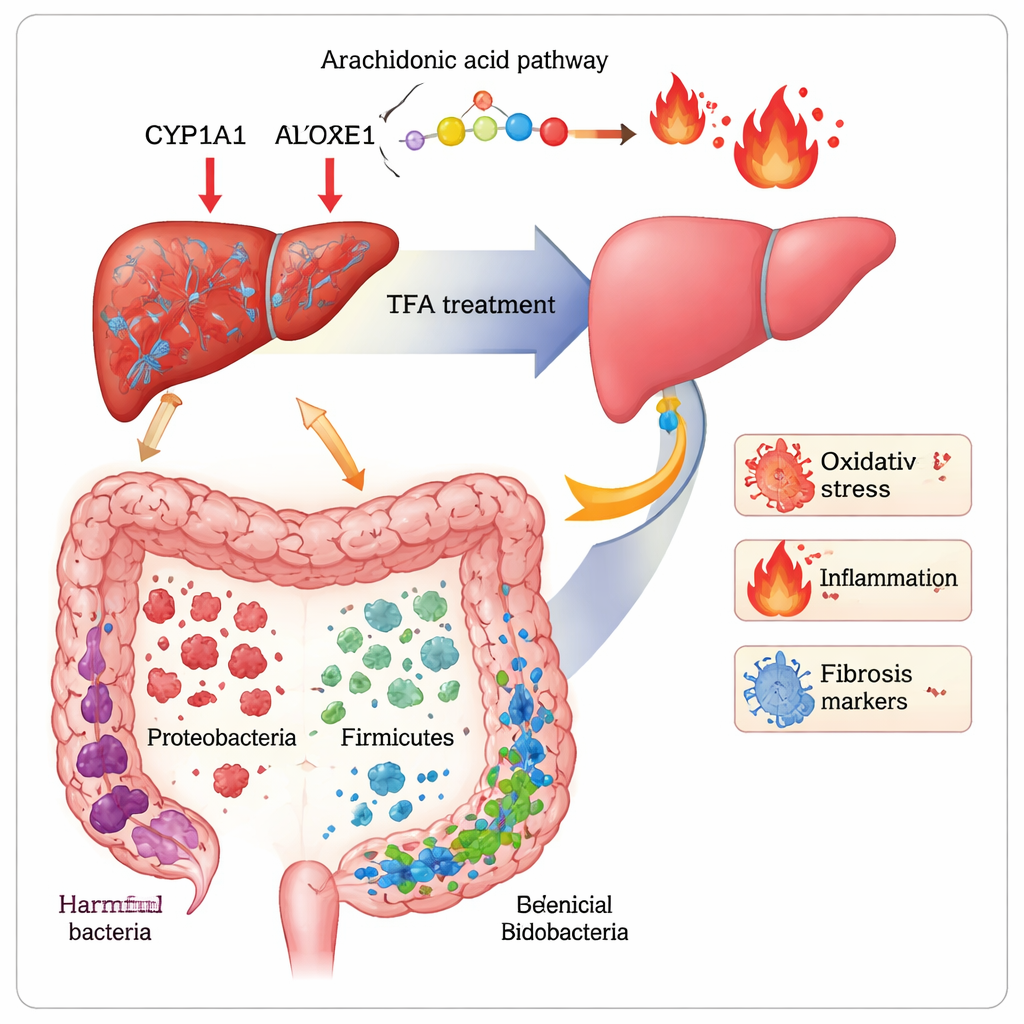
Rééquilibrer la chimie corporelle et les microbes intestinaux
Pour comprendre comment le TFA produit ces bénéfices, les chercheurs ont combiné deux outils puissants : la métabolomique, qui profile des centaines de petites molécules dans le sang, et le séquençage 16S rRNA, qui cartographie les types de bactéries présentes dans l’intestin. Chez les souris fibrosées, des dizaines de métabolites impliqués dans le métabolisme des lipides et la dégradation des acides aminés étaient perturbés. Le TFA a partiellement rétabli l’équilibre dans des voies liées aux membranes cellulaires (glycérophospholipides), à l’acide aminé lié à l’humeur tryptophane, et à un acide gras appelé acide arachidonique, précurseur de signaux inflammatoires. Les niveaux de deux produits de l’acide arachidonique, 20‑HETE et 16(R)‑HETE — tous deux associés au stress oxydatif et à la fibrose — ont été ramenés vers la normale. Dans le foie, le TFA a diminué l’abondance de trois enzymes (CYP1A1, CYP2E1, ALOX15) qui contribuent à la génération de ces molécules nocives. Parallèlement, le CCl4 perturbait le microbiote intestinal, réduisant des groupes bénéfiques tels que les Firmicutes, Lactobacillus et Bifidobacterium et permettant à des Proteobacteria potentiellement nuisibles de proliférer. Le TFA a inversé une grande partie de ce déséquilibre, augmentant la diversité et rétablissant des bactéries « amies » associées à une meilleure fonction de barrière et à une inflammation moindre.
Une stratégie multi‑cible sur l’autoroute intestin–foie
En reliant les changements bactériens aux signatures chimiques sanguines et aux marqueurs de la maladie, l’étude suggère que le TFA agit le long de l’« axe intestin–foie » — l’autoroute active des signaux, nutriments et toxines allant de l’intestin au foie. Les bactéries et leurs produits nocifs semblent corrélés à une inflammation et une cicatrisation plus importantes, tandis que les microbes bénéfiques s’associent à des profils métaboliques plus sains et à moins de fibrose. Le TFA semble pousser l’ensemble de ce système vers un meilleur équilibre : il renforce les défenses antioxydantes, calme les voies inflammatoires alimentées par l’acide arachidonique, reconfigure la communauté microbienne intestinale et, en fin de compte, atténue la réponse de cicatrisation dans le foie.
Ce que cela pourrait signifier pour les traitements futurs
Pour le grand public, le message essentiel est qu’un extrait floral utilisé de longue date en médecine traditionnelle a montré un réel potentiel dans un test moderne et rigoureux de la cicatrisation hépatique chronique. Chez la souris, le TFA n’a pas seulement protégé les cellules hépatiques — il a simultanément réduit la chimie toxique et les microbes intestinaux nuisibles. Si ces résultats ne prouvent pas encore un bénéfice chez l’être humain, et n’ont été obtenus que chez des animaux mâles et pour un type unique de lésion hépatique, ils mettent en évidence une thérapie multi‑cible potentielle qui agit avec les réseaux biologiques du corps plutôt que contre une seule molécule. Avec des investigations supplémentaires, de telles flavones d’origine végétale pourraient un jour faire partie d’un arsenal plus large pour ralentir ou même inverser la fibrose hépatique.
Citation: Li, D., Ge, H., Zhang, Y. et al. Integrated metabolomics and 16S rRNA sequencing reveal the mechanism of total flavones of Abelmoschus manihot (L.) Medic against liver fibrosis. Sci Rep 16, 7342 (2026). https://doi.org/10.1038/s41598-026-38192-5
Mots-clés: fibrose hépatique, microbiote intestinal, métabolomique, flavonoïdes, médecine traditionnelle chinoise